Clear Sky Science · it
Il LPS di Klebsiella pneumoniae induce la repressione stromale di p53 e la chemioresistenza nel cancro colorettale
Perché i batteri intestinali contano nel trattamento del cancro
Il cancro colorettale è di norma trattato con potenti farmaci chemioterapici, ma molti tumori imparano a sopravvivere a questi attacchi. Questo studio esplora un complice inaspettato: alcuni batteri intestinali. I ricercatori mostrano come molecole prodotte da questi microbi possano indebolire silenziosamente una delle principali difese anticancro del nostro organismo all’interno dei tumori, rendendo i trattamenti standard meno efficaci—anche quando le cellule tumorali non sono direttamente contattate dai batteri.
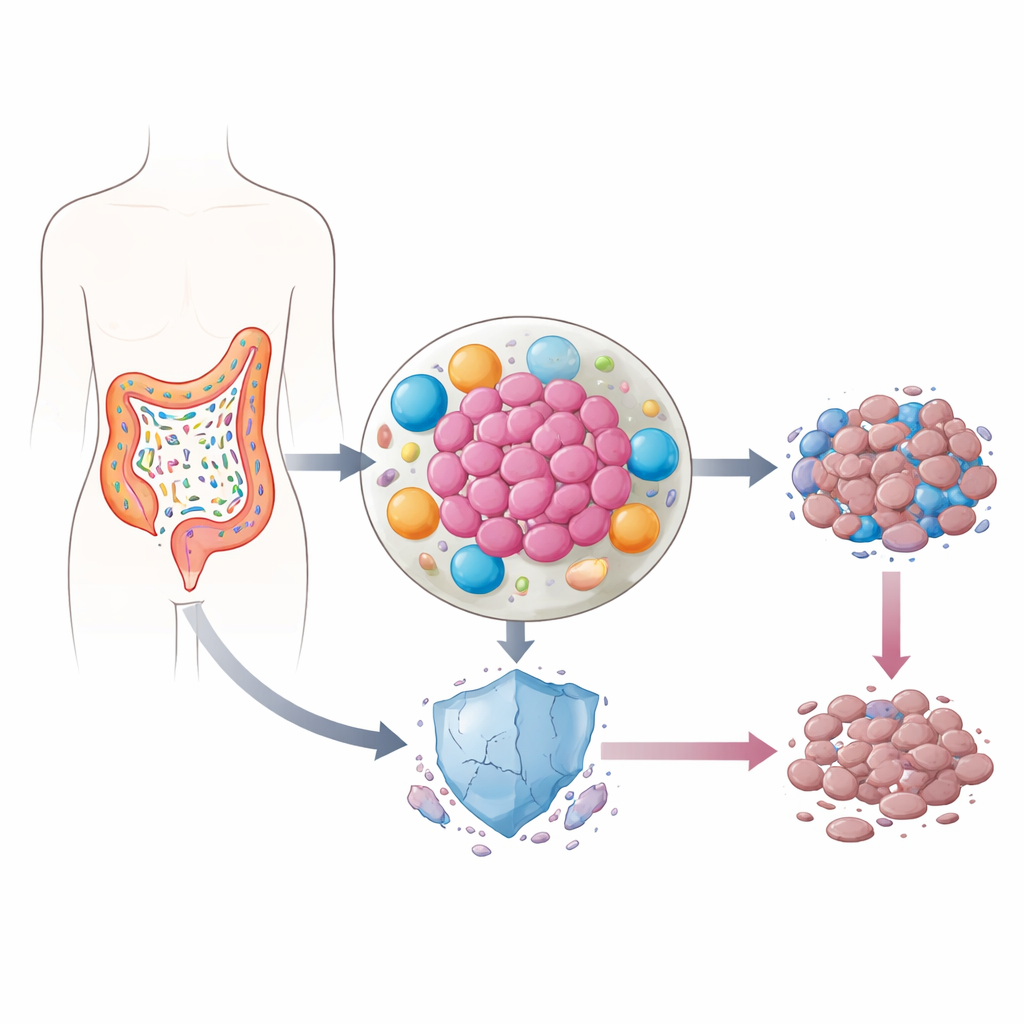
Germi che vivono all’interno dei tumori
Il nostro intestino ospita trilioni di batteri, la maggior parte innocui o addirittura utili. Nel cancro colorettale, tuttavia, l’equilibrio delle specie spesso cambia. Alcuni batteri si spostano all’interno del tumore, dove rilasciano molecole infiammatorie e rimodellano il quartiere cellulare che circonda il cancro. Lavori precedenti avevano suggerito che in queste nicchie infiammate i livelli di p53—una proteina spesso definita “guardiano del genoma” perché aiuta le cellule danneggiate ad autodistruggersi—sono insolitamente bassi. Dato che p53 è cruciale per la risposta delle cellule tumorali alla chemioterapia, gli autori si sono chiesti se i batteri intestinali potessero sabotare silenziosamente questa salvaguardia.
Una rete di supporto nascosta attorno alle cellule tumorali
Il team si è concentrato sul lipopolisaccaride (LPS), una forte molecola infiammatoria presente sulla superficie di comuni microbi intestinali come Klebsiella pneumoniae e altri Enterobatteri, spesso aumentati nel cancro colorettale. Sorprendentemente, quando hanno aggiunto LPS direttamente alle cellule di cancro colorettale, non è successo molto: le cellule non sono diventate più resistenti ai farmaci e i livelli di p53 sono rimasti gli stessi. Il quadro è cambiato completamente quando hanno prima esposto cellule immunitarie chiamate macrofagi o cellule del tessuto connettivo chiamate fibroblasti a LPS, e poi hanno trasferito il liquido in cui queste cellule erano cresciute alle cellule tumorali. In queste condizioni, la chemioterapia ha ucciso molte meno cellule tumorali e la proteina p53 non è riuscita a accumularsi come normalmente succede dopo il trattamento.
Messaggi confezionati in piccole vescicole
Per capire cosa inviassero i macrofagi, i ricercatori hanno usato analisi proteiche avanzate per mappare migliaia di cambiamenti all’interno delle cellule tumorali trattate sia con chemioterapia sia con le secrezioni dei macrofagi stimolati con LPS. Hanno osservato un chiaro schema: i segnali legati all’infiammazione e all’attivazione immune aumentavano, mentre molte vie controllate da p53 coinvolte nella divisione cellulare e nell’autodistruzione regolata diminuivano. Esperimenti successivi hanno mostrato che questa soppressione non derivava dagli ormoni infiammatori classici come l’interleuchina-6. I messaggeri chiave erano invece piccole bolle di membrana, note come vescicole extracellulari, rilasciate dai macrofagi attivati. Quando queste vescicole sono state isolate e aggiunte alle cellule tumorali, la proteina p53 è risultata destabilizzata e più rapidamente degradata dal sistema di riciclo cellulare, proteggendo così le cellule dalla morte indotta da p53.
Un silenziamento selettivo del guardiano della cellula
Gli autori hanno scoperto che questo segnale batterico–stromale non spegne semplicemente p53 ovunque. Piuttosto, attenua selettivamente un gruppo di geni controllati da p53, lasciandone altri—soprattutto quelli legati all’infiammazione—inalterati o addirittura potenziati. Analizzando campioni tumorali di pazienti con cancro colorettale, hanno trovato un modello corrispondente: nei tumori dove le firme geniche legate all’infiammazione erano elevate, questo gruppo di geni legati all’attività di p53 tendeva a essere basso, particolarmente nei tumori che conservavano un gene TP53 intatto. Importante, i pazienti i cui tumori mostravano una forte espressione di questo cluster dipendente da p53 tendevano ad avere esiti migliori alla chemioterapia rispetto a chi presentava una bassa espressione, suggerendo che il silenziamento non genetico di p53 da parte di un microambiente tumorale infiammato può peggiorare gli esiti clinici.
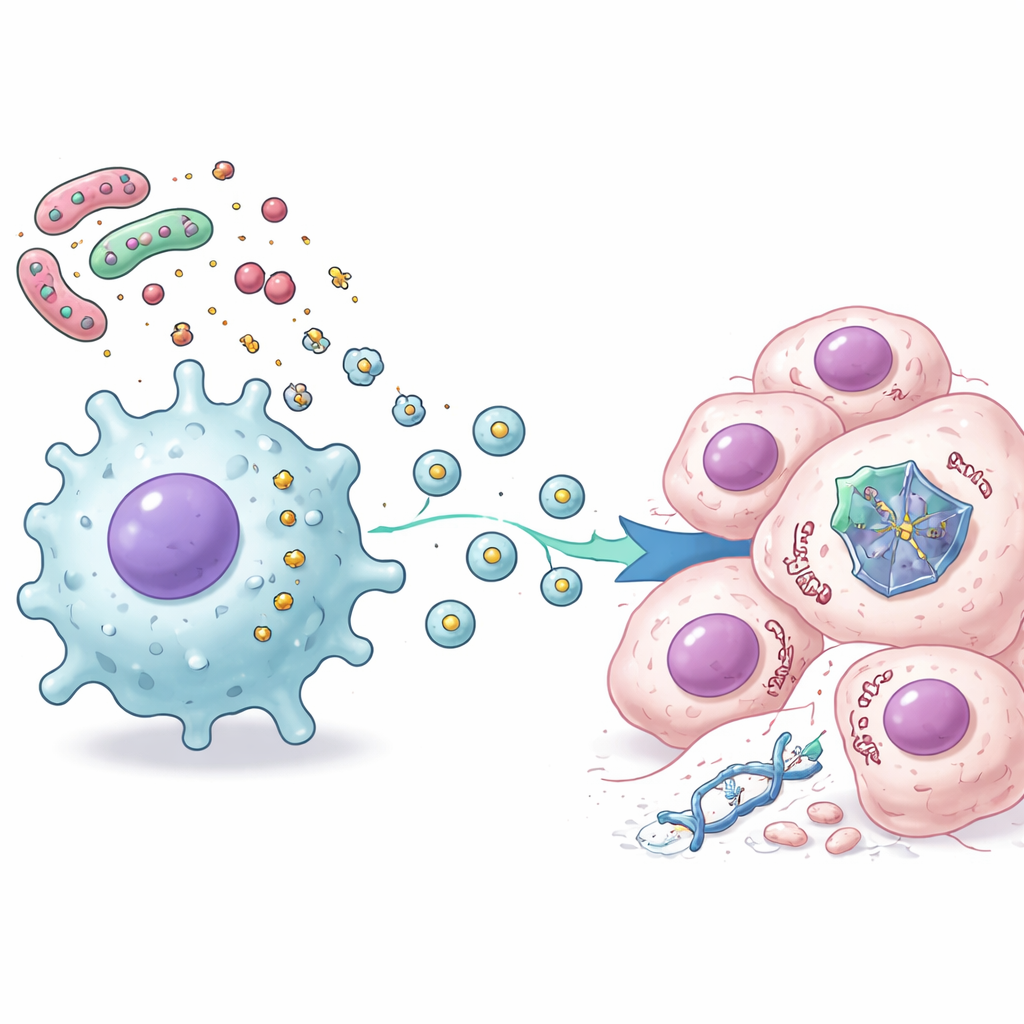
Cosa significa questo per pazienti e terapie
Complessivamente, il lavoro rivela una catena di eventi che collega i batteri intestinali alla resistenza alla chemioterapia: il LPS batterico attiva le cellule stromali e immunitarie vicine, queste cellule rilasciano vescicole extracellulari e le vescicole entrano nelle cellule tumorali destabilizzando la proteina p53 e attenuando le sue decisioni di vita o morte dopo il trattamento. Anche quando il gene p53 è normale, questa pressione esterna può effettivamente mettere a tacere il suo ruolo protettivo. Per i pazienti, ciò suggerisce che lo stato del microbioma intestinale e l’infiammazione locale potrebbero contribuire a spiegare perché alcuni tumori colorettali resistono ai farmaci standard. In futuro, strategie che rimodulano i batteri intestinali, placano l’infiammazione dannosa o bloccano la produzione o l’azione di queste vescicole potrebbero aiutare a ripristinare il potere soppressore tumorale di p53 e rendere più efficaci le chemioterapie esistenti.
Citazione: Fragkoulis, K., Łasut-Szyszka, B., Végvári, Á. et al. Klebsiella pneumoniae LPS drives stromal-mediated repression of p53 and colorectal cancer chemoresistance. Cell Death Dis 17, 395 (2026). https://doi.org/10.1038/s41419-026-08756-4
Parole chiave: cancro colorettale, microbioma intestinale, resistenza alla chemioterapia, soppressore tumorale p53, microambiente tumorale