Clear Sky Science · fr
Le LPS de Klebsiella pneumoniae induit dans le stroma la répression de p53 et la chimiorésistance du cancer colorectal
Pourquoi vos bactéries intestinales comptent pour le traitement du cancer
Le cancer colorectal est généralement traité par des médicaments de chimiothérapie puissants, mais de nombreuses tumeurs apprennent à survivre à ces attaques. Cette étude explore un complice inattendu : certaines bactéries intestinales. Les chercheurs montrent comment des molécules issues de ces microbes peuvent affaiblir en silence l’un des principaux dispositifs de défense anticancer de notre organisme au sein des tumeurs, rendant les traitements standards moins efficaces — même lorsque les cellules cancéreuses elles‑mêmes ne sont pas directement atteintes par les bactéries.
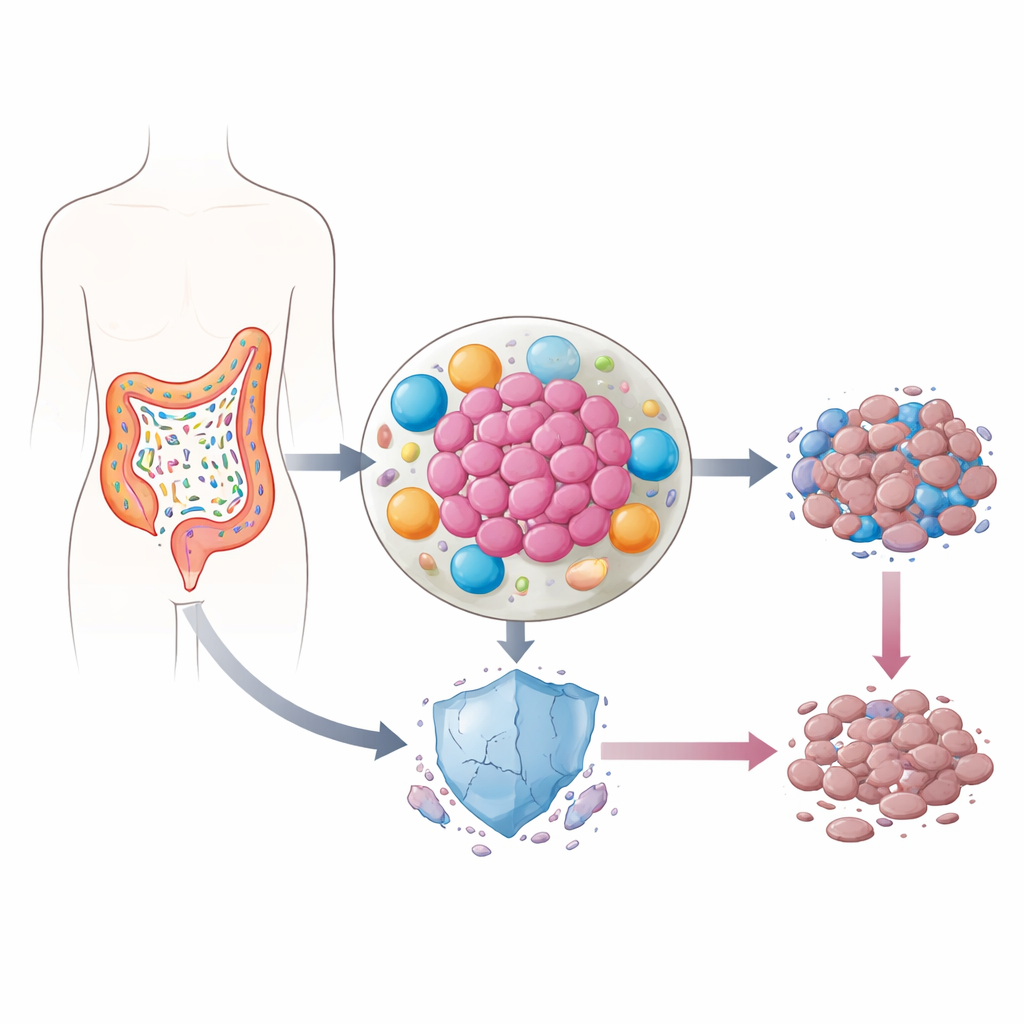
Des germes vivant à l’intérieur des tumeurs
Nos intestins hébergent des billions de bactéries, la plupart inoffensives voire bénéfiques. Dans le cancer colorectal, cependant, l’équilibre des espèces se modifie souvent. Certaines bactéries envahissent la tumeur elle‑même, y libèrent des molécules inflammatoires et remodèlent le voisinage cellulaire qui entoure le cancer. Des travaux antérieurs ont suggéré que dans ces niches enflammées, les niveaux de p53 — une protéine souvent qualifiée de « gardien du génome » parce qu’elle aide les cellules endommagées à s’autodétruire — sont anormalement bas. Comme p53 est crucial pour la réponse des cellules cancéreuses à la chimiothérapie, les auteurs se sont demandé si les bactéries intestinales ne sabotaient pas discrètement cette garde.
Un réseau de soutien caché autour des cellules tumorales
L’équipe s’est focalisée sur le lipopolysaccharide (LPS), une molécule inflammatoire puissante présente à la surface de microbes intestinaux courants comme Klebsiella pneumoniae et d’autres entérobactéries, souvent enrichies dans le cancer colorectal. De façon surprenante, lorsqu’ils ont ajouté du LPS directement aux cellules de cancer colorectal, rien de notable ne s’est produit : les cellules ne sont pas devenues plus résistantes aux médicaments et les niveaux de p53 sont restés inchangés. Le tableau a complètement changé lorsqu’ils ont d’abord exposé des cellules immunitaires appelées macrophages ou des cellules du tissu conjonctif appelées fibroblastes au LPS, puis transféré le liquide dans lequel ces cellules avaient été cultivées aux cellules cancéreuses. Dans ces conditions, la chimiothérapie a tué beaucoup moins de cellules tumorales, et la protéine p53 n’a pas pu s’accumuler comme elle le ferait normalement après le traitement.
Des messages emballés dans de minuscules vésicules
Pour comprendre ce que les macrophages envoyait, les chercheurs ont utilisé une analyse protéique avancée pour cartographier des milliers de changements à l’intérieur des cellules cancéreuses traitées à la fois par la chimiothérapie et par les sécrétions de macrophages stimulés au LPS. Ils ont observé un schéma clair : les signaux liés à l’inflammation et à l’activation immune augmentaient, tandis que de nombreuses voies contrôlées par p53 impliquées dans la division cellulaire et l’autodestruction régulée diminuaient. Des expériences complémentaires ont montré que cette suppression ne provenait pas des hormones inflammatoires classiques comme l’interleukine‑6. En revanche, les messagers clés étaient de minuscules bulles membranaires, dites vésicules extracellulaires, libérées par les macrophages activés. Lorsque ces vésicules ont été isolées et ajoutées aux cellules cancéreuses, la protéine p53 a été déstabilisée et détruite plus rapidement par le système de recyclage de la cellule, protégeant ainsi les cellules d’une mort dirigée par p53.
Un silencement sélectif du gardien cellulaire
Les auteurs ont découvert que ce signal bactérien‑stromal n’éteint pas simplement p53 partout. Il atténue de manière sélective un groupe de gènes contrôlés par p53, tout en laissant d’autres — en particulier ceux liés à l’inflammation — inchangés ou même renforcés. En examinant des échantillons tumoraux de patients atteints de cancer colorectal, ils ont trouvé un motif similaire : dans les tumeurs où les signatures géniques liées à l’inflammation étaient élevées, ce groupe de gènes dépendant de l’activité de p53 avait tendance à être bas, particulièrement dans les cancers conservant un gène TP53 intact. Fait important, les patients dont les tumeurs présentaient une forte expression de ce groupe de gènes dépendant de p53 s’en sortaient généralement mieux avec la chimiothérapie que ceux ayant une faible expression, ce qui suggère que le silencement non génétique de p53 par un microenvironnement tumoral enflammé peut aggraver les résultats cliniques.
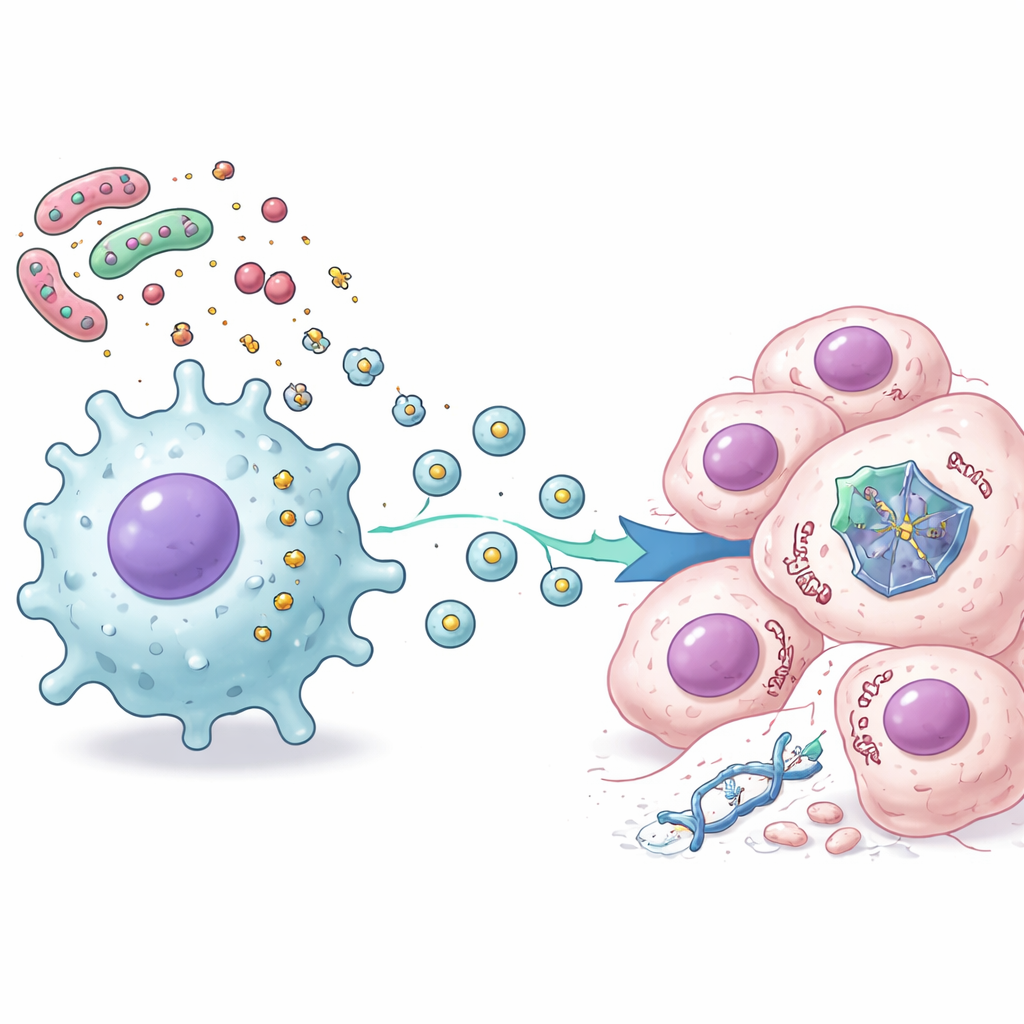
Ce que cela signifie pour les patients et les thérapies
Ensemble, les travaux révèlent une chaîne d’événements liant les bactéries intestinales à la résistance à la chimiothérapie : le LPS bactérien active les cellules stromales et immunitaires voisines, ces cellules libèrent des vésicules extracellulaires, et les vésicules pénètrent dans les cellules cancéreuses pour déstabiliser la protéine p53 et affaiblir ses décisions de vie ou de mort après le traitement. Même lorsque le gène p53 est normal, cette pression extérieure peut effectivement réduire son rôle protecteur. Pour les patients, cela suggère que l’état du microbiote intestinal et l’inflammation locale pourraient aider à expliquer pourquoi certaines tumeurs colorectales résistent aux médicaments standards. À l’avenir, des stratégies visant à remodeler les bactéries intestinales, calmer l’inflammation nocive ou bloquer la production ou l’action de ces vésicules pourraient aider à restaurer le pouvoir suppresseur de tumeur de p53 et améliorer l’efficacité des chimiothérapies existantes.
Citation: Fragkoulis, K., Łasut-Szyszka, B., Végvári, Á. et al. Klebsiella pneumoniae LPS drives stromal-mediated repression of p53 and colorectal cancer chemoresistance. Cell Death Dis 17, 395 (2026). https://doi.org/10.1038/s41419-026-08756-4
Mots-clés: cancer colorectal, microbiote intestinal, résistance à la chimiothérapie, suppresseur de tumeur p53, microenvironnement tumoral