Clear Sky Science · es
El LPS de Klebsiella pneumoniae impulsa la represión estromal de p53 y la quimiorresistencia en cáncer colorrectal
Por qué importan tus bacterias intestinales para el tratamiento del cáncer
El cáncer colorrectal suele tratarse con fármacos quimioterapéuticos potentes, pero muchos tumores aprenden a sobrevivir a estos ataques. Este estudio explora un cómplice inesperado: ciertas bacterias del intestino. Los investigadores muestran cómo moléculas procedentes de estos microbios pueden debilitar silenciosamente uno de los principales mecanismos de defensa antitumoral de nuestro cuerpo dentro de los tumores, haciendo que los tratamientos estándar sean menos eficaces, incluso cuando las bacterias no interactúan directamente con las células cancerosas.
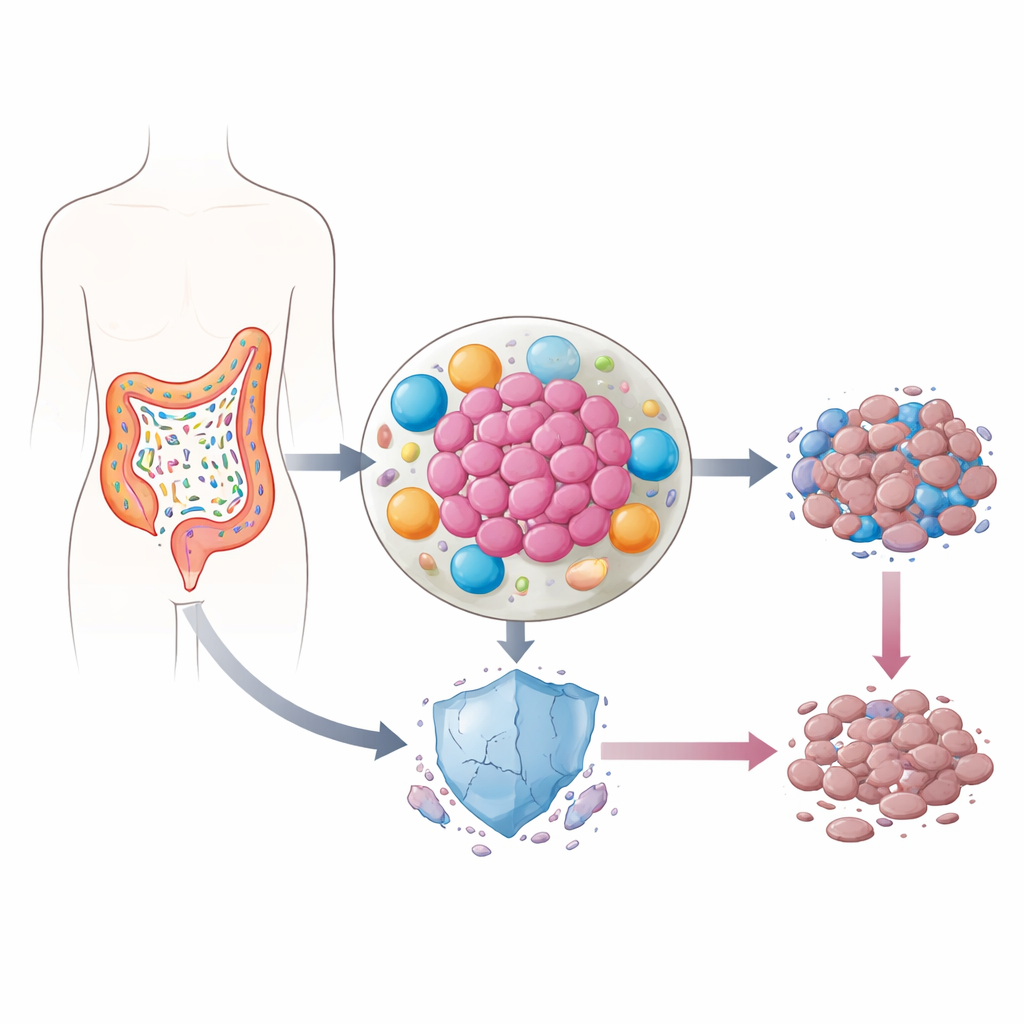
Gérmenes que viven dentro de los tumores
Nuestros intestinos albergan billones de bacterias, la mayoría inofensivas o incluso beneficiosas. En el cáncer colorrectal, sin embargo, el equilibrio de especies suele cambiar. Algunas bacterias se instalan dentro del propio tumor, donde liberan moléculas inflamatorias y remodelan el vecindario celular que rodea al cáncer. Trabajos previos sugerían que en estos nichos inflamados los niveles de p53 —una proteína a menudo llamada “guardián del genoma” porque ayuda a que las células dañadas se autodestruyan— son inusualmente bajos. Dado que p53 es crucial para la respuesta de las células cancerosas a la quimioterapia, los autores se preguntaron si las bacterias intestinales podrían estar saboteando silenciosamente esta salvaguarda.
Una red de apoyo oculta alrededor de las células tumorales
El equipo se centró en el lipopolisacárido (LPS), una potente molécula inflamatoria presente en la superficie de microbios intestinales comunes como Klebsiella pneumoniae y otras Enterobacterias, que suelen aumentar en el cáncer colorrectal. Sorprendentemente, cuando añadieron LPS directamente a células de cáncer colorrectal, no ocurrió mucho: las células no se volvieron más resistentes a los fármacos y los niveles de p53 permanecieron iguales. El panorama cambió por completo cuando primero expusieron a LPS a células inmunitarias llamadas macrófagos o a células del tejido conectivo llamadas fibroblastos, y luego transfirieron el líquido en el que habían crecido esas células a las células cancerosas. En estas condiciones, la quimioterapia mató a muchas menos células tumorales y la proteína p53 no se acumuló como normalmente lo haría tras el tratamiento.
Mensajes empaquetados en vesículas diminutas
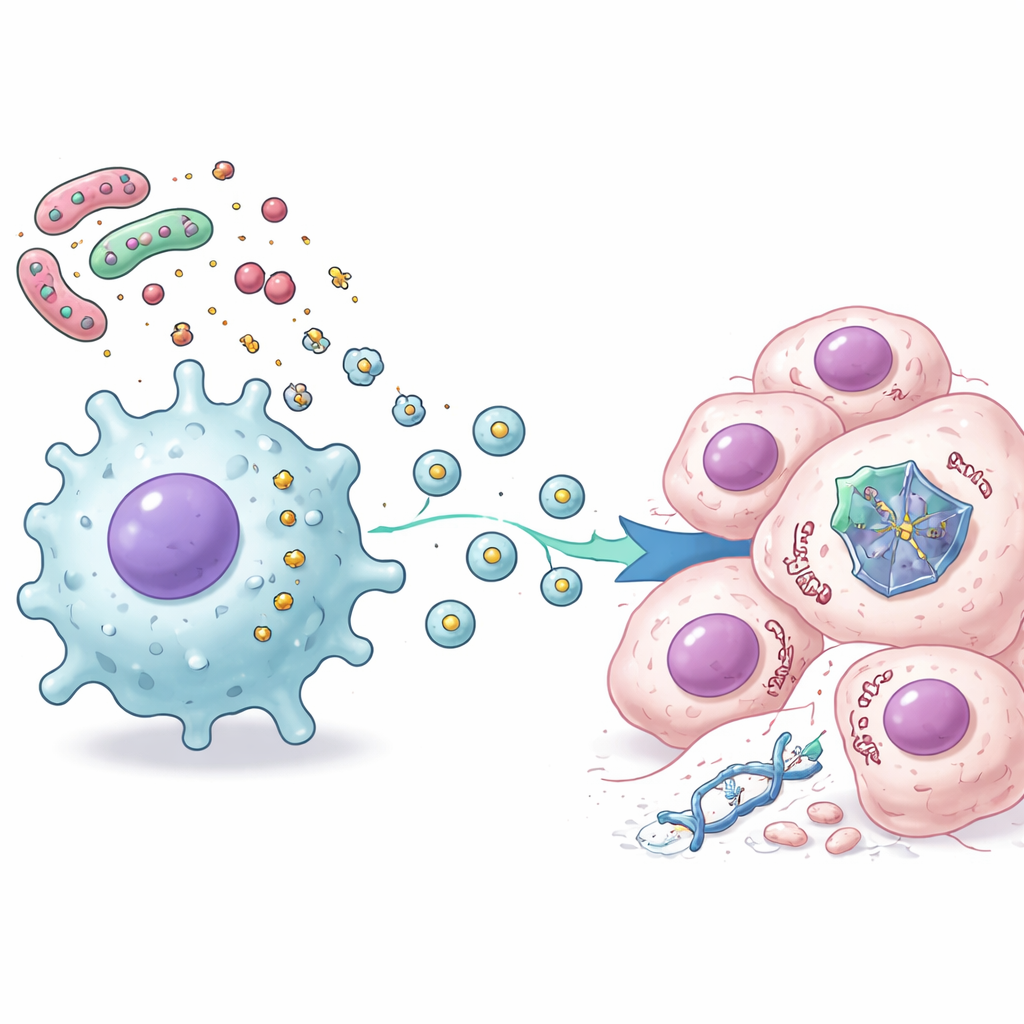
Para entender qué enviaban los macrófagos, los investigadores utilizaron un análisis proteico avanzado para trazar miles de cambios dentro de las células cancerosas tratadas con quimioterapia y con secreciones de macrófagos estimulados por LPS. Observaron un patrón claro: aumentaron las señales relacionadas con la inflamación y la activación inmune, mientras que muchas vías controladas por p53 implicadas en la división celular y la autodestrucción regulada disminuyeron. Experimentos adicionales mostraron que esta supresión no procedía de hormonas inflamatorias clásicas como la interleucina-6. En su lugar, los mensajeros clave eran pequeñas burbujas de membrana, conocidas como vesículas extracelulares, liberadas por los macrófagos activados. Cuando estas vesículas se aislaron y se añadieron a las células cancerosas, la proteína p53 se desestabilizó y fue destruida más rápidamente por la propia maquinaria de reciclaje celular, protegiendo así a las células de la muerte mediada por p53.
Un silenciamiento selectivo del guardián celular
Los autores descubrieron que esta señal bacteriana–estromal no apaga p53 por completo en todas partes. Más bien, atenúa selectivamente un grupo de genes controlados por p53, mientras deja otros —especialmente los vinculados a la inflamación— sin cambios o incluso aumentados. Al analizar muestras tumorales de pacientes con cáncer colorrectal, encontraron un patrón coincidente: en tumores donde las firmas génicas relacionadas con la inflamación eran altas, este grupo de genes de “actividad de p53” tendía a ser bajo, en particular en cánceres que conservaban un gen TP53 intacto. De forma importante, los pacientes cuyos tumores mostraban una fuerte expresión de este conjunto dependiente de p53 tendieron a responder mejor a la quimioterapia que aquellos con baja expresión, lo que sugiere que el silenciamiento no genético de p53 por el entorno tumoral inflamado puede empeorar los resultados clínicos.
Qué significa esto para pacientes y terapias
En conjunto, el trabajo revela una cadena de eventos que vincula las bacterias intestinales con la resistencia a la quimioterapia: el LPS bacteriano activa células estromales e inmunitarias cercanas, estas células liberan vesículas extracelulares, y las vesículas entran en las células cancerosas para desestabilizar la proteína p53 y atenuar sus decisiones de vida o muerte tras el tratamiento. Incluso cuando el gen p53 es normal, esta presión externa puede silenciar efectivamente su papel protector. Para los pacientes, esto sugiere que el estado del microbioma intestinal y la inflamación local podrían ayudar a explicar por qué algunos tumores colorrectales resisten los fármacos estándar. En el futuro, estrategias que modifiquen las bacterias intestinales, calmen la inflamación nociva o bloqueen la producción o acción de estas vesículas podrían ayudar a restaurar el poder supresor tumoral de p53 y mejorar la eficacia de las quimioterapias existentes.
Cita: Fragkoulis, K., Łasut-Szyszka, B., Végvári, Á. et al. Klebsiella pneumoniae LPS drives stromal-mediated repression of p53 and colorectal cancer chemoresistance. Cell Death Dis 17, 395 (2026). https://doi.org/10.1038/s41419-026-08756-4
Palabras clave: cáncer colorrectal, microbioma intestinal, resistencia a la quimioterapia, supresor tumoral p53, microambiente tumoral