Clear Sky Science · de
Klebsiella pneumoniae-LPS treibt stromal vermittelte Unterdrückung von p53 und Chemoresistenz bei kolorektalem Krebs
Warum Ihre Darmbakterien für die Krebstherapie wichtig sind
Kolorektales Karzinom wird üblicherweise mit starken Chemotherapeutika behandelt, doch viele Tumoren lernen, diesen Angriffen zu trotzen. Diese Studie untersucht einen unerwarteten Komplizen: bestimmte Darmbakterien. Die Forschenden zeigen, wie Moleküle dieser Mikroben eines der wichtigsten körpereigenen Krebsabwehrsysteme innerhalb von Tumoren still schwächen können, wodurch Standardtherapien weniger wirksam werden – selbst wenn die Krebszellen selbst nicht direkt von den Bakterien betroffen sind.
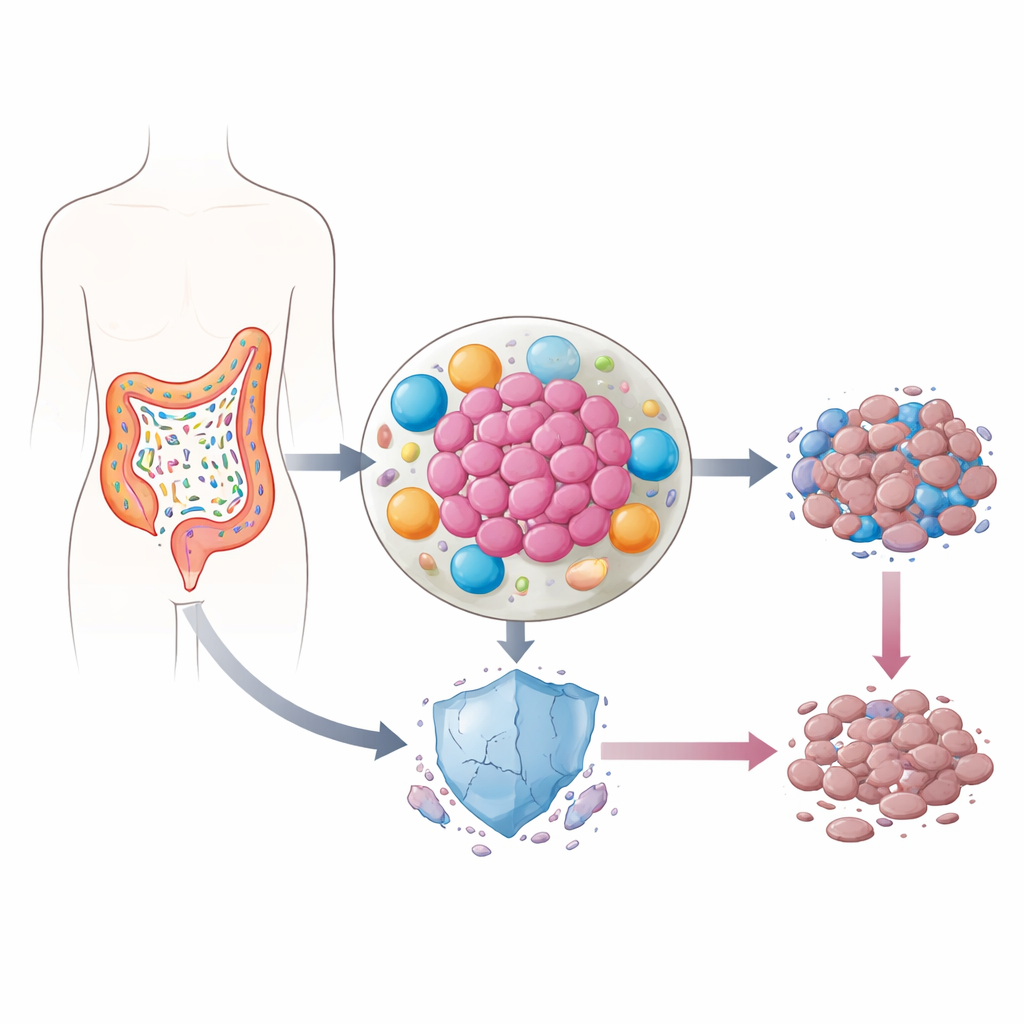
Keime, die im Tumor leben
Unser Darm beherbergt Billionen von Bakterien, die meist harmlos oder sogar nützlich sind. Bei kolorektalem Krebs verschiebt sich jedoch häufig das Gleichgewicht der Arten. Einige Bakterien dringen in den Tumor ein, wo sie entzündungsfördernde Moleküle freisetzen und die Umgebung der Tumorzellen umgestalten. Frühere Arbeiten legten nahe, dass in diesen entzündeten Bereichen die p53-Spiegel – ein Protein, das oft als „Wächter des Genoms“ bezeichnet wird, weil es geschädigte Zellen zur Selbstzerstörung bringt – ungewöhnlich niedrig sind. Da p53 für die Reaktion von Krebszellen auf Chemotherapie entscheidend ist, fragten die Autorinnen und Autoren, ob Darmbakterien dieses Schutzsystem heimlich sabotieren könnten.
Ein verstecktes Unterstützungsnetzwerk um Tumorzellen
Das Team konzentrierte sich auf Lipopolysaccharid (LPS), ein stark entzündungsförderndes Molekül auf der Oberfläche häufiger Darmkeime wie Klebsiella pneumoniae und anderer Enterobakterien, die bei kolorektalem Krebs oft vermehrt vorkommen. Überraschenderweise führte die direkte Zugabe von LPS zu kolorektalen Krebszellen zu kaum sichtbaren Effekten: Die Zellen wurden nicht widerstandsfähiger gegen Medikamente und die p53-Spiegel blieben unverändert. Das Bild änderte sich völlig, wenn man zunächst Immunzellen (Makrophagen) oder Bindegewebszellen (Fibroblasten) LPS aussetzte und dann die Flüssigkeit, in der diese Zellen kultiviert worden waren, auf die Krebszellen übertrug. Unter diesen Bedingungen tötete die Chemotherapie deutlich weniger Tumorzellen, und p53-Protein baute sich nach der Behandlung nicht wie üblich auf.
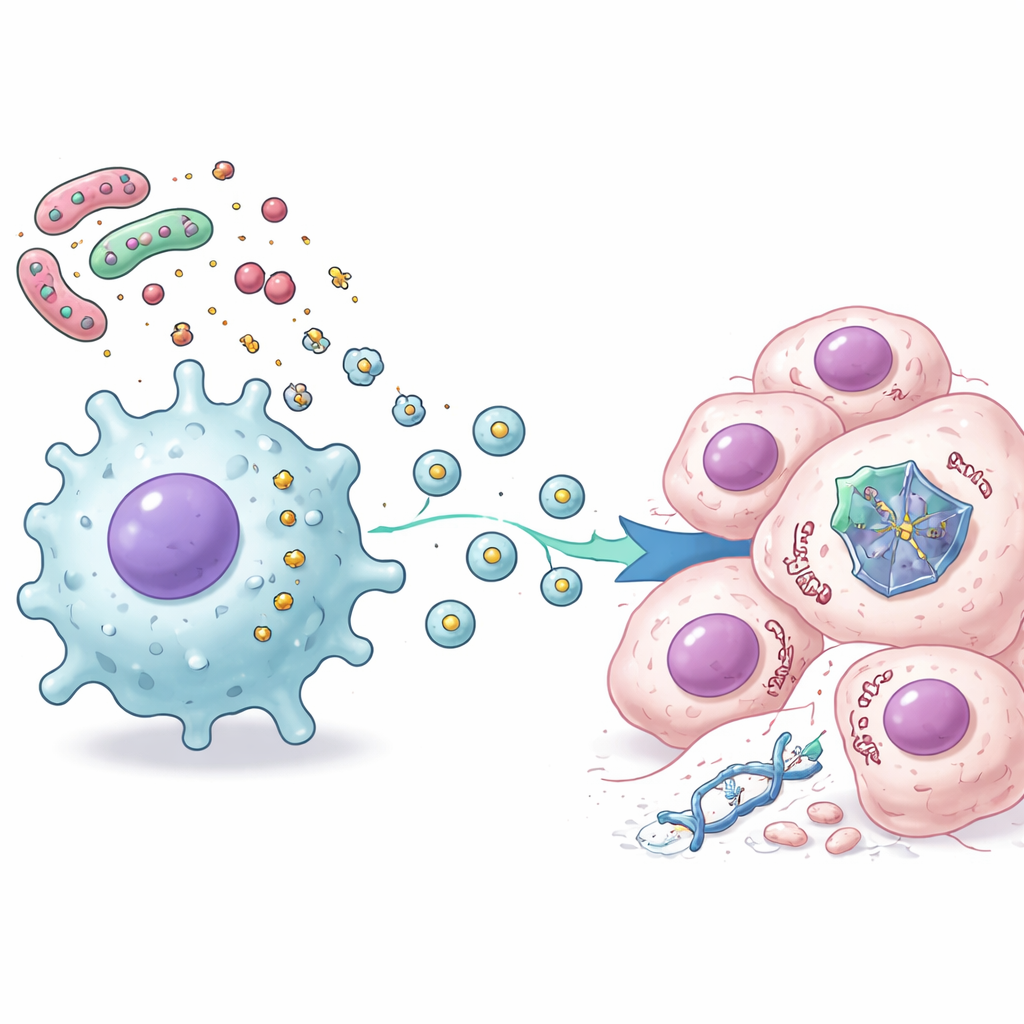
Nachrichten verpackt in winzigen Vesikeln
Um zu verstehen, was Makrophagen verschickten, nutzten die Forschenden fortgeschrittene Proteomanalysen, um Tausende von Veränderungen in Krebszellen zu kartieren, die sowohl mit Chemotherapie als auch mit LPS-aktivierten Makrophagensekreten behandelt worden waren. Sie beobachteten ein klares Muster: Signale, die mit Entzündung und Immunaktivierung zusammenhängen, stiegen an, während viele p53-gesteuerte Wege, die an Zellteilung und kontrolliertem Zelltod beteiligt sind, nachgaben. Weitere Experimente zeigten, dass diese Unterdrückung nicht von klassischen Entzündungsboten wie Interleukin-6 ausging. Stattdessen waren die Schlüsselnachrichten winzige Membranbläschen, sogenannte extrazelluläre Vesikel, die von den aktivierten Makrophagen freigesetzt wurden. Wurden diese Vesikel isoliert und zu Krebszellen gegeben, wurde p53-Protein destabilisiert und schneller vom zellulären Recyclingmechanismus abgebaut, wodurch die Zellen vor dem p53-vermittelten Zelltod geschützt waren.
Eine selektive Stummschaltung des Wächterproteins
Die Autorinnen und Autoren fanden heraus, dass dieses bakterielle–stromale Signal p53 nicht einfach überall ausschaltet. Vielmehr dämpft es selektiv eine Gruppe p53-kontrollierter Gene, während andere – insbesondere solche, die mit Entzündung verbunden sind – unverändert bleiben oder sogar verstärkt werden. Beim Blick auf Tumorproben von Patientinnen und Patienten mit kolorektalem Krebs zeigte sich ein entsprechendes Muster: In Tumoren mit hohen Entzündungs‑Genexpressionssignaturen war der „p53‑Aktivitäts“‑Gencluster tendenziell niedrig, insbesondere in Tumoren mit intaktem TP53-Gen. Wichtig ist, dass Patientinnen und Patienten, deren Tumoren eine starke Expression dieses p53‑abhängigen Clusters zeigten, tendenziell besser auf die Chemotherapie ansprachen als diejenigen mit niedriger Expression, was nahelegt, dass eine nicht‑genetische Stummschaltung von p53 durch die entzündete Tumorumgebung die klinischen Ergebnisse verschlechtern kann.
Was das für Patientinnen, Patienten und Therapien bedeutet
Insgesamt beschreibt die Arbeit eine Ablauffolge, die Darmbakterien mit Chemoresistenz verbindet: bakterielles LPS aktiviert nahegelegene stromale und Immunzellen, diese Zellen setzen extrazelluläre Vesikel frei, und die Vesikel gelangen in Krebszellen, destabilisieren p53‑Protein und schwächen dessen lebens‑oder‑tod‑Entscheidungen nach der Behandlung. Selbst wenn das p53‑Gen selbst normal ist, kann dieser äußere Druck seine Schutzfunktion effektiv zum Schweigen bringen. Für Patientinnen und Patienten legt das nahe, dass der Zustand des Darmmikrobioms und lokale Entzündungen erklären könnten, warum manche kolorektale Tumoren gegenüber Standardmedikamenten resistent sind. Zukünftige Strategien, die das Darmmikrobiom umgestalten, schädliche Entzündungen dämpfen oder die Produktion bzw. Wirkung dieser Vesikel blockieren, könnten helfen, die tumorsuppressive Kraft von p53 wiederherzustellen und bestehende Chemotherapien wirksamer zu machen.
Zitation: Fragkoulis, K., Łasut-Szyszka, B., Végvári, Á. et al. Klebsiella pneumoniae LPS drives stromal-mediated repression of p53 and colorectal cancer chemoresistance. Cell Death Dis 17, 395 (2026). https://doi.org/10.1038/s41419-026-08756-4
Schlüsselwörter: kolorektales Karzinom, Darmmikrobiom, Resistenz gegen Chemotherapie, p53-Tumorsuppressor, Tumormikroumgebung