Clear Sky Science · ru
LPS Klebsiella pneumoniae вызывает стромально-опосредованное подавление p53 и химиорезистентность при колоректальном раке
Почему кишечные бактерии важны для лечения рака
Колоректальный рак обычно лечат мощными химиотерапевтическими препаратами, но многие опухоли учатся выживать при этих атаках. В этом исследовании рассматривается неожиданный соучастник: определённые кишечные бактерии. Авторы показывают, как молекулы от этих микробов тихо ослабляют один из главных защитных механизмов организма против рака внутри опухолей, делая стандартные методы лечения менее эффективными — даже если сами раковые клетки напрямую не контактируют с бактериями.
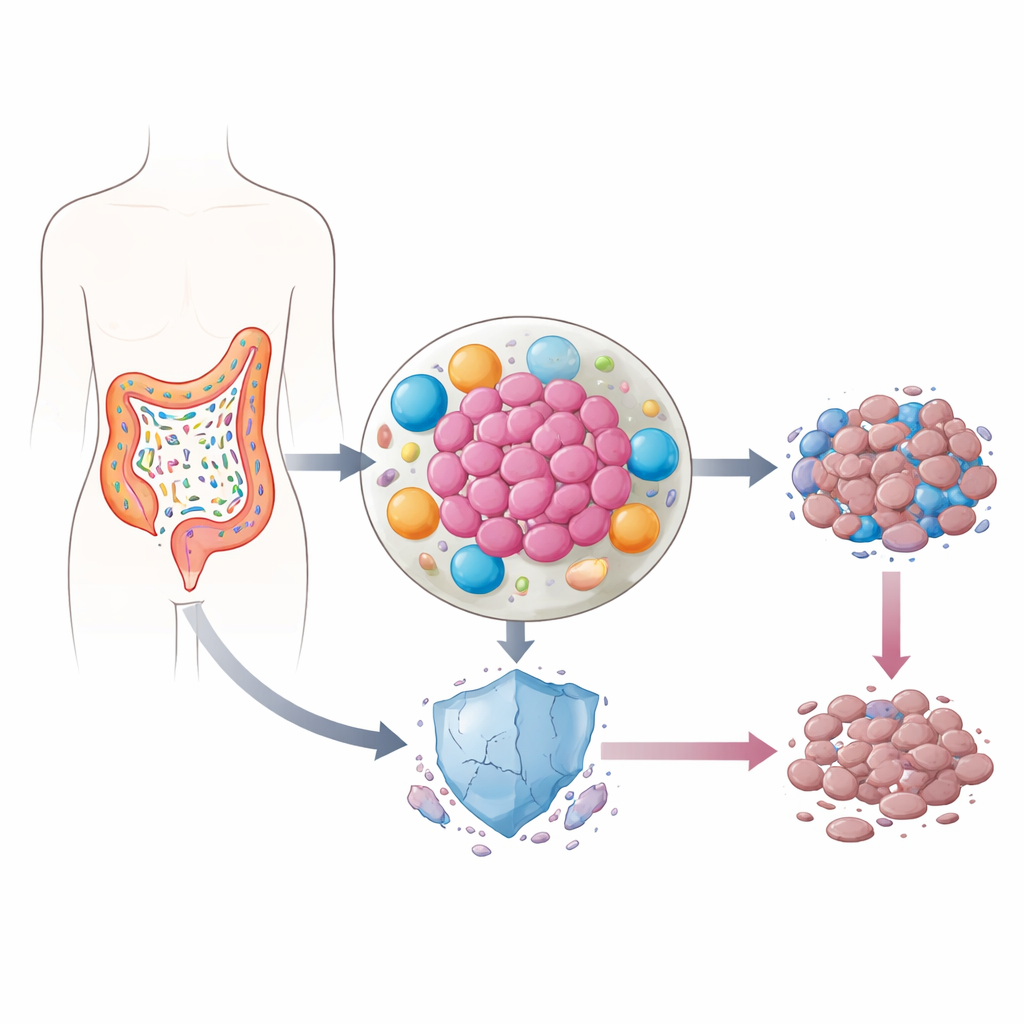
Микробы, живущие внутри опухолей
В наших кишечниках обитает триллионы бактерий, большинство из которых безвредны или даже полезны. Однако при колоректальном раке баланс видов часто смещается. Некоторые бактерии проникают прямо в опухоль, где выделяют провоспалительные молекулы и перестраивают окружение клеток, окружающих рак. Предыдущие работы показали, что в этих воспалённых очагах уровни p53 — белка, часто называемого «стражем генома», потому что он помогает повреждённым клеткам самоуничтожаться — необычно низки. Поскольку p53 критически важен для ответа раковых клеток на химиотерапию, авторы задали вопрос, не саботируют ли кишечные бактерии этот барьер незаметно.
Скрытая поддерживающая сеть вокруг опухолевых клеток
Команда сосредоточилась на липополисахариде (LPS) — сильной провоспалительной молекуле на поверхности обычных кишечных микробов, таких как Klebsiella pneumoniae и другие энтеробактерии, которые часто увеличены при колоректальном раке. Удивительно, но при добавлении LPS напрямую к клеткам колоректального рака почти ничего не происходило: клетки не становились более устойчивыми к препаратам, а уровни p53 оставались прежними. Совсем иная картина возникла, когда сначала подвергали воздействию LPS иммунные клетки — макрофаги — или клетки соединительной ткани — фибробласты, а затем переносили жидкость, в которой эти клетки росли, на раковые клетки. В таких условиях химиотерапия убивала значительно меньше опухолевых клеток, и уровень белка p53 не накапливался так, как должен был после лечения.
Сообщения в крошечных пузырьках
Чтобы понять, что отправляют макрофаги, исследователи использовали продвинутый протеомный анализ, чтобы проследить тысячи изменений внутри раковых клеток, обработанных и химиотерапией, и секретом LPS-активированных макрофагов. Они выявили чёткий паттерн: сигналы, связанные с воспалением и активацией иммунитета, возросли, тогда как многие пути, контролируемые p53 и участвующие в контроле деления клеток и запрограммированного самоуничтожения, снизились. Дальнейшие эксперименты показали, что это подавление не опирается на классические провоспалительные гормоны, такие как интерлейкин-6. Вместо этого ключевыми посланцами оказались крошечные мембранные пузырьки — внеклеточные везикулы, выделяемые активированными макрофагами. Когда эти везикулы выделяли и добавляли к раковым клеткам, белок p53 становился нестабильным и быстрее разрушался клеточными механизмами утилизации, защищая клетки от гибели, индуцируемой p53.
Селективное «отключение» стража клетки
Авторы обнаружили, что этот бактериально-стромальный сигнал не просто выключает p53 везде. Наоборот, он выборочно подавляет одну группу генов, контролируемых p53, оставляя другие — особенно связанные с воспалением — без изменений или даже усиливая их. При анализе образцов опухолей пациентов с колоректальным раком они обнаружили соответствующий паттерн: в опухолях с высокой активностью воспалительных сигнатур этот кластер генов, отражающий «активность p53», был низким, особенно в опухолях с интактным геномом TP53. Важно, что пациенты, чьи опухоли демонстрировали высокую экспрессию этого p53-зависимого кластера, как правило, лучше отвечали на химиотерапию по сравнению с теми, у кого экспрессия была низкой, что указывает на то, что негенетическое подавление p53 воспалённым микроокружением может ухудшать клические исходы.
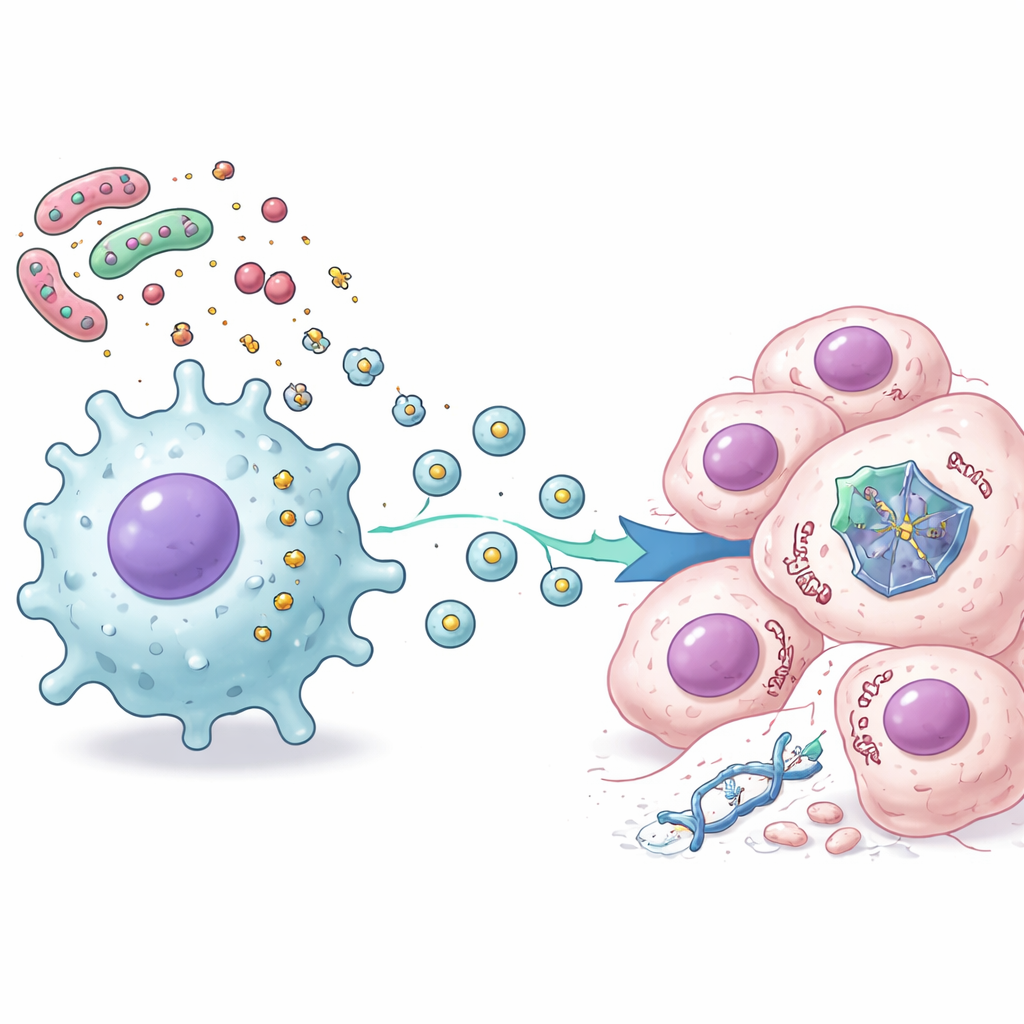
Что это значит для пациентов и терапии
В целом работа раскрывает цепочку событий, связывающую кишечные бактерии с резистентностью к химиотерапии: бактериальный LPS активирует соседние стромальные и иммунные клетки, эти клетки выделяют внеклеточные везикулы, а везикулы попадают в раковые клетки, дестабилизируют белок p53 и смягчают его решения о жизни и смерти после лечения. Даже при нормальном гене p53 внешнее давление может эффективно заглушать его защитную роль. Для пациентов это означает, что состояние микробиоты кишечника и местное воспаление могут помогать объяснять, почему некоторые колоректальные опухоли сопротивляются стандартным препаратам. В будущем стратегии, которые изменяют состав кишечных бактерий, уменьшают вредное воспаление или блокируют образование либо действие этих везикул, могут помочь восстановить опухолевый супрессорный потенциал p53 и повысить эффективность существующих химиотерапий.
Цитирование: Fragkoulis, K., Łasut-Szyszka, B., Végvári, Á. et al. Klebsiella pneumoniae LPS drives stromal-mediated repression of p53 and colorectal cancer chemoresistance. Cell Death Dis 17, 395 (2026). https://doi.org/10.1038/s41419-026-08756-4
Ключевые слова: колоректальный рак, микробиота кишечника, устойчивость к химиотерапии, опухолевый супрессор p53, опухолевое микроокружение