Clear Sky Science · tr
Klebsiella pneumoniae LPS, stromal kaynaklı p53 baskılanmasını ve kolorektal kanser kemoterapi direncini tetikliyor
Bağırsak Bakterilerinizin Kanser Tedavisi İçin Neden Önemli Olduğu
Kolorektal kanser genellikle güçlü kemoterapi ilaçlarıyla tedavi edilir, ancak birçok tümör bu saldırılardan kurtulmayı öğrenir. Bu çalışma beklenmedik bir suç ortağını araştırıyor: belirli bağırsak bakterileri. Araştırmacılar, bu mikroplardan gelen moleküllerin tümör içindeki vücudumuzun ana kanserle savaş mekanizmalarından birini sessizce zayıflatabileceğini gösteriyor; bu da standart tedavileri daha az etkili kılabiliyor—üstelik kanser hücreleri bakteriler tarafından doğrudan etkilenmese bile.
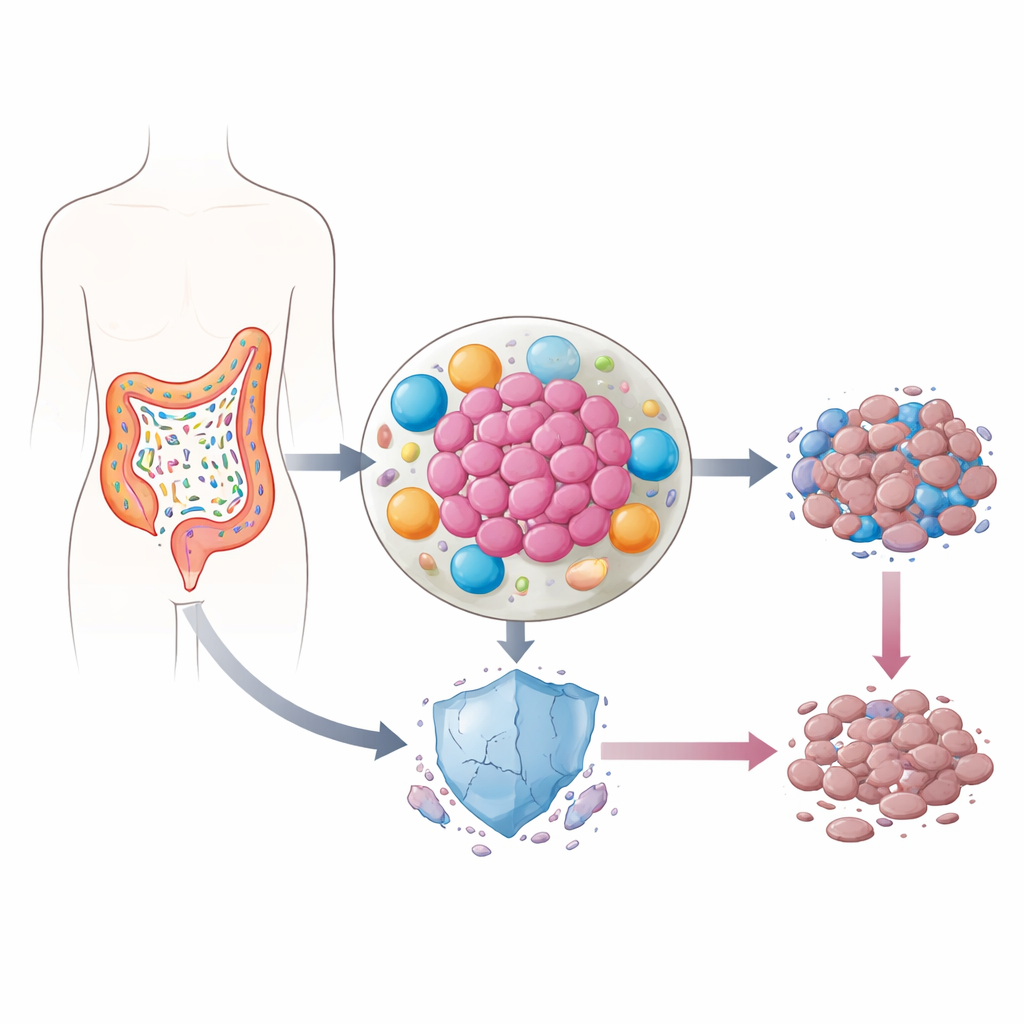
Tümörlerin İçinde Yaşayan Mikroplar
Bağırsaklarımız trilyonlarca bakteri barındırır; bunların çoğu zararsız veya yararlı bile olabilir. Ancak kolorektal kanserde türlerin dengesi sık sık değişir. Bazı bakteriler tümörün kendisine yerleşir, burada iltihaplanma tetikleyen moleküller salar ve kanseri çevreleyen hücrelerin ortamını yeniden şekillendirir. Önceki çalışmalar bu iltihaplı bölgelerde p53 düzeylerinin—hasarlı hücrelerin kendi kendini imha etmesine yardımcı olduğu için sıklıkla “genomun bekçisi” olarak adlandırılan bir protein—alışılmadık biçimde düşük olduğunu öne sürmüştü. p53, kanser hücrelerinin kemoterapiye yanıtında kritik olduğundan, yazarlar bağırsak bakterilerinin bu koruyucu mekanizmayı sessizce sabote edip etmediğini araştırdılar.
Tümör Hücrelerinin Etrafındaki Gizli Bir Destek Ağı
Ekip, Klebsiella pneumoniae ve kolorektal kanserde sıklıkla artan diğer Enterobakteriler gibi yaygın bağırsak mikroplarının yüzeyinde bulunan güçlü bir iltihap yapıcı molekül olan lipopolisakkarid (LPS) üzerinde yoğunlaştı. İlginç şekilde, LPS’yi doğrudan kolorektal kanser hücrelerine eklediklerinde pek bir şey olmadı: hücreler daha dirençli hale gelmedi ve p53 seviyeleri aynı kaldı. Durum tamamen değiştiğinde, önce makrofaj adı verilen bağışıklık hücrelerini veya fibroblast olarak bilinen bağ doku hücrelerini LPS’ye maruz bıraktılar, ardından bu hücrelerin yetiştirildiği sıvıyı kanser hücrelerine aktardılar. Bu koşullar altında kemoterapi çok daha az tümör hücresini öldürdü ve p53 proteini tedavi sonrası normalde olacağı gibi birikmedi.
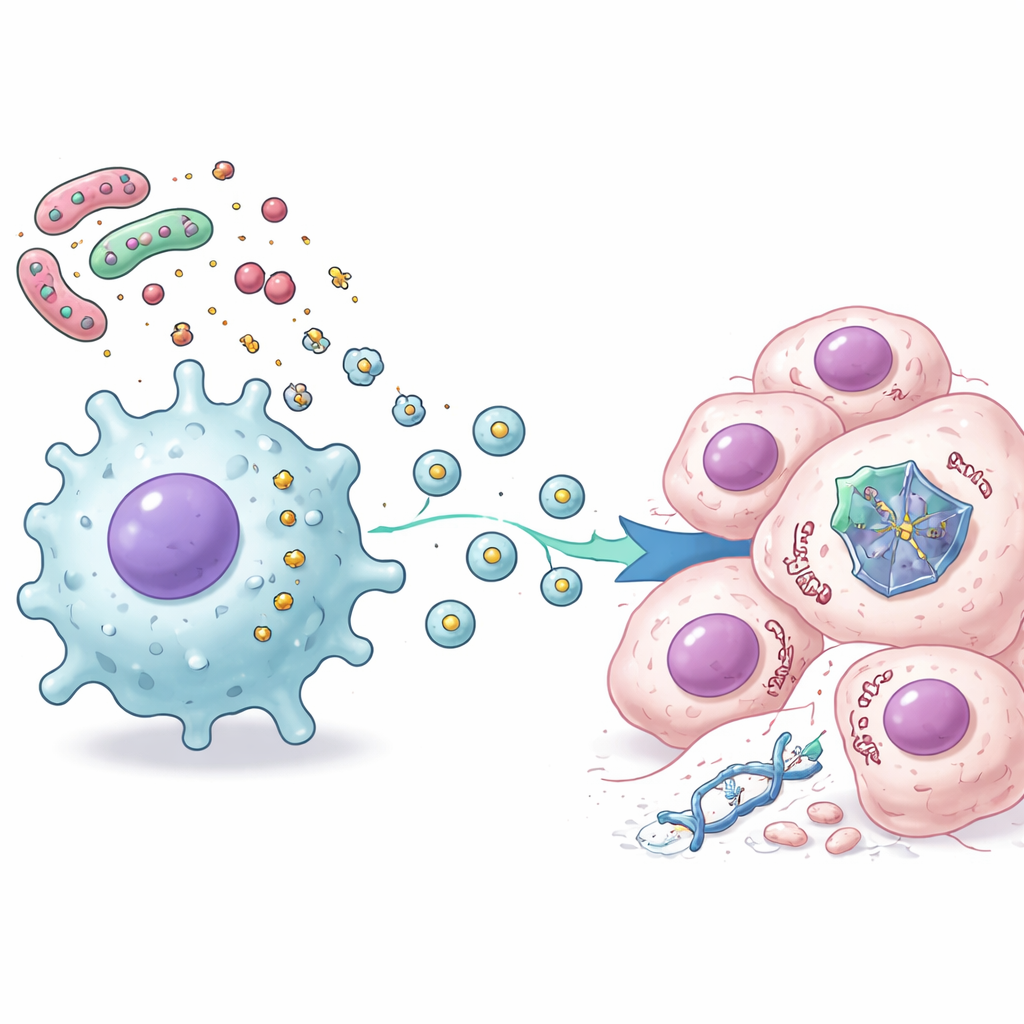
Küçük Keseciklere Paketlenmiş Mesajlar
Makrofajların ne gönderdiğini anlamak için araştırmacılar, kemoterapi ile birlikte LPS ile uyarılmış makrofaj salgılarıyla muamele edilen kanser hücreleri içinde binlerce değişikliği haritalamak üzere gelişmiş protein analizleri kullandılar. Net bir desen gördüler: iltihap ve bağışıklık aktivasyonu ile ilgili sinyaller arttı, oysa hücre bölünmesi ve kontrollü hücre ölümüyle ilgili birçok p53 kontrollü yol azaldı. Daha ileri deneyler, bu baskılanmanın interlökin-6 gibi klasik iltihap hormonlarından kaynaklanmadığını gösterdi. Bunun yerine kilit haberciler, uyarılmış makrofajlar tarafından salınan ekstraselüler vezikül olarak bilinen küçük zar kabarcıklarıydı. Bu veziküller izole edilip kanser hücrelerine eklendiğinde p53 proteini kararsızlaştı ve hücrenin kendi geri dönüşüm mekanizmasıyla daha hızlı yok edildi; böylece hücreler p53 kaynaklı ölümden korunmuş oldu.
Hücresel Bekçiyi Seçici Olarak Susturma
Yazarlar, bu bakteriyel–stromal sinyalin p53’ü her yerde basitçe kapatmadığını keşfettiler. Bunun yerine p53 kontrollü genlerin bir grubunu seçici olarak zayıflatıyor, diğerlerini—özellikle iltihapla bağlantılı olanları—ysa değiştirmiyor veya hatta artırıyordu. Kolorektal kanser hastalarından alınmış tümör örneklerine baktıklarında uyumlu bir desen buldular: iltihap ilişkili gen imzalarının yüksek olduğu tümörlerde bu “p53 aktivitesi” gen kümesi düşük olma eğilimindeydi, özellikle TP53 geni hâlâ sağlam olan kanserlerde. Önemli olarak, tümörleri bu p53-bağımlı küme ifadesini güçlü şekilde gösteren hastalar, düşük ifade gösterenlere göre kemoterapide daha iyi sonuçlar alma eğilimindeydi; bu da iltihaplı tümör ortamının p53’ü genetik olmayan yollardan susturmasının klinik sonuçları kötüleştirebileceğini düşündürüyor.
Hastalar ve Tedaviler İçin Anlamı
Birlikte ele alındığında bu çalışma, bağırsak bakterilerini kemoterapi direncine bağlayan bir olay zincirini ortaya koyuyor: bakteriyel LPS çevredeki stromal ve bağışıklık hücrelerini aktifleştiriyor, bu hücreler ekstraselüler veziküller salıyor ve bu veziküller kanser hücrelerine girerek p53 proteinini kararsızlaştırıp tedavi sonrası yaşam ve ölüm kararlarını köreltiyor. p53 geni normal olsa bile bu dış baskı koruyucu rolünü etkili bir şekilde susturabiliyor. Hastalar için bu, bağırsak mikrobiyomu durumu ve yerel iltihabın bazı kolorektal tümörlerin standart ilaçlara neden direnç gösterdiğini açıklamaya yardımcı olabileceğini öne sürüyor. Gelecekte, bağırsak bakterilerini yeniden şekillendiren, zararlı iltihabı yatıştıran veya bu veziküllerin üretimini ya da etkisini engelleyen stratejiler p53’ün tümör baskılayıcı gücünü geri kazandırmaya ve mevcut kemoterapilerin etkinliğini artırmaya yardımcı olabilir.
Atıf: Fragkoulis, K., Łasut-Szyszka, B., Végvári, Á. et al. Klebsiella pneumoniae LPS drives stromal-mediated repression of p53 and colorectal cancer chemoresistance. Cell Death Dis 17, 395 (2026). https://doi.org/10.1038/s41419-026-08756-4
Anahtar kelimeler: kolorektal kanser, bağırsak mikrobiyomu, kemoterapi direnci, p53 tümör baskılayıcısı, tümör mikroçevresi