Clear Sky Science · zh
lincRNA‑EPS 在炎性微环境中通过防止过度铁代谢缓解破骨细胞形成
这对疼痛牙龈和脆弱牙齿为何重要
许多成年人因牙周炎而出现牙龈出血和牙齿松动——这种慢性感染在不知不觉中破坏固定牙齿的骨质。本研究深入这一过程,发现一种鲜为人知的 RNA 分子如何维持破骨细胞与铁利用的平衡,并指出在牙龈病期间保护颌骨的新思路。
炎性牙龈中正在工作的“吞骨者”
在牙周炎中,牙周细菌刺激牙龈产生强烈免疫反应。炎症激活了一类特殊的“吞骨”细胞——破骨细胞,它们在颌骨上挖出空洞,最终可导致牙齿脱落。作者使用一种通过将细菌组分系在牙齿周围建立的鼠类牙龈病模型,并通过三维扫描证实炎症导致明显的骨丧失。他们聚焦于名为 lincRNA‑EPS 的分子,这是一种已知能在其他组织抑制炎性信号的非编码 RNA,探查其是否也能在这种恶劣环境中制约破骨细胞的活性。
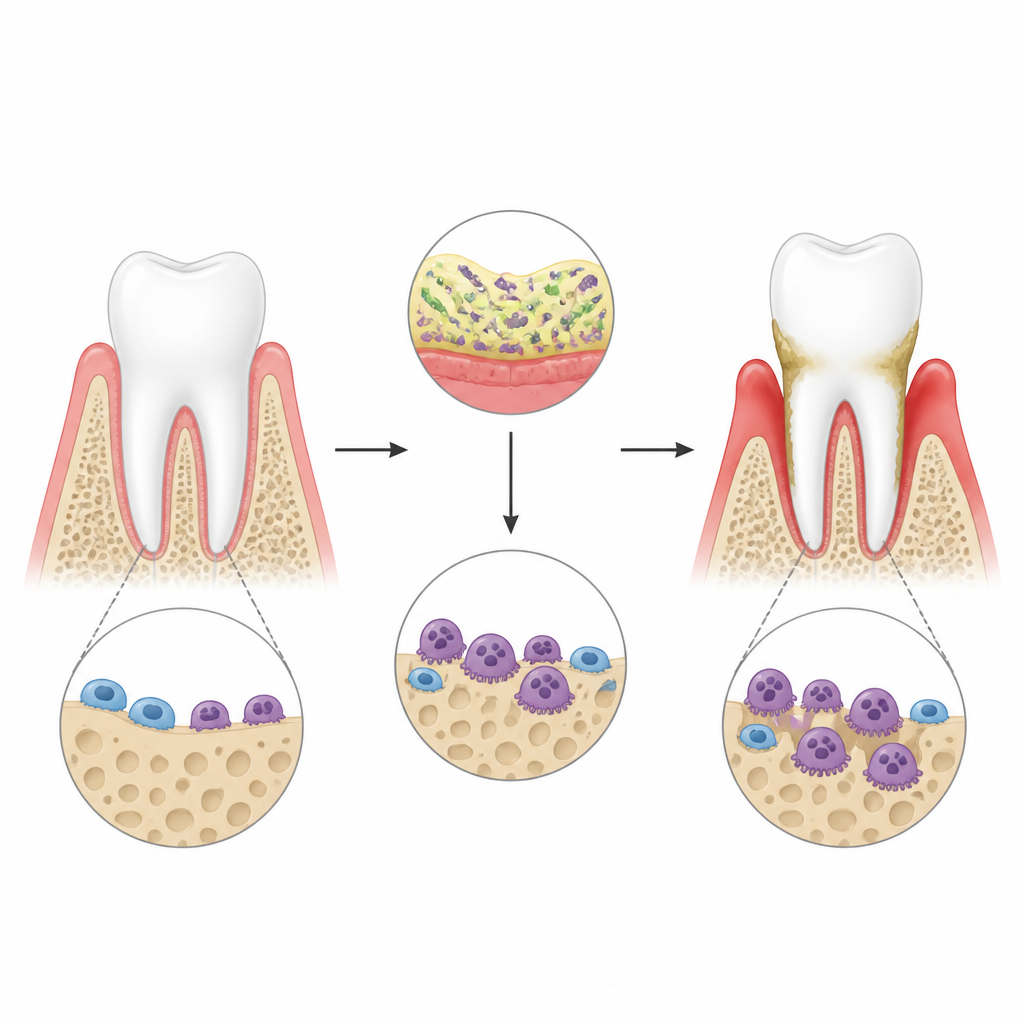
一种将骨丧失控制住的保护性 RNA
当研究者在小鼠体内敲除 lincRNA‑EPS 后,牙龈感染后的牙周骨丧失明显加重。颌骨表面出现更多且更大的破骨细胞,在体外骨片上的侵蚀坑更深更宽。在细胞培养中,来自正常和敲除动物的骨髓细胞先被诱导向破骨细胞分化,随后暴露于模拟细菌毒素的炎性刺激下。缺失 lincRNA‑EPS 的细胞更容易分化为侵袭性的破骨细胞,并以更高水平开启骨吸收相关基因和蛋白。这些发现表明,在炎性应激下,lincRNA‑EPS 通常起到对破骨细胞生长和功能的制动作用。
铁处理是隐藏的联系
为弄清这种 RNA 如何发挥作用,团队比较了来自正常与敲除小鼠的前体细胞和成熟破骨细胞的基因表达与蛋白谱。他们发现不仅破骨细胞程序更强,还在控制铁利用、储存和转运的通路中出现显著变化。一种分泌蛋白脂泌素‑2(Lcn2),可在细胞间运送铁,在 lincRNA‑EPS 缺失时尤其在炎性刺激后显著上调。进一步实验显示,在缺失 lincRNA‑EPS 的组织和培养细胞中,Lcn2 水平持续偏高,铁处理相关蛋白持续活化,破骨细胞内的可动用铁保持升高,所有这些都是过度活跃的铁代谢为高能耗的“吞骨者”提供燃料的迹象。
调节一种铁运输子以平息骨损伤
研究者随后直接操控 Lcn2 以观察其对系统的影响。在正常的前体细胞中降低 Lcn2 可抑制铁转运机制并改变破骨细胞形态,产生体积更小、核较少的细胞,尽管细胞数量可能增加。补充额外 Lcn2 则相反,帮助细胞融合成更大、更有力的骨吸收单元。在患有牙龈疾病的小鼠中,降低牙周组织的 Lcn2 可减少骨丧失与破骨细胞活性,但这种效应仅在 lincRNA‑EPS 存在时明显。当 lincRNA‑EPS 缺失时,改变 Lcn2 水平或外源补充 Lcn2 对铁水平和破骨细胞行为的影响较弱且迟缓,表明该 RNA 对炎症期间铁代谢的快速且稳定调节是必需的。
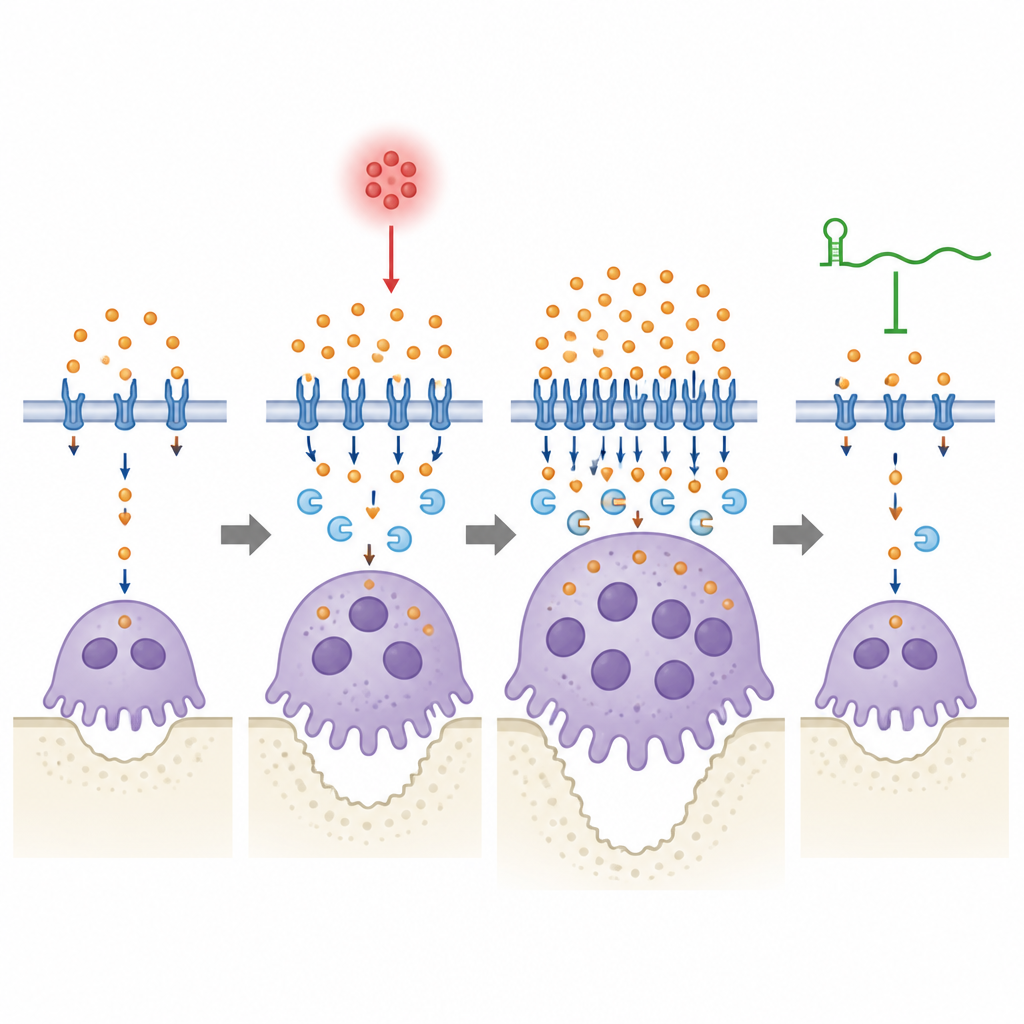
铁与骨之间的微妙平衡
从非专业角度来看,这项工作表明调控性 RNA lincRNA‑EPS 通过防止破骨细胞大量摄取并长期滞留铁,从而帮助颌骨在牙龈感染中幸存。在发炎的口腔环境中,Lcn2 上升并推动更多铁进入破骨细胞,促进其生长并侵蚀骨质;lincRNA‑EPS 帮助这些细胞感知并纠正这种激增,使铁利用回到安全水平。当该 RNA 缺失时,这一安全阀失灵,铁处理持续过度,骨丧失加剧。尽管该研究为临床前研究,但它强调了铁调控及 lincRNA‑EPS–Lcn2 轴作为未来治疗靶点的潜力,目标是通过温和放慢骨吸收而非完全关闭来保护牙齿。
引用: Wang, J., Wang, Y., Zhang, Z. et al. LincRNA-EPS alleviates osteoclastogenesis under inflammatory microenvironment through preventing excessive iron metabolism. Cell Death Dis 17, 444 (2026). https://doi.org/10.1038/s41419-026-08716-y
关键词: 牙周炎, 破骨细胞, 铁代谢, 脂泌素‑2, 长链非编码 RNA