Clear Sky Science · fr
Le lincRNA‑EPS atténue l’ostéoclastogenèse en microenvironnement inflammatoire en empêchant un métabolisme du fer excessif
Pourquoi cela importe pour les gencives douloureuses et les dents fragiles
Beaucoup d’adultes vivent avec des gencives qui saignent et des dents mobiles causées par la parodontite, une infection chronique qui ronge silencieusement l’os qui maintient les dents. Cette étude explore ce processus en profondeur et révèle comment une molécule d’ARN peu connue aide à maintenir l’équilibre entre les cellules qui résorbent l’os et l’utilisation du fer, ouvrant des pistes pour mieux protéger l’os mandibulaire lors de la maladie des gencives.
Les mangeurs d’os à l’œuvre dans les gencives enflammées
Dans la parodontite, les bactéries autour des dents déclenchent une forte réponse immunitaire dans les gencives. Cette inflammation réveille des cellules spécialisées de résorption osseuse, les ostéoclastes, qui creusent des cavités dans l’os de la mâchoire et peuvent finalement entraîner la perte des dents. Les auteurs ont utilisé un modèle murin de maladie gingivale obtenu en fixant des composants bactériens autour des dents et ont confirmé par tomographies 3D que l’inflammation provoquait une perte osseuse nette. Ils se sont concentrés sur une molécule nommée lincRNA‑EPS, un ARN non codant déjà connu pour atténuer les signaux inflammatoires dans d’autres tissus, afin de vérifier si elle limite aussi l’activité des ostéoclastes dans cet environnement hostile.
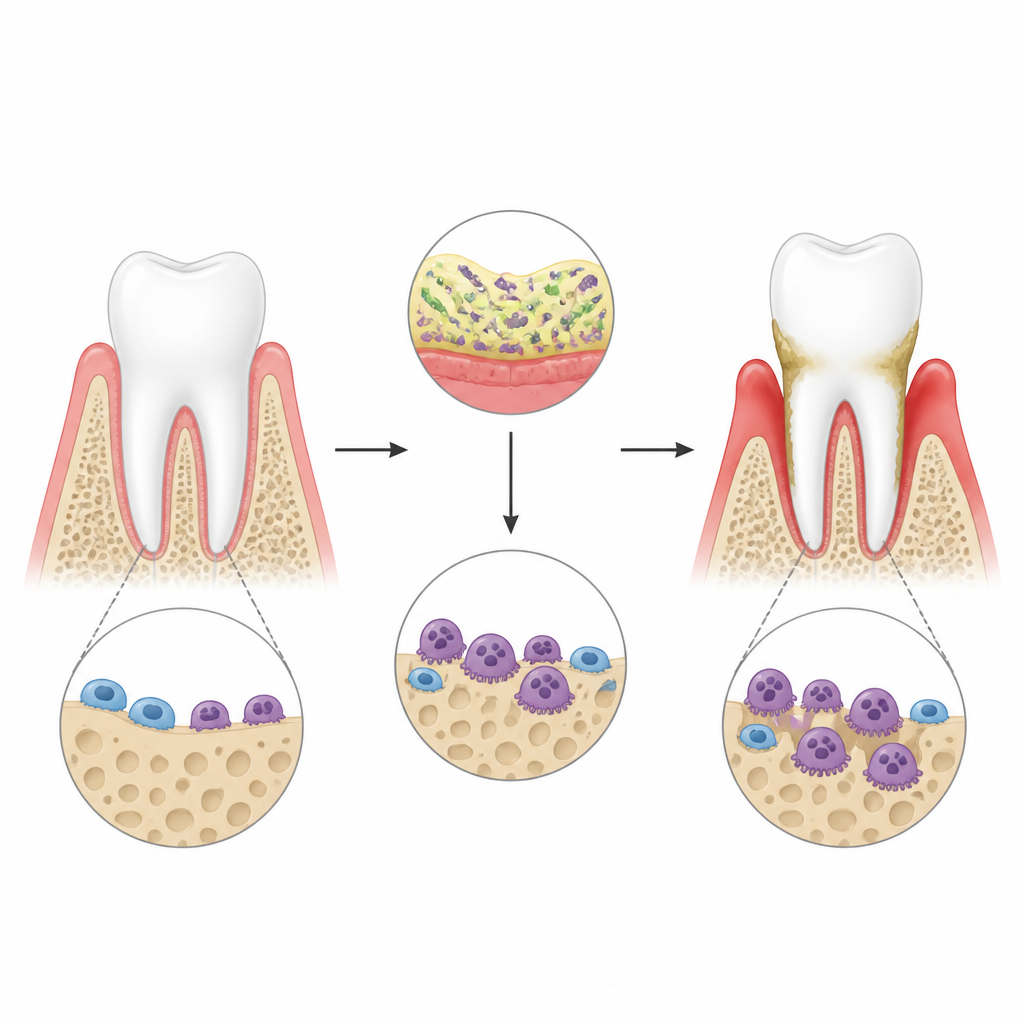
Un ARN protecteur qui freine la perte osseuse
Quand les chercheurs ont supprimé le lincRNA‑EPS chez la souris, la perte osseuse autour des dents s’est aggravée de façon notable après l’infection gingivale. La surface de la mâchoire présentait plus d’ostéoclastes, de plus grande taille, et les puits qu’ils ont creusés dans les tranches d’os en laboratoire étaient plus profonds et plus larges. En culture cellulaire, des cellules de moelle osseuse provenant d’animaux normaux et de souris knock‑out ont d’abord été orientées vers une différenciation ostéoclastique, puis exposées à un déclencheur inflammatoire mimant les toxines bactériennes. Les cellules dépourvues de lincRNA‑EPS se sont transformées plus facilement en ostéoclastes agressifs et ont activé à des niveaux plus élevés les gènes et protéines responsables de la résorption osseuse. Ces résultats suggèrent que le lincRNA‑EPS agit normalement comme un frein à la croissance et à la fonction des ostéoclastes en situation de stress inflammatoire.
La gestion du fer, lien caché
Pour comprendre comment cet ARN exerce son effet, l’équipe a comparé l’activité génique et les profils protéiques dans des précurseurs cellulaires et des ostéoclastes matures issus de souris normales et knock‑out. Ils ont trouvé non seulement des programmes ostéoclastiques renforcés, mais aussi des modifications marquantes des voies contrôlant l’utilisation, le stockage et le transport du fer. Une protéine sécrétée, la lipocaline‑2 (Lcn2), capable de transporter le fer vers l’intérieur et l’extérieur des cellules, s’est distinguée par une augmentation marquée en l’absence de lincRNA‑EPS, surtout après stimulation inflammatoire. Des tests complémentaires ont montré que dans les tissus et cellules en culture privés de lincRNA‑EPS, les niveaux de Lcn2 restaient élevés, les protéines de gestion du fer restaient activées plus longtemps et le fer mobile à l’intérieur des ostéoclastes demeurait élevé — autant de signes d’un métabolisme du fer hyperactif qui alimente ces cellules consommatrices d’énergie.
Régler une navette du fer pour calmer les dégâts osseux
Les scientifiques ont ensuite manipulé directement Lcn2 pour évaluer son influence. Réduire Lcn2 dans des précurseurs normaux a atténué la machinerie de transport du fer et modifié la morphologie des ostéoclastes, donnant des cellules plus petites avec moins de noyaux, même si leur nombre pouvait augmenter. Ajouter de la Lcn2 en excès provoquait l’effet inverse, favorisant la fusion des cellules en unités de résorption plus grandes et plus puissantes. Chez les souris atteintes de maladie gingivale, diminuer Lcn2 dans les tissus péri‑dentaires réduisait la perte osseuse et l’activité ostéoclastique, mais seulement en présence de lincRNA‑EPS. Lorsque le lincRNA‑EPS manquait, modifier les niveaux de Lcn2 ou ajouter de la Lcn2 avait des effets plus faibles et plus lents sur les niveaux de fer et le comportement des ostéoclastes, suggérant que cet ARN est nécessaire pour un ajustement rapide et stable du métabolisme du fer pendant l’inflammation.
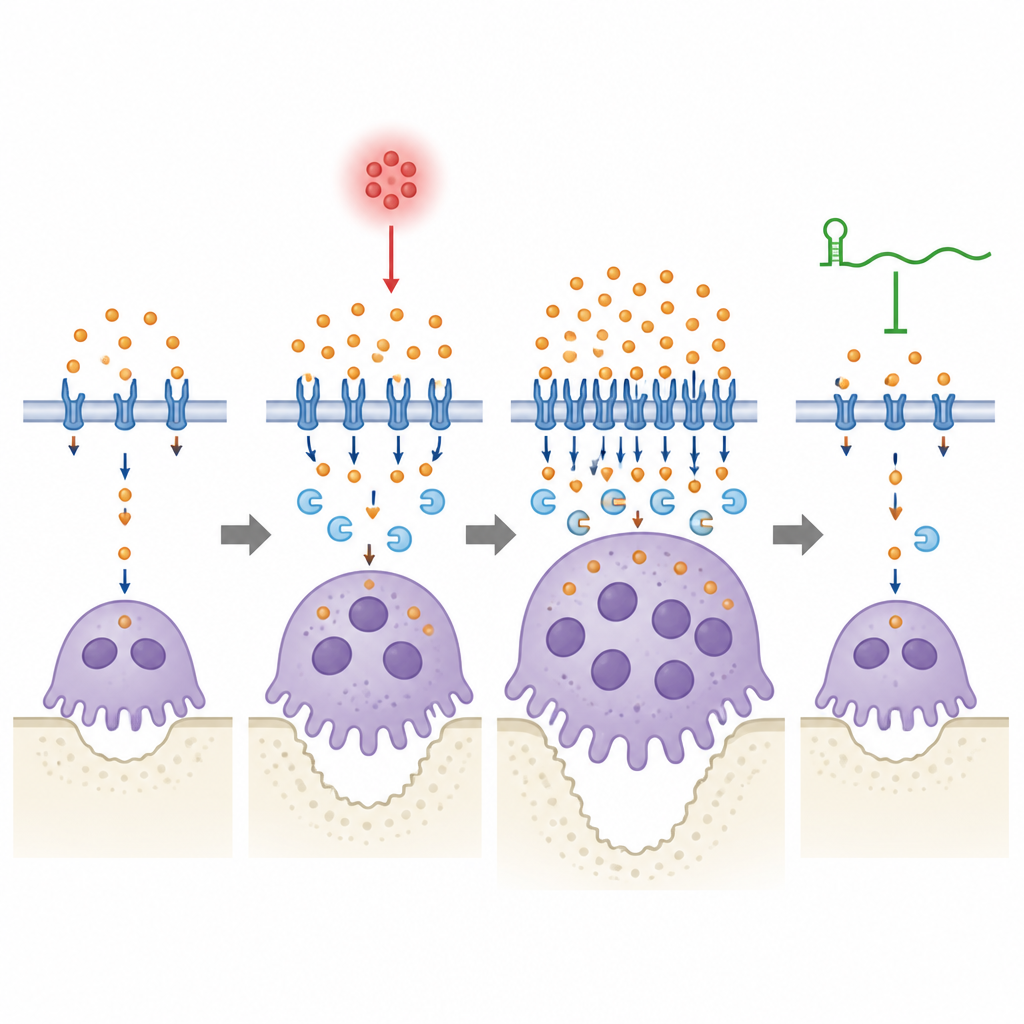
Un équilibre fin entre fer et os
Pour un lecteur non spécialiste, ce travail montre qu’un ARN régulateur, le lincRNA‑EPS, aide l’os mandibulaire à survivre à l’infection gingivale en empêchant les ostéoclastes de se gaver de fer et de rester hyperactifs trop longtemps. Dans une bouche enflammée, la Lcn2 augmente et pousse davantage de fer dans les ostéoclastes, favorisant leur croissance et la dégradation osseuse ; le lincRNA‑EPS aide ces cellules à détecter et corriger cette poussée pour ramener l’utilisation du fer à un niveau sûr. En l’absence de cet ARN, cette soupape de sécurité fait défaut, la gestion du fer reste excessive et la perte osseuse s’aggrave. Bien que l’étude soit préclinique, elle met en lumière la régulation du fer et le couple lincRNA‑EPS–Lcn2 comme cibles potentielles pour des thérapies futures visant à protéger les dents en ralentissant doucement la résorption osseuse plutôt qu’en l’éteignant complètement.
Citation: Wang, J., Wang, Y., Zhang, Z. et al. LincRNA-EPS alleviates osteoclastogenesis under inflammatory microenvironment through preventing excessive iron metabolism. Cell Death Dis 17, 444 (2026). https://doi.org/10.1038/s41419-026-08716-y
Mots-clés: parodontite, ostéoclastes, métabolisme du fer, lipocaline‑2, ARN long non codant