Clear Sky Science · pt
LincRNA-EPS alivia a osteoclastogênese em microambiente inflamatório prevenindo metabolismo excessivo do ferro
Por que isso importa para gengivas doloridas e dentes frágeis
Muitos adultos convivem com gengivas que sangram e dentes soltos causados pela periodontite, uma infecção crônica que silenciosamente corrói o osso que sustenta os dentes. Este estudo investiga esse processo e revela como uma molécula de RNA pouco conhecida ajuda a manter em equilíbrio as células que comem osso e o uso de ferro, apontando novas maneiras de proteger o osso da mandíbula durante a doença gengival.
Ostéoclastos em ação em gengivas inflamadas
Na periodontite, bactérias ao redor dos dentes desencadeiam uma forte resposta imune nas gengivas. Essa inflamação ativa células especiais que degradam o osso, chamadas osteoclastos, que escavam cavidades na mandíbula e podem eventualmente levar à perda dentária. Os autores usaram um modelo murino de doença gengival criado com componentes bacterianos amarrados aos dentes e confirmaram por meio de exames 3D que a inflamação levou a perda óssea evidente. Eles focaram em uma molécula chamada lincRNA-EPS, um RNA não codificante já conhecido por acalmar sinais inflamatórios em outros tecidos, para investigar se ela também reprime a atividade dos osteoclastos nesse ambiente adverso.
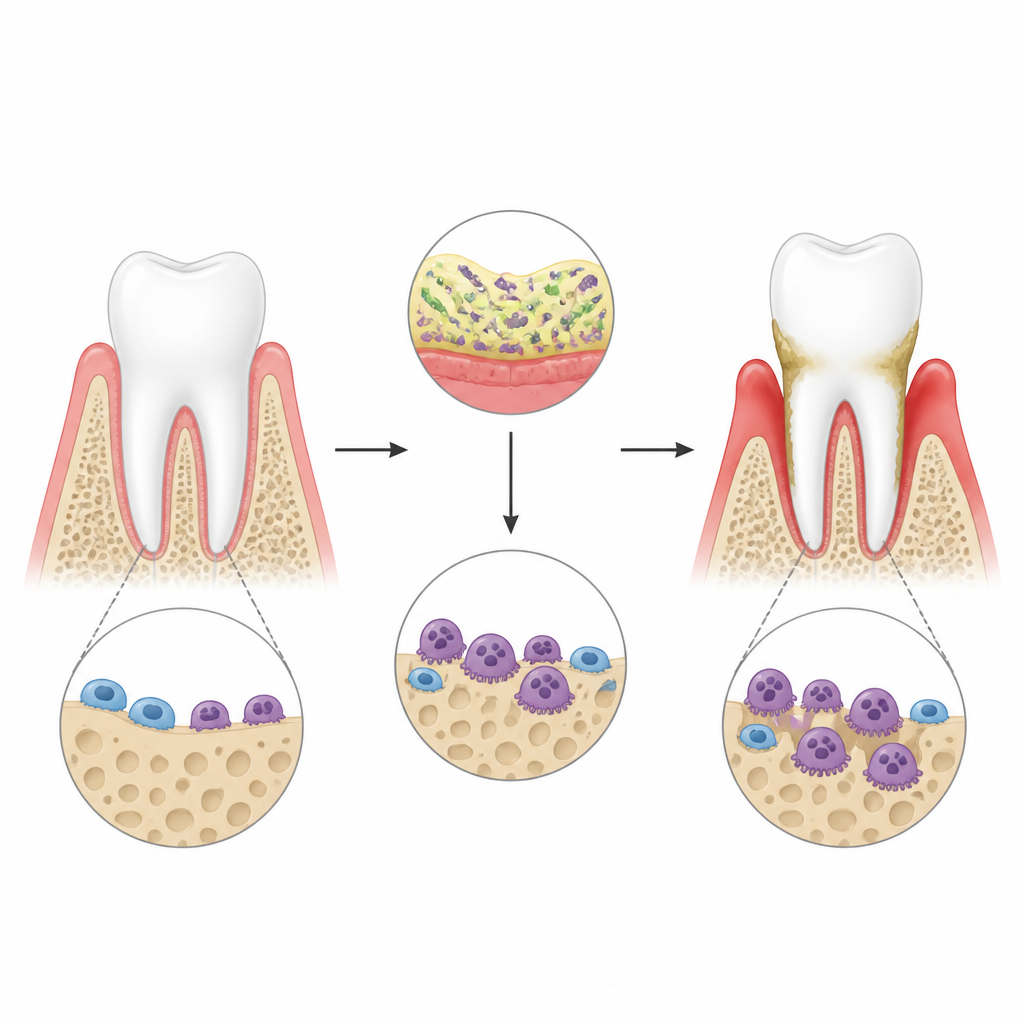
Um RNA protetor que mantém a perda óssea sob controle
Quando os pesquisadores removeram lincRNA-EPS em camundongos, a perda óssea ao redor dos dentes piorou visivelmente após a infecção gengival. A superfície da mandíbula mostrou mais osteoclastos maiores, e as lacunas que eles escavaram em lâminas de osso no laboratório foram mais profundas e largas. Em cultura celular, células-tronco da medula óssea de animais normais e knockout foram primeiro induzidas a se tornar osteoclastos e depois expostas a um estímulo inflamatório que imita toxinas bacterianas. Células sem lincRNA-EPS se transformaram em osteoclastos agressivos com mais facilidade e ativaram genes e proteínas reabsorvedoras de osso em níveis mais altos. Esses achados sugerem que lincRNA-EPS atua normalmente como um freio ao crescimento e à função dos osteoclastos sob estresse inflamatório.
O manejo do ferro como elo oculto
Para entender como esse RNA exerce seu efeito, a equipe comparou a atividade gênica e os perfis proteicos em células precursoras e osteoclastos maduros de camundongos normais e knockout. Eles encontraram não apenas programas osteoclásticos mais fortes, mas também alterações marcantes em vias que controlam o uso, armazenamento e transporte do ferro. Uma proteína secretada, lipocalina-2 (Lcn2), que pode transportar ferro para dentro e fora das células, destacou-se por estar fortemente aumentada quando lincRNA-EPS estava ausente, especialmente após estimulação inflamatória. Testes adicionais mostraram que em tecidos e células cultivadas sem lincRNA-EPS, os níveis de Lcn2 permaneciam altos, as proteínas de manejo do ferro continuavam ativadas por mais tempo e o ferro móvel dentro dos osteoclastos ficava elevado — todos sinais de uma economia de ferro hiperativa que alimenta esses devoradores de osso energeticamente exigentes.
Regulando um shuttle de ferro para acalmar o dano ósseo
Os cientistas então manipularam diretamente a Lcn2 para ver como ela influencia esse sistema. Reduzir Lcn2 em células precursoras normais atenuou o maquinário de transporte de ferro e alterou a morfologia dos osteoclastos, produzindo células menores com menos núcleos, embora seus números pudessem aumentar. Adicionar Lcn2 extra teve o efeito oposto, ajudando as células a fundirem-se em unidades maiores e mais potentes de reabsorção óssea. Em camundongos com doença gengival, abaixar os níveis de Lcn2 nos tecidos ao redor dos dentes reduziu a perda óssea e a atividade osteoclástica, mas apenas quando lincRNA-EPS estava presente. Quando lincRNA-EPS estava ausente, alterar os níveis de Lcn2 ou acrescentar Lcn2 extra teve efeitos mais fracos e mais lentos sobre os níveis de ferro e o comportamento dos osteoclastos, sugerindo que esse RNA é necessário para um ajuste rápido e estável do metabolismo do ferro durante a inflamação.
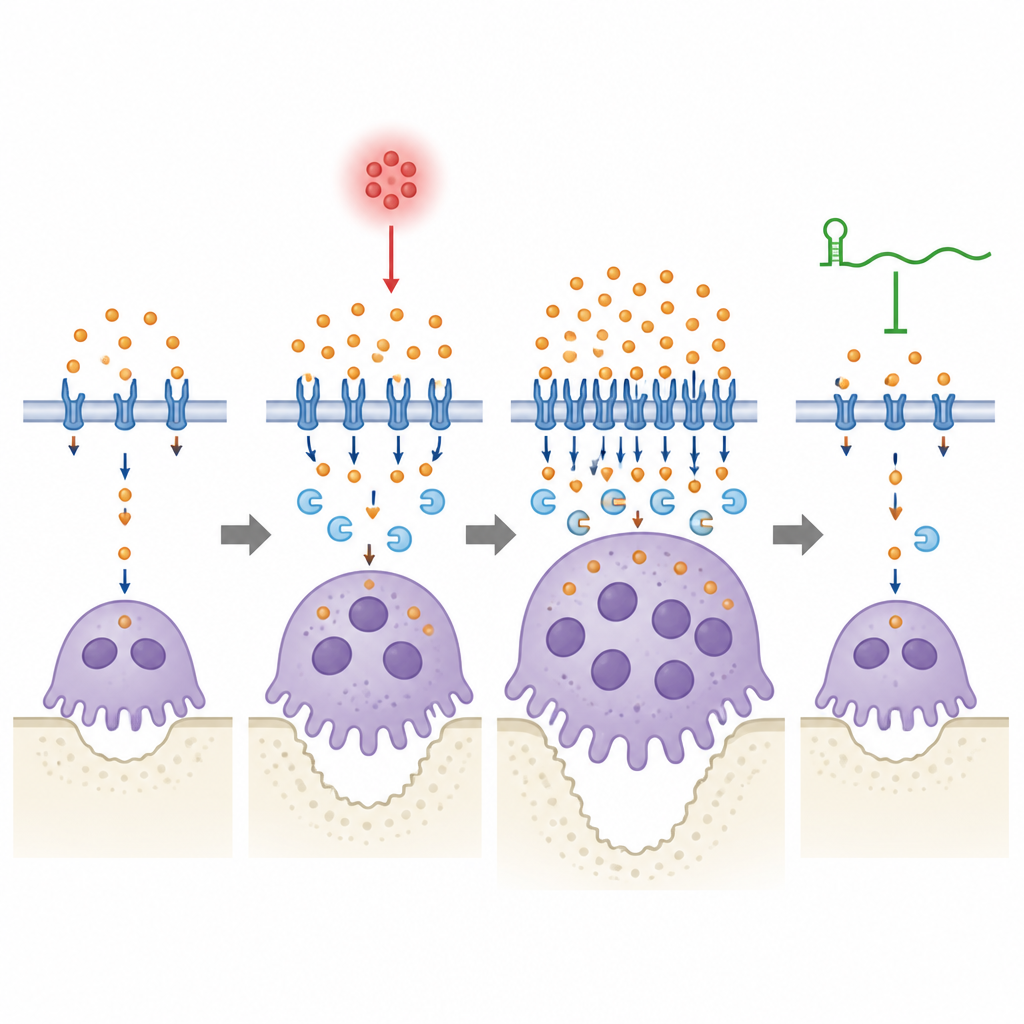
Um equilíbrio delicado entre ferro e osso
Em termos leigos, este trabalho mostra que um RNA regulatório, lincRNA-EPS, ajuda o osso da mandíbula a sobreviver à infecção gengival prevenindo que células que comem osso se banquetem de ferro e permaneçam hiperativas por tempo excessivo. Em uma boca inflamada, Lcn2 aumenta e empurra mais ferro para dentro dos osteoclastos, ajudando-os a crescer e corroer o osso; lincRNA-EPS ajuda essas células a detectar e corrigir esse pico para que o uso de ferro retorne a um nível seguro. Quando o RNA está ausente, essa válvula de segurança falha, o manejo do ferro permanece excessivo e a perda óssea piora. Embora o estudo seja pré-clínico, ele destaca a regulação do ferro e o par lincRNA-EPS–Lcn2 como alvos potenciais para futuras terapias que visem proteger os dentes desacelerando suavemente a reabsorção óssea em vez de bloqueá-la completamente.
Citação: Wang, J., Wang, Y., Zhang, Z. et al. LincRNA-EPS alleviates osteoclastogenesis under inflammatory microenvironment through preventing excessive iron metabolism. Cell Death Dis 17, 444 (2026). https://doi.org/10.1038/s41419-026-08716-y
Palavras-chave: periodontite, osteoclastos, metabolismo do ferro, lipocalina-2, RNA longo não codificante