Clear Sky Science · sv
LincRNA-EPS lindrar osteoklastogenes under inflammatorisk mikromiljö genom att förhindra överdriven järnmetabolism
Varför detta är viktigt för ömt tandkött och sköra tänder
Många vuxna lever med blödande tandkött och lösa tänder orsakade av parodontit, en kronisk infektion som tyst äter upp det ben som håller tänderna på plats. Denna studie undersöker det inre av den processen och upptäcker hur en relativt okänd RNA-molekyl hjälper till att hålla bennedbrytande celler och järnanvändning i balans, vilket pekar på nya sätt att skydda käkbenet vid tandköttssjukdom.
Bennedbrytare i arbete i inflammerat tandkött
Vid parodontit framkallar bakterier runt tänderna en kraftig immunrespons i tandköttet. Denna inflammation väcker särskilda bennedbrytande celler, så kallade osteoklaster, som gräver hål i käkbenet och så småningom kan leda till tandförlust. Författarna använde en musmodell för tandköttssjukdom där bakteriekomponenter fästs runt tänderna, och bekräftade med 3D-skanningar att inflammationen ledde till tydlig benförlust. De fokuserade på en molekyl kallad lincRNA-EPS, ett icke-kodande RNA som redan är känt för att dämpa inflammatoriska signaler i andra vävnader, för att se om den också hämmar osteoklastaktivitet i denna hårda miljö.
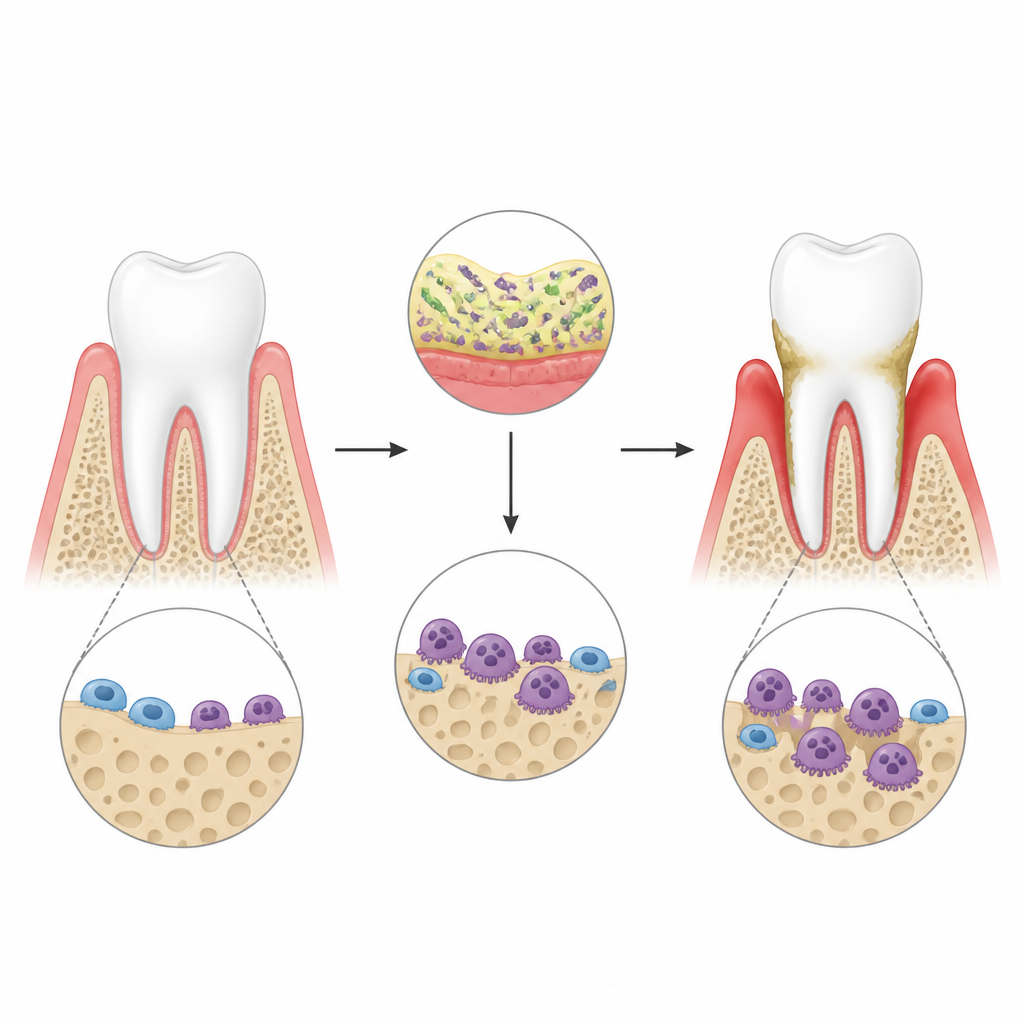
En skyddande RNA som håller benförlust i schack
När forskarna borttog lincRNA-EPS från möss blev benförlusten runt tänderna märkbart värre efter tandköttsinflammation. Käkbenets yta visade fler och större osteoklaster, och de gropar de utskär i benprov i labbet var djupare och bredare. I cellodling stimulerades benmärgsceller från normala och knockout-djur först mot att bli osteoklaster, och exponerades sedan för en inflammatorisk trigger som efterliknar bakterietoxiner. Celler utan lincRNA-EPS omvandlades lättare till aggressiva osteoklaster och slog på gener och proteiner för benresorption i högre grad. Dessa fynd tyder på att lincRNA-EPS normalt fungerar som en broms på osteoklasttillväxt och funktion under inflammatorisk stress.
Järnhantering som den dolda länken
För att förstå hur denna RNA utövar sin effekt jämförde teamet genaktivitet och proteinmönster i prekursorceller och mogna osteoklaster från normala och knockout-möss. De fann inte bara starkare osteoklastprogram, utan också markanta förändringar i vägar som styr järnanvändning, lagring och transport. Ett sekretoriskt protein, lipocalin-2 (Lcn2), som kan frakta järn in och ut ur celler, stack ut som starkt ökat när lincRNA-EPS saknades, särskilt efter inflammatorisk stimulering. Ytterligare tester visade att i vävnader och odlade celler utan lincRNA-EPS hölls Lcn2-nivåerna höga, järnhanteringsproteiner förblev aktiva längre och det rörliga järnet inne i osteoklaster förblev förhöjt — alla tecken på en överaktiv järnekonomi som matar de energikrävande bennedbitarna.
Finjustering av en järntransportör för att dämpa bent skada
Forskarna manipulerade sedan Lcn2 direkt för att se hur det påverkar systemet. Att minska Lcn2 i normala prekursorceller dämpade järntransportmaskineriet och ändrade osteoklasternas form, vilket gav mindre celler med färre kärnor, även om deras antal kunde öka. Att tillsätta extra Lcn2 hade motsatt effekt och hjälpte celler att förena sig till större, mer kraftfulla benresorberande enheter. I möss med tandköttssjukdom minskade sänkning av Lcn2 i vävnaderna runt tänderna benförlusten och osteoklastaktiviteten, men endast när lincRNA-EPS var närvarande. När lincRNA-EPS saknades hade förändringar i Lcn2-nivåer eller tillförsel av extra Lcn2 svagare och långsammare effekter på järnnivåer och osteoklastbeteende, vilket tyder på att detta RNA krävs för en snabb och stabil justering av järnmetabolism under inflammation.
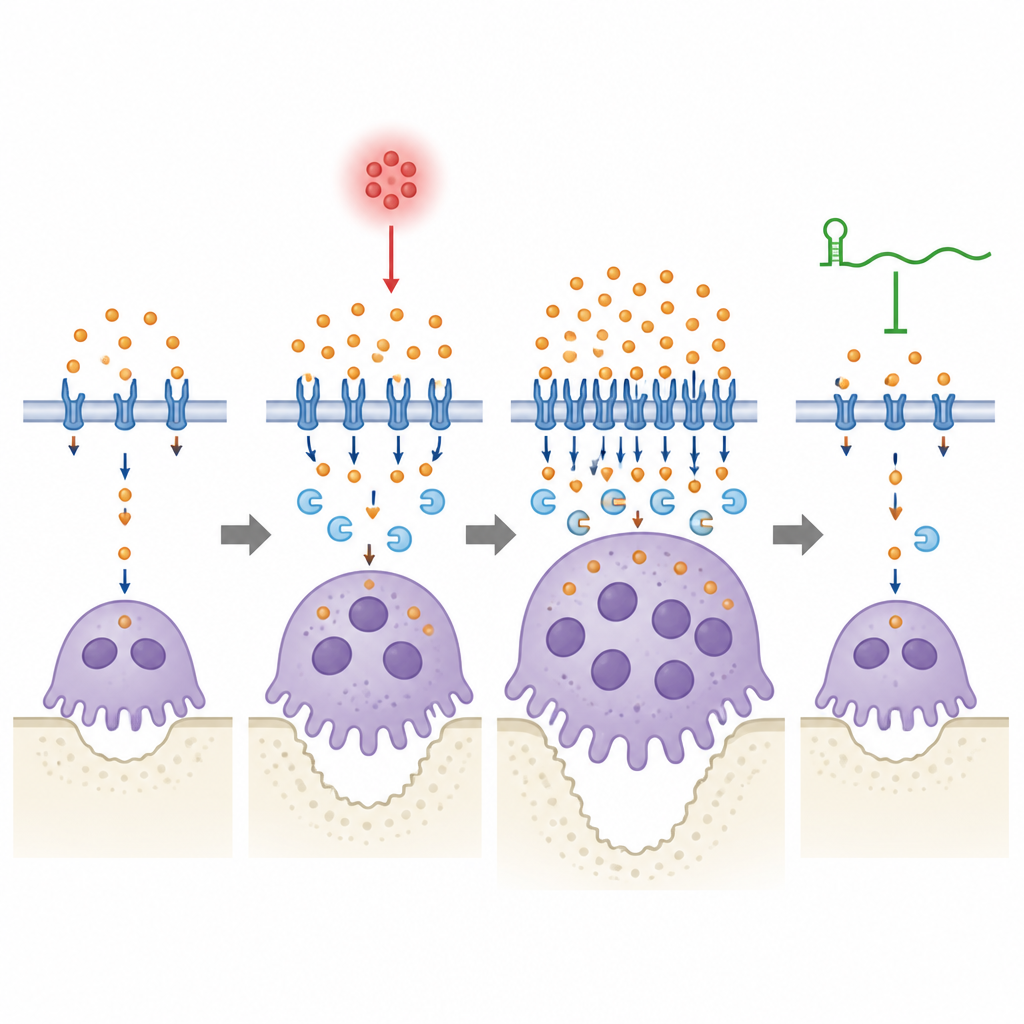
En finavvägd balans mellan järn och ben
Ur ett populärvetenskapligt perspektiv visar detta arbete att ett reglerande RNA, lincRNA-EPS, hjälper käkbenet att överleva tandköttsinflammation genom att förhindra att bennedbrytande celler överäter järn och förblir överaktiva för länge. I en inflammerad mun stiger Lcn2 och driver mer järn in i osteoklaster, vilket hjälper dem att växa och äta sig igenom ben; lincRNA-EPS hjälper dessa celler att känna av och rätta till den ökningen så att järnanvändningen återgår till en säker nivå. När RNA:t saknas misslyckas denna säkerhetsventil, järnhanteringen förblir överdriven och benförlusten förvärras. Även om studien är preklinisk lyfter den fram järnreglering och paret lincRNA-EPS–Lcn2 som potentiella mål för framtida terapier som syftar till att skydda tänder genom att varsamt bromsa benresorption i stället för att helt stänga ner den.
Citering: Wang, J., Wang, Y., Zhang, Z. et al. LincRNA-EPS alleviates osteoclastogenesis under inflammatory microenvironment through preventing excessive iron metabolism. Cell Death Dis 17, 444 (2026). https://doi.org/10.1038/s41419-026-08716-y
Nyckelord: parodontit, osteoklaster, järnmetabolism, lipocalin-2, lång icke-kodande RNA