Clear Sky Science · nl
LincRNA-EPS vermindert osteoclastogenese in een ontstekingsrijke omgeving door overmatige ijzerstofwisseling te voorkomen
Waarom dit belangrijk is voor pijnlijk tandvlees en kwetsbare tanden
Veel volwassenen hebben last van bloedend tandvlees en losse tanden door parodontitis, een chronische infectie die langzaam het bot dat tanden op hun plaats houdt wegvreet. Deze studie onderzoekt dat proces en ontdekt hoe een weinig bekend RNA-molecuul helpt om botetende cellen en ijzergebruik in balans te houden, en wijst daarmee op nieuwe manieren om het kaakbot te beschermen tijdens tandvleesziekte.
Boteters aan het werk in ontstoken tandvlees
Bij parodontitis veroorzaken bacteriën rondom de tanden een sterke immuunreactie in het tandvlees. Deze ontsteking activeert speciale botetende cellen, osteoclasten genoemd, die gaten in het kaakbot graven en uiteindelijk tandverlies kunnen veroorzaken. De auteurs gebruikten een muismodel van tandvleesziekte waarbij bacteriële componenten rond de tanden werden aangebracht, en bevestigden met 3D-scans dat de ontsteking leidde tot duidelijk botverlies. Ze concentreerden zich op een molecuul genaamd lincRNA-EPS, een niet-coderend RNA dat al bekendstaat om ontstekingssignalen in andere weefsels te remmen, om te onderzoeken of het ook de activiteit van osteoclasten in deze vijandige omgeving onder controle houdt.
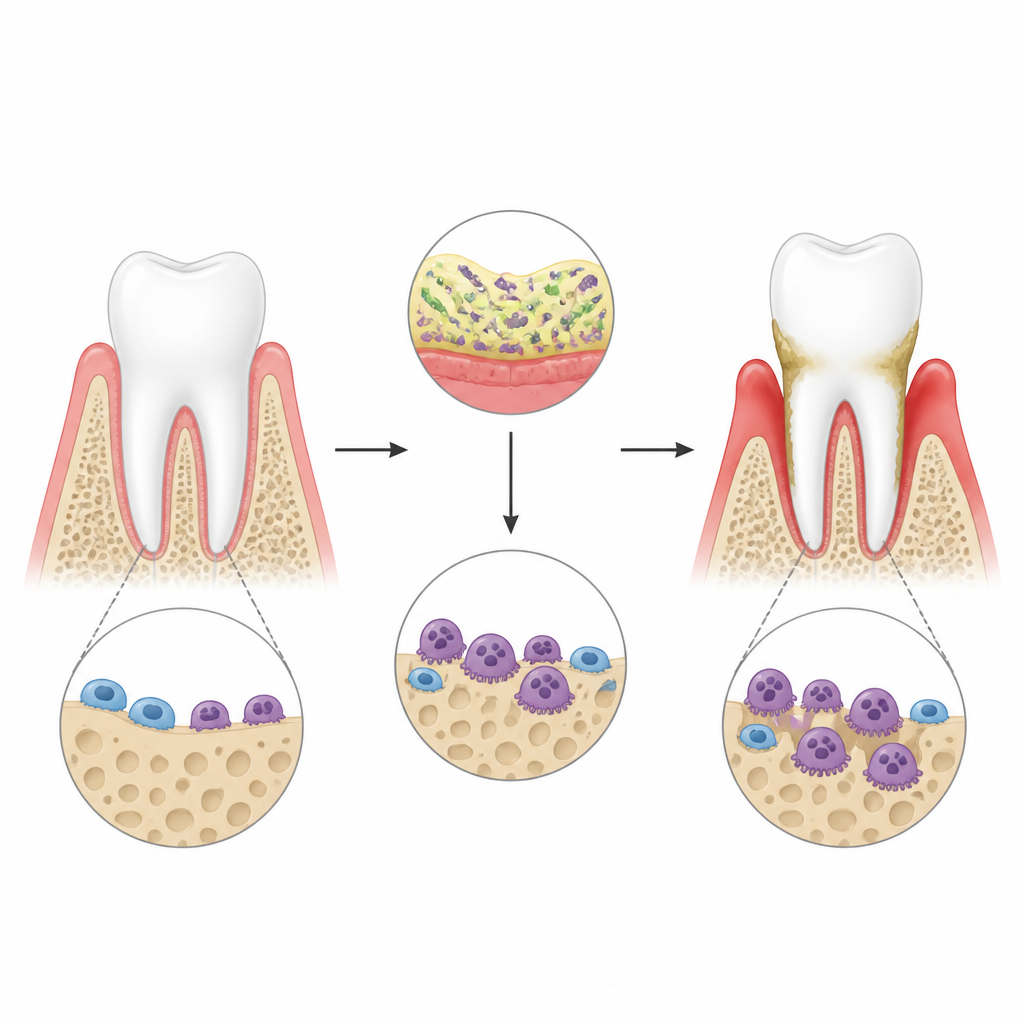
Een beschermend RNA dat botverlies in bedwang houdt
Toen de onderzoekers lincRNA-EPS uit muizen verwijderden, verslechterde het botverlies rond de tanden merkbaar na een tandvleesinfectie. Het kaakbotoppervlak vertoonde meer en grotere osteoclasten, en de putten die zij in botplaten in het laboratorium groeven, waren dieper en wijder. In celkweek werden beenmergcellen van normale en knockout-dieren eerst richting osteoclastdifferentiatie gestimuleerd en daarna blootgesteld aan een ontstekingstrigger die bacteriële toxines nabootst. Cellen zonder lincRNA-EPS ontwikkelden zich gemakkelijker tot agressieve osteoclasten en schakelden botresorberende genen en eiwitten sterker aan. Deze bevindingen suggereren dat lincRNA-EPS normaal gesproken als een rem fungeert op osteoclastgroei en -functie onder ontstekingsstress.
Ijzerhuishouding als de verborgen schakel
Om te begrijpen hoe dit RNA zijn effect uitoefent, vergeleek het team genactiviteit en eiwitpatronen in voorlopercellen en rijpe osteoclasten van normale en knockout-muizen. Ze vonden niet alleen sterkere osteoclastprogramma's, maar ook opvallende veranderingen in routes die ijzergebruik, opslag en transport beheersen. Eén uitgescheiden eiwit, lipocaline-2 (Lcn2), dat ijzer in en uit cellen kan vervoeren, viel op door sterke verhoging wanneer lincRNA-EPS ontbrak, vooral na ontstekingsstimulus. Verdere tests lieten zien dat in weefsels en gekweekte cellen zonder lincRNA-EPS de Lcn2-niveaus hoog bleven, ijzerregulerende eiwitten langer ingeschakeld bleven en mobiel ijzer in osteoclasten verhoogd bleef — allemaal tekenen van een overactieve ijzereconomie die de energie-intensieve boteters voedt.
Het afstemmen van een ijzertransporteur om botbeschadiging te kalmeren
De onderzoekers manipuleerden vervolgens Lcn2 rechtstreeks om te zien hoe het dit systeem beïnvloedt. Het verminderen van Lcn2 in normale voorlopercellen dempte het ijzertransportmechanisme en veranderde de vorm van osteoclasten, waardoor kleinere cellen met minder kernen ontstonden, hoewel hun aantallen konden stijgen. Extra Lcn2 had het tegenovergestelde effect: het bevorderde het fusieproces tot grotere, krachtigere botresorberende eenheden. In muizen met tandvleesziekte verminderde het verlagen van Lcn2 in het weefsel rond de tanden botverlies en osteoclastactiviteit, maar alleen wanneer lincRNA-EPS aanwezig was. Wanneer lincRNA-EPS ontbrak, hadden veranderingen in Lcn2-niveaus of het toevoegen van extra Lcn2 zwakkere en langzamere effecten op ijzerniveaus en osteoclastgedrag, wat suggereert dat dit RNA nodig is voor een snelle en stabiele aanpassing van de ijzerstofwisseling tijdens ontsteking.
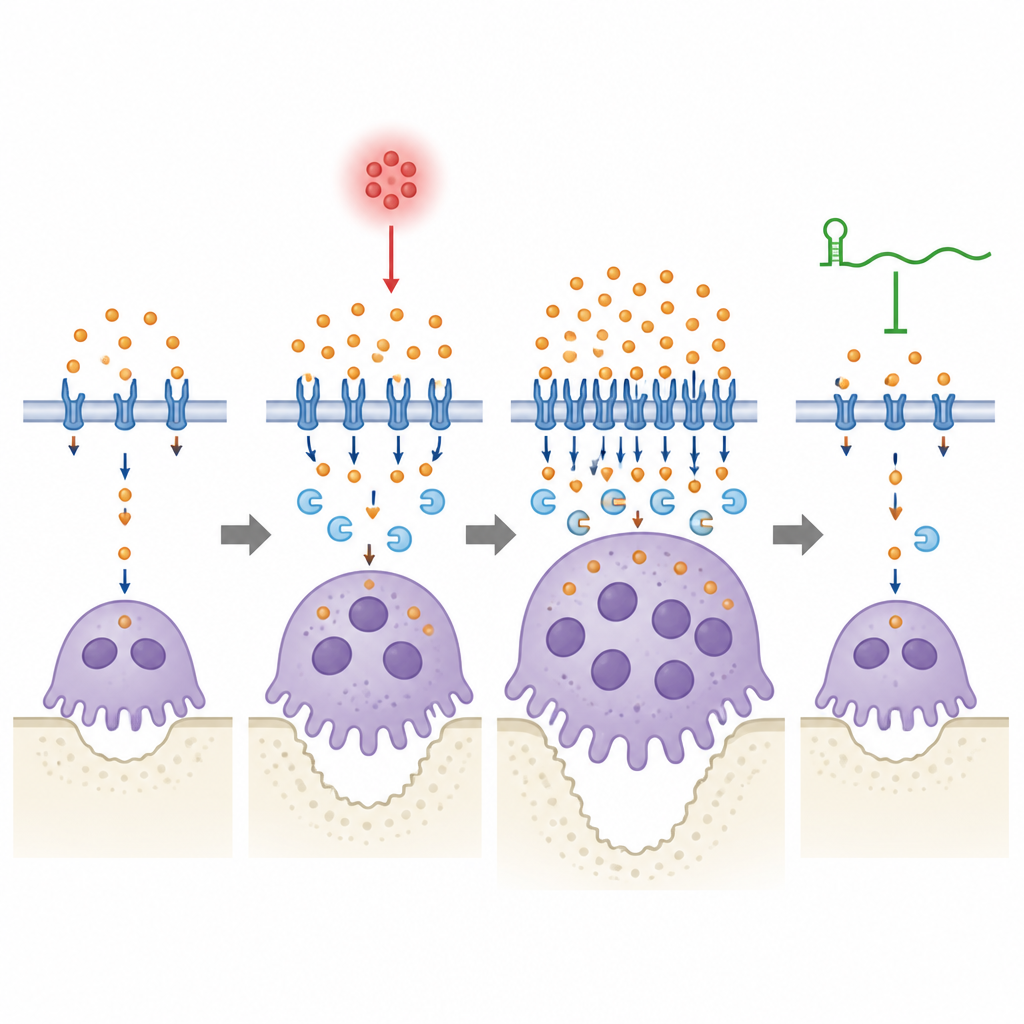
Een fijn afgestemde balans tussen ijzer en bot
Voor een breed publiek laat dit werk zien dat een regulerend RNA, lincRNA-EPS, het kaakbot helpt overleven tijdens een tandvleesinfectie door te voorkomen dat botetende cellen zich tegoed doen aan ijzer en te lang overactief blijven. In een ontstoken mond stijgt Lcn2 en duwt het meer ijzer in osteoclasten, wat hun groei en botafbraak bevordert; lincRNA-EPS helpt deze cellen dat surplus te herkennen en te corrigeren zodat het ijzergebruik terugkeert naar een veilig niveau. Wanneer het RNA ontbreekt, faalt dit veiligheidssysteem, blijft de ijzerhuishouding excessief en verslechtert het botverlies. Hoewel de studie preklinisch is, benadrukt ze ijzerregulatie en het lincRNA-EPS–Lcn2-koppel als potentiële doelen voor toekomstige therapieën die tanden willen beschermen door botresorptie geleidelijk te remmen in plaats van volledig uit te schakelen.
Bronvermelding: Wang, J., Wang, Y., Zhang, Z. et al. LincRNA-EPS alleviates osteoclastogenesis under inflammatory microenvironment through preventing excessive iron metabolism. Cell Death Dis 17, 444 (2026). https://doi.org/10.1038/s41419-026-08716-y
Trefwoorden: parodontitis, osteoclasten, ijzerstofwisseling, lipocaline-2, lange niet-coderende RNA