Clear Sky Science · pl
LincRNA-EPS łagodzi osteoklastogenezę w zapalnym mikrośrodowisku poprzez zapobieganie nadmiernemu metabolizmowi żelaza
Dlaczego to ma znaczenie dla bolących dziąseł i łamliwych zębów
Wielu dorosłych żyje z krwawiącymi dziąsłami i ruszającymi się zębami spowodowanymi zapaleniem przyzębia — przewlekłą infekcją, która cicho niszczy kość utrzymującą zęby. To badanie zagląda w głąb tego procesu i odkrywa, jak mało znana cząsteczka RNA pomaga utrzymać równowagę między komórkami niszczącymi kość a gospodarką żelaza, wskazując nowe sposoby ochrony szczęki podczas choroby dziąseł.
Pracujące „zjadacze kości” w zapalnych dziąsłach
W zapaleniu przyzębia bakterie wokół zębów wywołują silną odpowiedź immunologiczną w dziąsłach. To zapalenie aktywuje specjalne komórki rozpuszczające kość — osteoklasty — które drążą jamy w kości szczęki i ostatecznie mogą prowadzić do utraty zęba. Autorzy zastosowali model myszy z chorobą przyzębia wywołaną komponentami bakteryjnymi umieszczonymi wokół zębów i potwierdzili za pomocą skanów 3D, że zapalenie prowadzi do wyraźnej utraty kości. Skoncentrowali się na cząsteczce nazwanej lincRNA-EPS, niekodującym RNA już znanym z tłumienia sygnałów zapalnych w innych tkankach, aby sprawdzić, czy także ogranicza aktywność osteoklastów w tym trudnym środowisku.
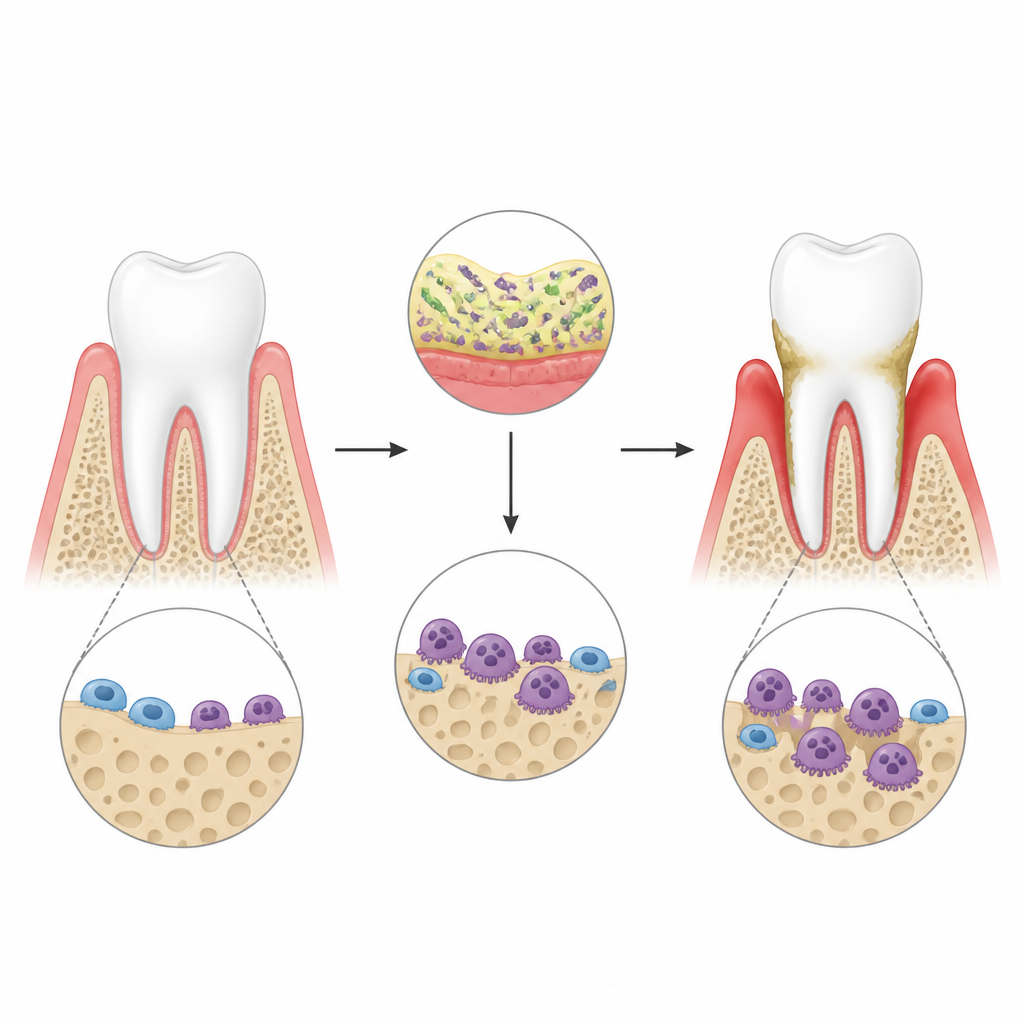
Ochronny RNA, który hamuje utratę kości
Gdy badacze usunęli lincRNA-EPS u myszy, utrata kości wokół zębów po infekcji dziąseł stała się wyraźnie większa. Powierzchnia szczęki wykazywała więcej i większe osteoklasty, a zagłębienia, które te komórki wyżłobiły w preparatach kostnych w laboratorium, były głębsze i szersze. W hodowli komórkowej komórki szpiku kostnego z myszy normalnych i z defektem lincRNA-EPS najpierw stymulowano do różnicowania w osteoklasty, a potem narażano na czynnik zapalny naśladujący toksyny bakteryjne. Komórki pozbawione lincRNA-EPS przekształcały się łatwiej w agresywne osteoklasty i uruchamiały geny oraz białka odpowiedzialne za resorpcję kości na wyższym poziomie. Wyniki te sugerują, że lincRNA-EPS działa jak hamulec dla wzrostu i funkcji osteoklastów w warunkach stresu zapalnego.
Gospodarka żelazem jako ukryte ogniwo
Aby zrozumieć mechanizm działania tego RNA, zespół porównał aktywność genów i wzorce białkowe w komórkach prekursorowych oraz dojrzałych osteoklastach u myszy normalnych i z mutacją. Odkryli nie tylko wzmocnione programy osteoklastogenne, ale też wyraźne zmiany w szlakach kontrolujących wykorzystanie, magazynowanie i transport żelaza. Jedno wydzielane białko, lipokalina-2 (Lcn2), które może transportować żelazo do i z komórek, wyróżniało się znacznym wzrostem przy braku lincRNA-EPS, zwłaszcza po stymulacji zapalnej. Dalsze testy wykazały, że w tkankach i hodowlach komórek bez lincRNA-EPS poziomy Lcn2 pozostawały podwyższone, białka zajmujące się gospodarowaniem żelazem były dłużej aktywne, a wolne żelazo wewnątrz osteoklastów utrzymywało się na podwyższonym poziomie — wszystkie te cechy wskazują na nadmiernie aktywną gospodarkę żelazem, która zasila energetyczne, „żerne” osteoklasty.
Dostrajanie transportera żelaza, by złagodzić uszkodzenia kości
Naukowcy bezpośrednio manipulowali poziomami Lcn2, aby zobaczyć, jak wpływa ono na układ. Zmniejszenie Lcn2 w normalnych komórkach prekursorowych osłabiło maszynerię transportu żelaza i zmieniło kształt osteoklastów, dając mniejsze komórki z mniejszą liczbą jąder, choć ich liczba mogła wzrosnąć. Dodatkowe Lcn2 działało odwrotnie — sprzyjało fuzji komórek w większe, wydajniejsze jednostki resorbujące kość. U myszy z chorobą przyzębia obniżenie Lcn2 w tkankach wokół zębów zmniejszyło utratę kości i aktywność osteoklastów, ale tylko jeśli obecny był lincRNA-EPS. Gdy lincRNA-EPS brakowało, zmiany poziomu Lcn2 lub dodatkowe Lcn2 miały słabsze i wolniejsze efekty na poziom żelaza i zachowanie osteoklastów, co sugeruje, że ten RNA jest potrzebny do szybkiej i trwałej regulacji metabolizmu żelaza podczas zapalenia.
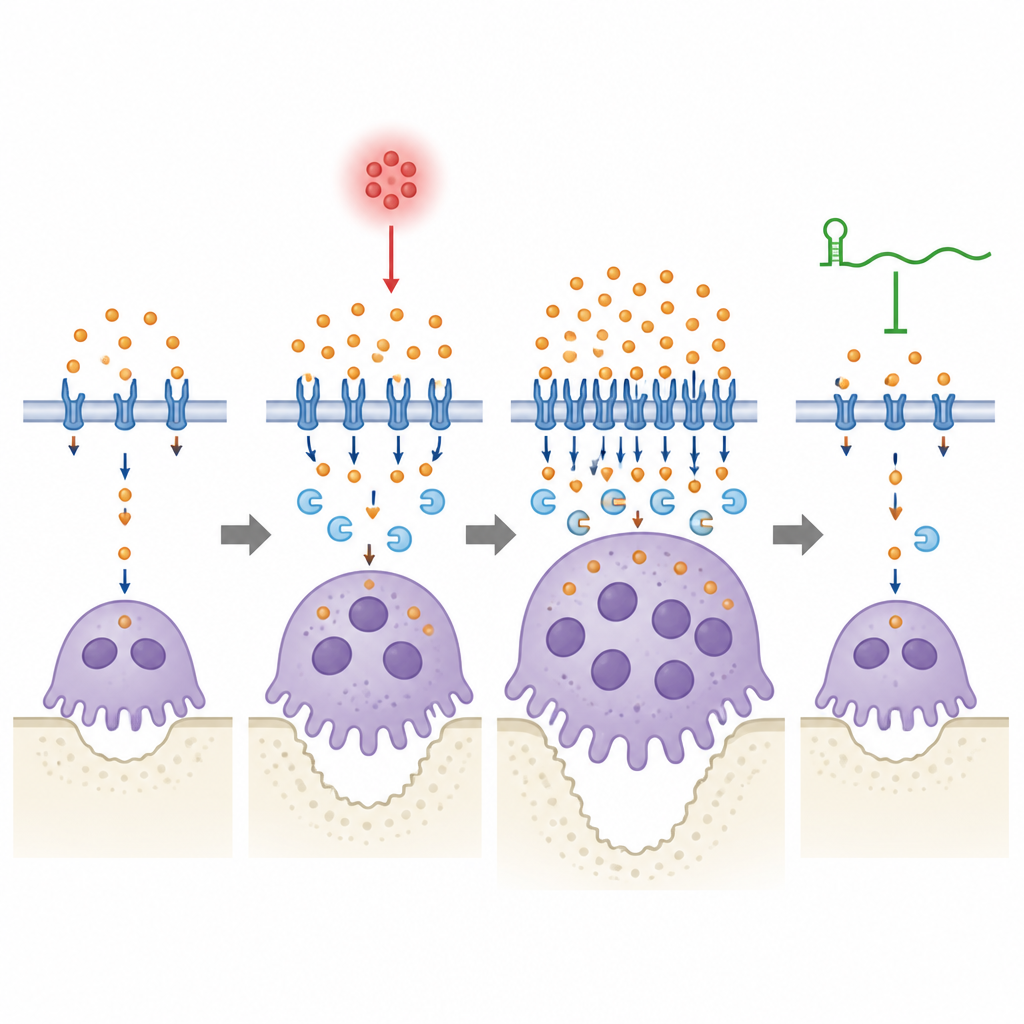
Delikatna równowaga między żelazem a kością
Z perspektywy laika praca ta pokazuje, że regulatorowy RNA, lincRNA-EPS, pomaga szczęce przetrwać infekcję dziąseł, zapobiegając temu, by komórki rozpuszczające kość nie objadały się żelazem i nie pozostawały nadmiernie aktywne zbyt długo. W zapalnym środowisku poziom Lcn2 rośnie i zwiększa napływ żelaza do osteoklastów, co sprzyja ich rozrostowi i niszczeniu kości; lincRNA-EPS pomaga tym komórkom wyczuć i skorygować ten napływ, tak by zużycie żelaza wróciło do bezpiecznego poziomu. Gdy RNA brak, ten zawór bezpieczeństwa zawodzi, gospodarka żelazem pozostaje nadmierna, a utrata kości pogłębia się. Chociaż badanie ma charakter przedkliniczny, podkreśla regulację żelaza oraz parę lincRNA-EPS–Lcn2 jako potencjalne cele przyszłych terapii, które mogłyby chronić zęby przez łagodne spowolnienie resorpcji kości zamiast jej całkowitego zahamowania.
Cytowanie: Wang, J., Wang, Y., Zhang, Z. et al. LincRNA-EPS alleviates osteoclastogenesis under inflammatory microenvironment through preventing excessive iron metabolism. Cell Death Dis 17, 444 (2026). https://doi.org/10.1038/s41419-026-08716-y
Słowa kluczowe: zapalenie przyzębia, osteoklasty, metabolizm żelaza, lipokalina-2, długa niekodująca RNA