Clear Sky Science · es
LincRNA-EPS alivia la osteoclastogénesis en un microambiente inflamatorio al prevenir el exceso de metabolismo del hierro
Por qué importa para las encías sensibles y los dientes frágiles
Muchos adultos conviven con encías sangrantes y dientes flojos causados por la periodontitis, una infección crónica que destruye silenciosamente el hueso que sujeta los dientes. Este estudio indaga en ese proceso y descubre cómo una molécula de ARN poco conocida ayuda a mantener en equilibrio a las células que comen hueso y el uso del hierro, lo que apunta a nuevas formas de proteger el maxilar durante la enfermedad periodontal.
Los comedores de hueso en acción en las encías inflamadas
En la periodontitis, las bacterias alrededor de los dientes desencadenan una fuerte respuesta inmune en las encías. Esta inflamación activa unas células especiales que comen hueso, llamadas osteoclastos, que excavan el hueso del maxilar y pueden acabar provocando la pérdida dental. Los autores usaron un modelo murino de enfermedad gingival creado con componentes bacterianos atados alrededor de los dientes y confirmaron mediante escaneos 3D que la inflamación condujo a una pérdida ósea evidente. Se centraron en una molécula llamada lincRNA-EPS, un ARN no codificante ya conocido por atenuar señales inflamatorias en otros tejidos, para ver si también frena la actividad osteoclástica en este entorno adverso.
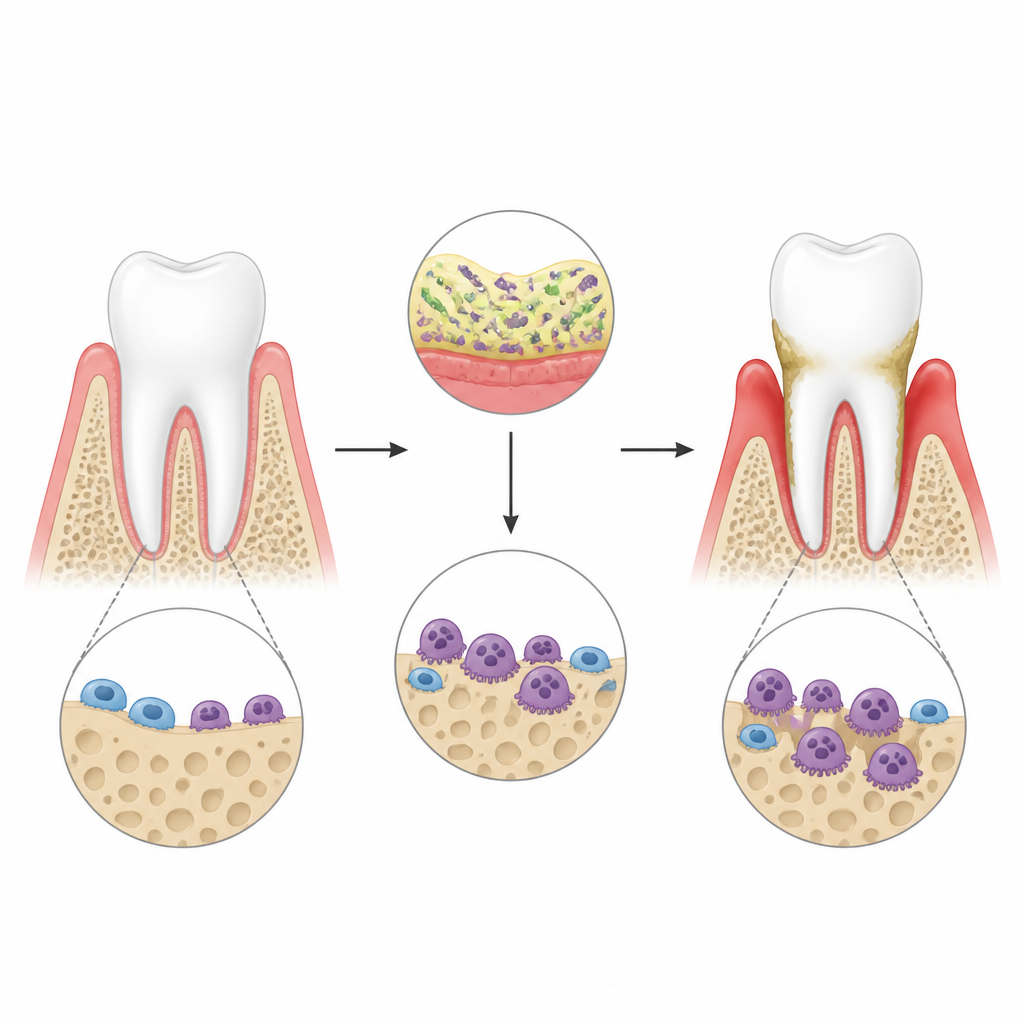
Un ARN protector que contiene la pérdida ósea
Cuando los investigadores eliminaron lincRNA-EPS en ratones, la pérdida ósea alrededor de los dientes empeoró notablemente tras la infección gingival. La superficie del maxilar mostró más osteoclastos y de mayor tamaño, y las cavidades que tallaban en rodajas de hueso en el laboratorio eran más profundas y anchas. En cultivo celular, las células de la médula ósea de animales normales y knockout se indujeron primero a diferenciarse hacia osteoclastos y luego se expusieron a un estímulo inflamatorio que imita toxinas bacterianas. Las células sin lincRNA-EPS se convirtieron más fácilmente en osteoclastos agresivos y activaron genes y proteínas que reabsorben hueso a niveles más altos. Estos hallazgos sugieren que lincRNA-EPS actúa normalmente como un freno sobre el crecimiento y la función osteoclástica bajo estrés inflamatorio.
La gestión del hierro como el vínculo oculto
Para entender cómo ejerce este ARN su efecto, el equipo comparó la actividad génica y los patrones proteicos en células precursoras y osteoclastos maduros de ratones normales y knockout. Encontraron no solo programas osteoclásticos más intensos, sino también cambios llamativos en vías que controlan el uso, el almacenamiento y el transporte del hierro. Una proteína secretada, la lipocalina-2 (Lcn2), que puede transportar hierro hacia dentro y fuera de las células, destacó por su fuerte aumento cuando faltaba lincRNA-EPS, especialmente tras la estimulación inflamatoria. Pruebas adicionales mostraron que en tejidos y células cultivadas sin lincRNA-EPS, los niveles de Lcn2 se mantenían altos, las proteínas implicadas en el manejo del hierro permanecían activadas por más tiempo y el hierro móvil dentro de los osteoclastos seguía elevado: todos signos de una economía del hierro sobreactivada que alimenta a estos comedores de hueso con alta demanda energética.
Ajustando una lanzadera de hierro para calmar el daño óseo
Los científicos manipularon directamente Lcn2 para ver cómo influye en este sistema. Reducir Lcn2 en células precursoras normales atenuó la maquinaria de transporte de hierro y alteró la morfología osteoclástica, produciendo células más pequeñas con menos núcleos, aunque su número podía aumentar. Añadir Lcn2 extra tuvo el efecto opuesto, favoreciendo la fusión en unidades más grandes y potentes de reabsorción ósea. En ratones con enfermedad gingival, disminuir Lcn2 en los tejidos alrededor de los dientes redujo la pérdida ósea y la actividad osteoclástica, pero solo cuando lincRNA-EPS estaba presente. Cuando faltaba lincRNA-EPS, cambiar los niveles de Lcn2 o añadir Lcn2 adicional tuvo efectos más débiles y lentos sobre los niveles de hierro y el comportamiento osteoclástico, lo que sugiere que este ARN es necesario para un ajuste rápido y estable del metabolismo del hierro durante la inflamación.
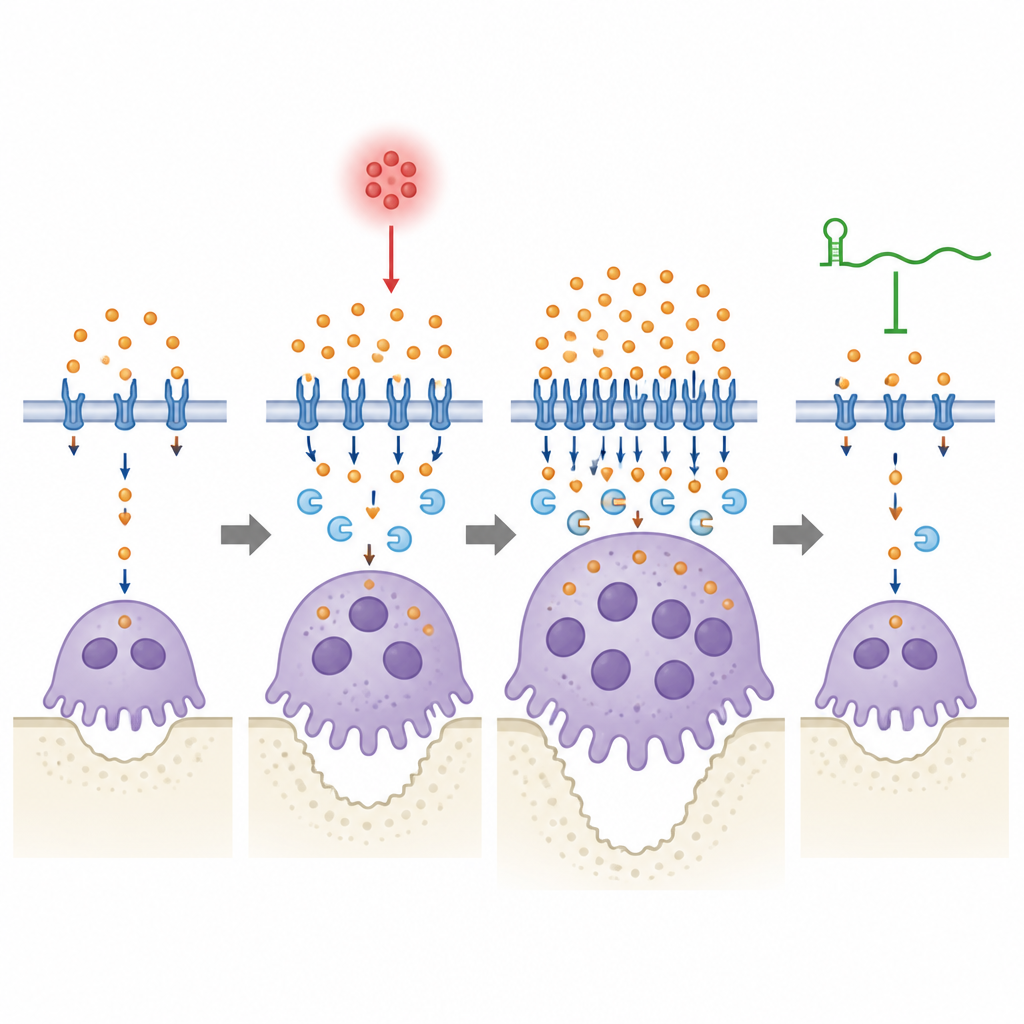
Un equilibrio fino entre el hierro y el hueso
Desde una perspectiva general, este trabajo muestra que un ARN regulador, lincRNA-EPS, ayuda al hueso mandibular a sobrevivir a la infección gingival al impedir que los osteoclastos se harten de hierro y permanezcan hiperactivos durante demasiado tiempo. En una boca inflamada, Lcn2 aumenta y empuja más hierro hacia los osteoclastos, ayudándoles a crecer y a masticar el hueso; lincRNA-EPS ayuda a estas células a detectar y corregir ese aumento para que el uso del hierro vuelva a niveles seguros. Cuando falta el ARN, esta válvula de seguridad falla, la gestión del hierro permanece excesiva y la pérdida ósea empeora. Aunque el estudio es preclínico, pone de relieve la regulación del hierro y el par lincRNA-EPS–Lcn2 como posibles dianas para futuras terapias que busquen proteger los dientes ralentizando con delicadeza la reabsorción ósea en lugar de detenerla por completo.
Cita: Wang, J., Wang, Y., Zhang, Z. et al. LincRNA-EPS alleviates osteoclastogenesis under inflammatory microenvironment through preventing excessive iron metabolism. Cell Death Dis 17, 444 (2026). https://doi.org/10.1038/s41419-026-08716-y
Palabras clave: periodontitis, osteoclastos, metabolismo del hierro, lipocalina-2, ARN largo no codificante