Clear Sky Science · de
LincRNA-EPS mildert Osteoklastogenese im entzündlichen Mikromilieu durch Verhinderung überschüssigen Eisenstoffwechsels
Warum das für entzündetes Zahnfleisch und brüchige Zähne wichtig ist
Viele Erwachsene haben Zahnfleischbluten und lockere Zähne durch Parodontitis, eine chronische Infektion, die still den Knochen abbaut, der die Zähne hält. Diese Studie blickt in diesen Prozess hinein und entdeckt, wie ein wenig bekanntes RNA‑Molekül dazu beiträgt, Osteoklasten und Eisenverwendung im Gleichgewicht zu halten, und damit auf neue Wege hinweist, den Kieferknochen bei Zahnfleischerkrankungen zu schützen.
Die Knochenfresser im entzündeten Zahnfleisch
Bei Parodontitis reizen Bakterien rund um die Zähne das Immunsystem im Zahnfleisch stark. Diese Entzündung „weckt“ spezielle knochenabbauende Zellen, sogenannte Osteoklasten, die Löcher in den Kieferknochen graben und schließlich zum Zahnverlust führen können. Die Autoren verwendeten ein Mausmodell der Zahnfleischerkrankung, das mit bakteriellen Komponenten um die Zähne erzeugt wurde, und bestätigten per 3D‑Scans, dass die Entzündung zu eindeutigem Knochenverlust führt. Sie konzentrierten sich auf ein Molekül namens lincRNA‑EPS, eine nichtkodierende RNA, die bereits dafür bekannt ist, Entzündungsreaktionen in anderen Geweben zu dämpfen, um zu prüfen, ob es auch in dieser belastenden Umgebung die Osteoklastenaktivität bremst.
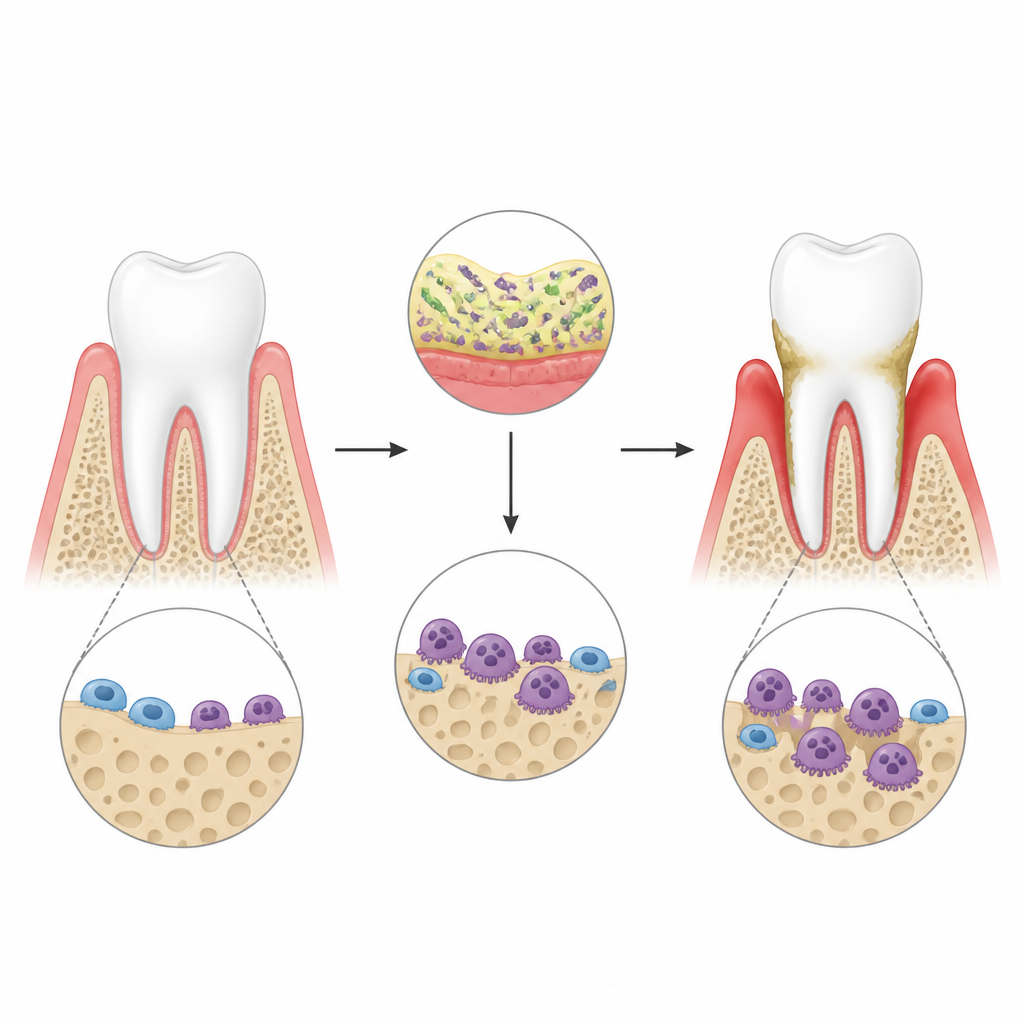
Eine schützende RNA, die Knochenverlust in Schach hält
Als die Forschenden lincRNA‑EPS bei Mäusen entfernten, verschlimmerte sich der Knochenverlust um die Zähne nach der Zahnfleischinfektion deutlich. Die Kieferknochenoberfläche wies mehr und größere Osteoklasten auf, und die Grübchen, die sie in Laborexperimenten in Knochenscheiben fraßen, waren tiefer und breiter. In Zellkulturen wurden Knochenmarkszellen aus normalen und Knockout‑Tieren zunächst in Richtung Osteoklasten differenziert und dann einem entzündlichen Reiz ausgesetzt, der bakteriellen Toxinen ähnelt. Zellen ohne lincRNA‑EPS wurden leichter zu aggressiven Osteoklasten und schalteten Knochenabbau‑Gene und ‑Proteine stärker ein. Diese Befunde deuten darauf hin, dass lincRNA‑EPS normalerweise als Brems‑Mechanismus für Wachstum und Funktion von Osteoklasten unter entzündlichem Stress wirkt.
Eisenverarbeitung als die verborgene Verbindung
Um zu verstehen, wie diese RNA ihre Wirkung entfaltet, verglich das Team die Genaktivität und Proteinprofile in Vorläuferzellen und ausgereiften Osteoklasten aus normalen und Knockout‑Mäusen. Sie fanden nicht nur stärkere Osteoklasten‑Programme, sondern auch markante Veränderungen in Signalwegen, die den Eisengebrauch, die Speicherung und den Transport steuern. Ein sezerniertes Protein, Lipocalin‑2 (Lcn2), das Eisen in die Zelle hinein und heraus transportieren kann, fiel besonders dadurch auf, dass es bei fehlender lincRNA‑EPS stark erhöht war, vor allem nach entzündlicher Stimulation. Weitere Tests zeigten, dass in Geweben und Kulturen ohne lincRNA‑EPS die Lcn2‑Spiegel hoch blieben, eisenregulierende Proteine länger aktiviert blieben und das mobile Eisen in Osteoklasten erhöht war – alles Anzeichen einer überaktiven Eisenökonomie, die die energieintensiven Knochenfresser antreibt.
Ein Eisen‑Shuttle feinjustieren, um Knochenschäden zu dämpfen
Die Forschenden manipulierten anschließend Lcn2 direkt, um zu sehen, wie es das System beeinflusst. Die Reduktion von Lcn2 in normalen Vorläuferzellen dämpfte die eisenvermittelnden Transportmechanismen und veränderte die Form der Osteoklasten, sodass kleinere Zellen mit weniger Zellkernen entstanden, obwohl ihre Zahl steigen konnte. Zusätzliche Lcn2 hatte den gegenteiligen Effekt und förderte das Verschmelzen zu größeren, leistungsfähigeren Knochenresorptions‑Einheiten. In Mäusen mit Zahnfleischentzündung verringerte das Absenken von Lcn2 im Gewebe um die Zähne Knochenverlust und Osteoklastenaktivität, jedoch nur, wenn lincRNA‑EPS vorhanden war. Fehlt lincRNA‑EPS, waren Veränderungen der Lcn2‑Spiegel oder zusätzlich zugeführtes Lcn2 weniger effektiv und langsamer in ihren Auswirkungen auf Eisenwerte und Osteoklastenverhalten, was darauf hindeutet, dass diese RNA für eine schnelle und stabile Anpassung des Eisenstoffwechsels während Entzündung erforderlich ist.
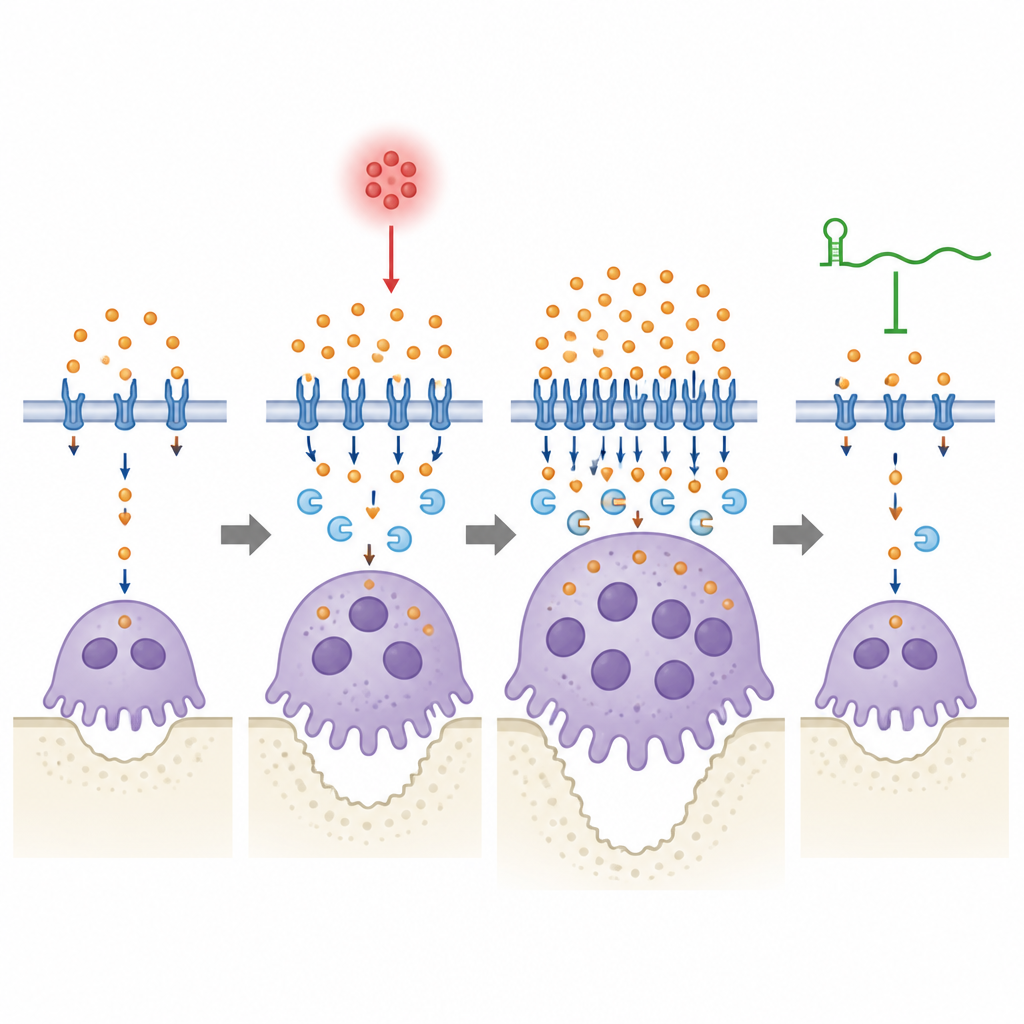
Ein fein austariertes Gleichgewicht zwischen Eisen und Knochen
Aus allgemeinverständlicher Sicht zeigt diese Arbeit, dass eine regulatorische RNA, lincRNA‑EPS, dem Kieferknochen während einer Zahnfleischinfektion hilft, indem sie verhindert, dass knochenabbauende Zellen sich an Eisen überfressen und zu lange überaktiv bleiben. In einem entzündeten Mund steigt Lcn2 an und treibt mehr Eisen in die Osteoklasten, was ihr Wachstum und ihre Knochendegradation fördert; lincRNA‑EPS hilft diesen Zellen, diese Spitze zu erfassen und zu korrigieren, sodass der Eisenverbrauch auf ein sicheres Niveau zurückkehrt. Fehlt die RNA, versagt dieses Sicherheitsventil, die Eisenhandhabung bleibt übermäßig und der Knochenverlust verschlechtert sich. Obwohl die Studie präklinisch ist, hebt sie die Eisenregulation und das lincRNA‑EPS–Lcn2‑Paar als potenzielle Ziele für künftige Therapien hervor, die darauf abzielen, Zähne zu schützen, indem sie den Knochenabbau sanft verlangsamen statt vollständig zu blockieren.
Zitation: Wang, J., Wang, Y., Zhang, Z. et al. LincRNA-EPS alleviates osteoclastogenesis under inflammatory microenvironment through preventing excessive iron metabolism. Cell Death Dis 17, 444 (2026). https://doi.org/10.1038/s41419-026-08716-y
Schlüsselwörter: Parodontitis, Osteoklasten, Eisenstoffwechsel, Lipocalin‑2, lange nichtkodierende RNA