Clear Sky Science · he
lincRNA‑EPS מקל על יצירת אוסטאוקלסטים במיקרו‑סביבה דלקתית על‑ידי מניעת מטבוליזם ברזל מופרז
מדוע זה חשוב לחניכיים כואבות ולשיניים שבירות
מבוגרים רבים חיים עם דימום חניכיים ושיניים רופפות הנגרמים על‑ידי מחלת חניכיים כרונית, זיהום שקט המאכל עצם שמחזיקה את השיניים במקומן. המחקר חוקר את התהליך הזה ומגלה כיצד מולקולת RNA פחות מוכרת מסייעת לשמור על איזון בין תאים אוכלי‑עצם לשימוש בברזל, ומצביע על דרכים חדשות להגן על לסת בזמן מחלת חניכיים.
תאי "אוכלי העצם" בפעולה בחניכיים דלקתיים
במחלת חניכיים, חיידקים סביב השיניים מעוררים תגובה חיסונית חזקה בחניכיים. הדלקת מפעילה תאים מיוחדים אוכלי עצם הנקראים אוסטאוקלסטים, שחופרים גומות בעצם הלסת ויכולים בסוף להוביל לאובדן שיניים. המחברים השתמשו במודל עכבר של מחלת חניכיים שנוצר על‑ידי רכיבים חיידקיים קשורים סביב השיניים, ואישרו בסריקות תלת‑ממד שהדלקת הובילה לאובדן עצם ברור. הם התמקדו במולקולה בשם lincRNA‑EPS, RNA לא מקודד שכבר ידוע כמעכב אותות דלקתיים ברקמות אחרות, כדי לבדוק האם היא גם מרסן פעילות אוסטאוקלסטית בסביבה הקשה הזו.
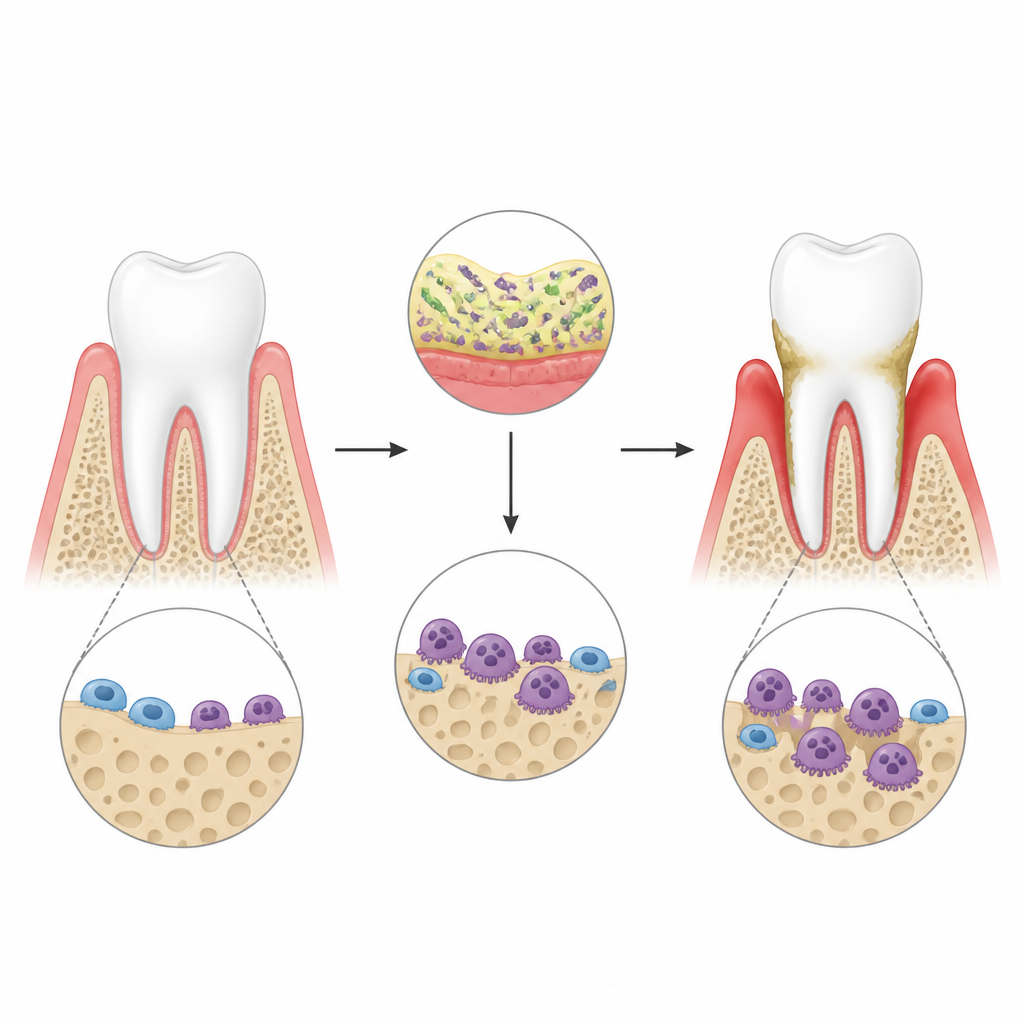
RNA מגן ששומר על אובדן עצם במגבלות
כאשר החוקרים הסירו את lincRNA‑EPS מעכברים, אובדן העצם סביב השיניים החמיר באופן בולט לאחר זיהום החניכיים. משטח הלסת הראה יותר אוסטאוקלסטים וגדולים יותר, והגומות שהם חפרו בפרוסות עצם במעבדה היו עמוקות ורחבות יותר. בתרבית תאים, תאי מוח העצם מעכברים רגילים ומ knockout נדחקו ראשית לעבר התמיינות לאוסטאוקלסטים, ואז נחשפו לגירוי דלקתי המדמה רעלנים חיידקיים. תאים חסרי lincRNA‑EPS הפכו לאוסטאוקלסטים תוקפניים ביתר קלות והפעילו גנים וחלבונים המפרקים עצם ברמות גבוהות יותר. ממצאים אלה מצביעים על כך ש‑lincRNA‑EPS בדרך כלל פועלת כבלם על גדילה ותפקוד האוסטאוקלסטים תחת מתחים דלקתיים.
טיפול בברזל כקישור נסתר
כדי להבין כיצד ה‑RNA הזה מפעיל את השפעתו, הקבוצה השוותה פעילות גנים ודפוסי חלבונים בתאי‑הקדמה ובאוסטאוקלסטים בוגרים מעכברים רגילים ומ knockout. הם מצאו לא רק תכניות אוסטאוקלסטיות חזקות יותר, אלא גם שינויים בולטים במסלולים השולטים בשימוש, אחסון והעברת ברזל. חלבון מופרש אחד, ליפוקלין‑2 (Lcn2), שיכול לשנע ברזל לתוך התא ומחוצה לו, בלט ברמות גבוהות כשה‑lincRNA‑EPS נעדר, במיוחד לאחר גירוי דלקתי. בדיקות נוספות הראו שברקמות ובתאים מתרבית ללא lincRNA‑EPS, רמות Lcn2 נשארו גבוהות, חלבוני טיפול בברזל נשארו מופעלים לפרקי זמן ארוכים יותר, וברזל נייד בתוך האוסטאוקלסטים נשאר גבוה — כל אלה סימנים לכלכלה של ברזל יתר שהדלה את תאי ה"אוכלי־העצם" התובעניים באנרגיה.
כיול מעביר ברזל להרגעת נזק לעצם
המדענים לאחר מכן המניפולו ישירות ב‑Lcn2 כדי לראות כיצד הוא משפיע על המערכת. הקטנת Lcn2 בתאי‑הקדמה רגילים החלישה את מכונת הובלת הברזל ושינתה את צורת האוסטאוקלסטים, ויצרה תאים קטנים יותר עם פחות גרעינים, אף שעלולים להתרבות במספר. הוספת Lcn2 עודפת נתנה את ההשפעה ההפוכה, וסייעה לתאים להתאחד ליחידות גדולות וחזקות יותר המפרקות עצם. בעכברים עם מחלת חניכיים, הורדת Lcn2 ברקמות סביב השיניים הפחיתה אובדן עצם ופעילות אוסטאוקלסטית, אך רק כאשר lincRNA‑EPS היה נוכח. כאשר lincRNA‑EPS נעדר, שינוי רמות Lcn2 או הוספת Lcn2 חיצוני השפיעו באופן חלש ואיטי יותר על רמות הברזל והתנהגות האוסטאוקלסטים, מה שמעיד כי ה‑RNA הזה דרוש לכיול מהיר ויציב של מטבוליזם הברזל בזמן דלקת.
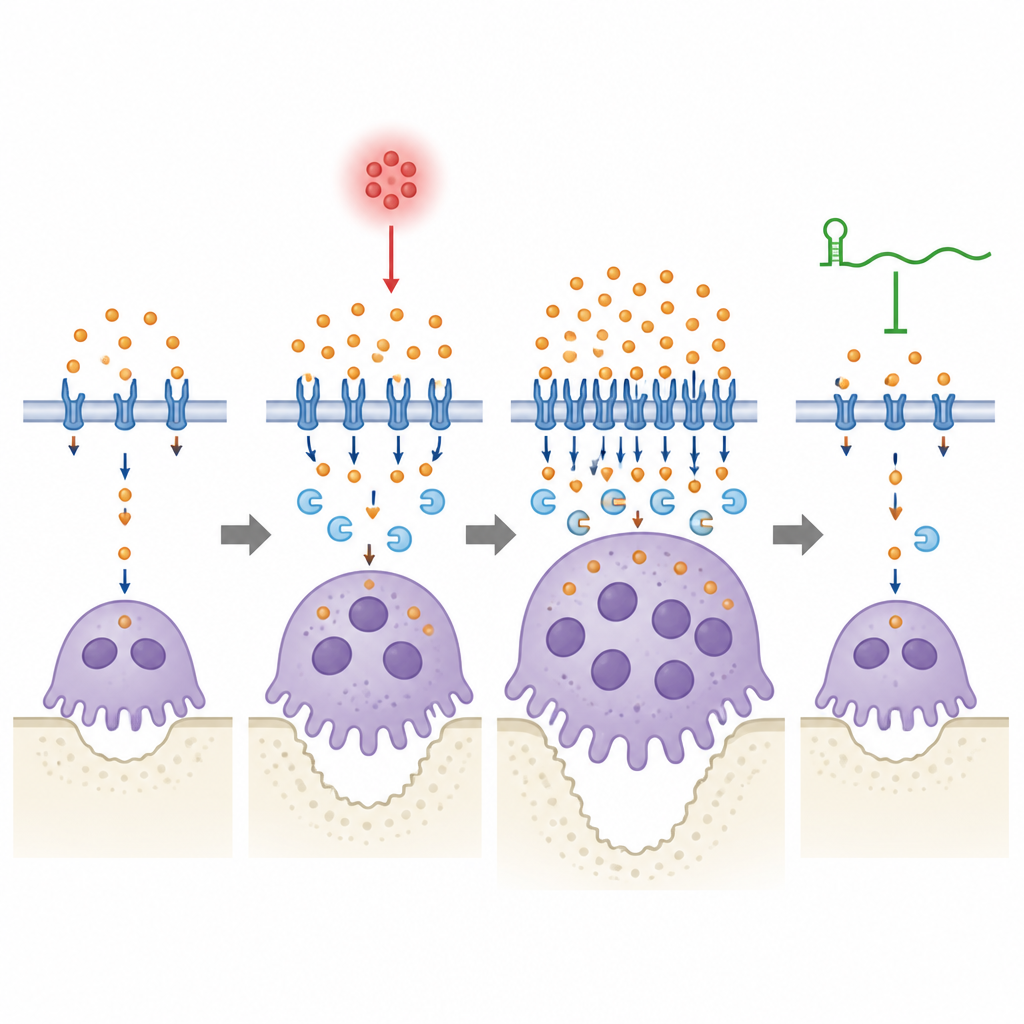
איזון מדויק בין ברזל ועצם
מנקודת מבט של קורא שאינו מומחה, העבודה מראה כי RNA רגולטורי, lincRNA‑EPS, מסייע לעצם הלסת לשרוד זיהום חניכיים על‑ידי מניעת כך שאוסטאוקלסטים יאכלו ברזל בהגזמה וישארו פעילים יותר מדי זמן. בפה דלקתי, Lcn2 עולה ודוחף יותר ברזל לתוך האוסטאוקלסטים, מסייע להם לגדול ולחרוש את העצם; lincRNA‑EPS עוזר לתאים אלה לחוש את הזינוק ולתקנו כך ששימוש הברזל חוזר לרמה בטוחה. כאשר ה‑RNA חסר, שסתום הבטיחות הזה נכשל, טיפול הברזל נשאר יתר־ממדי, ואובדן העצם מחמיר. אף על‑פי שהמחקר הינו פרה‑קליני, הוא מדגיש את ויסות הברזל וזוג lincRNA‑EPS–Lcn2 כיעדים פוטנציאליים לטיפולים עתידיים שמטרתם להגן על השיניים על‑ידי האטה עדינה של ספיגת העצם במקום להפסיקה לחלוטין.
ציטוט: Wang, J., Wang, Y., Zhang, Z. et al. LincRNA-EPS alleviates osteoclastogenesis under inflammatory microenvironment through preventing excessive iron metabolism. Cell Death Dis 17, 444 (2026). https://doi.org/10.1038/s41419-026-08716-y
מילות מפתח: מחלת חניכיים, אוסטאוקלסטים, מטבוליזם ברזל, ליפוקלין‑2, RNA לא מקודד ארוך