Clear Sky Science · ru
lincRNA‑EPS ослабляет остеокластогенез в воспалённой среде, предотвращая чрезмерный обмен железа
Почему это важно при болящих дёснах и хрупких зубах
Многие взрослые живут с кровоточивостью дёсен и подвижностью зубов из‑за пародонтита — хронической инфекции, которая незаметно разъедает кость, удерживающую зубы. В этом исследовании изучают механизмы этого процесса и обнаруживают, как малоизвестная молекула РНК помогает поддерживать равновесие между клетками, разрушающими кость, и использованием железа, указывая на новые подходы к защите челюстной кости при заболевании дёсен.
«Пожиратели кости» в работе при воспалении дёсен
При пародонтите бактерии вокруг зубов вызывают сильный иммунный ответ в дёснах. Это воспаление активирует специализированные клетки, разрушающие кость — остеокласты, которые прокладывают поры в челюстной кости и в конечном счёте могут привести к потере зубов. Авторы использовали модель заболевания дёсен у мышей, созданную с помощью бактериальных компонентов, помещённых вокруг зубов, и подтвердили трёхмерными снимками, что воспаление вызывает заметную потерю кости. Они сосредоточились на молекуле под названием lincRNA‑EPS, некодирующей РНК, уже известной как успокаивающая воспалительные сигналы в других тканях, чтобы проверить, сдерживает ли она активность остеокластов в этой суровой среде.
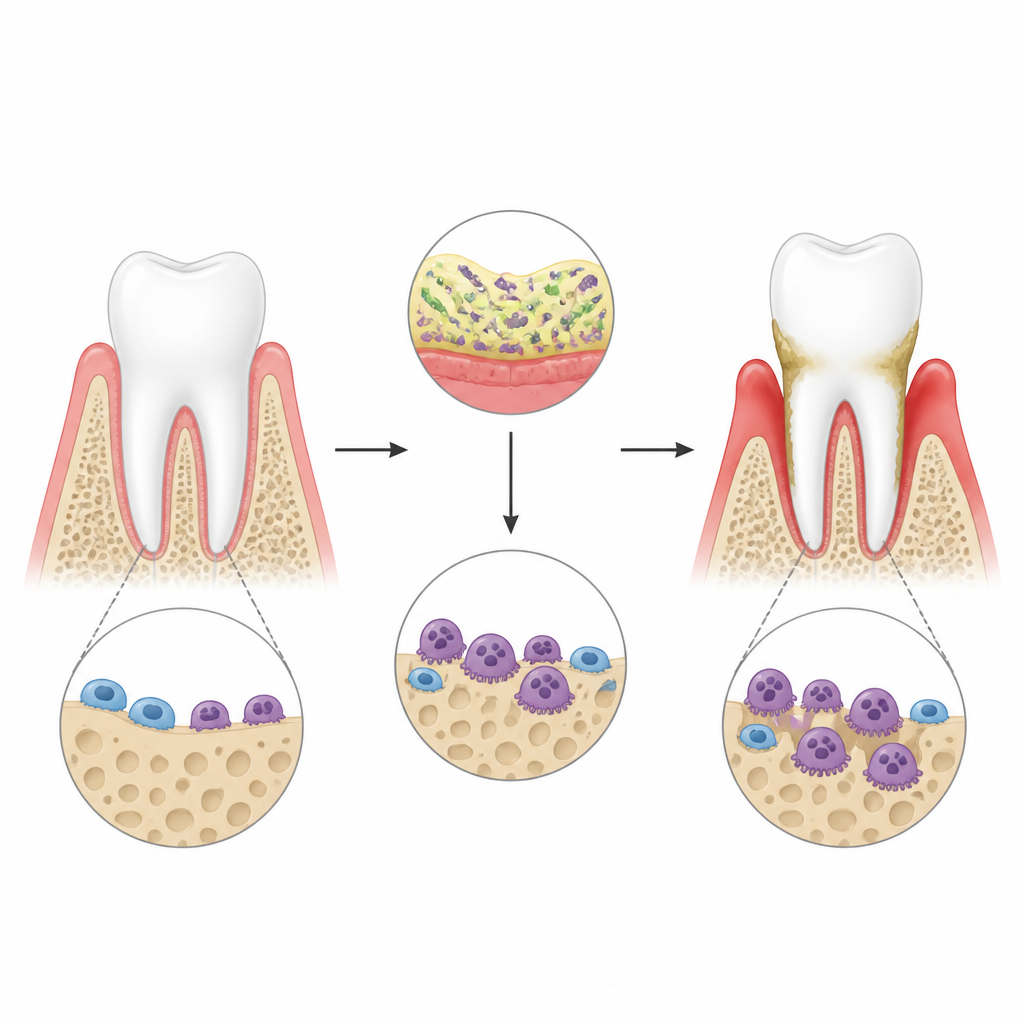
Защитная РНК, сдерживающая потерю кости
Когда исследователи удалили lincRNA‑EPS у мышей, потеря кости вокруг зубов после инфекции дёсен стала заметно серьёзнее. На поверхности челюсти выявили больше и более крупные остеокласты, а углубления, которые они вырезали в образцах кости в лаборатории, были глубже и шире. В клеточных культурах клетки костного мозга от нормальных и «нокаутных» животных сначала направляли на превращение в остеокласты, затем подвергали воспалительному стимулу, имитирующему бактериальные токсины. Клетки, лишённые lincRNA‑EPS, охотнее превращались в агрессивные остеокласты и активировали гены и белки, ответственные за резорбцию кости, в более высоких уровнях. Эти данные позволяют предположить, что lincRNA‑EPS обычно действует как тормоз роста и функции остеокластов при воспалительном стрессе.
Обращение с железом как скрытая связь
Чтобы понять, как эта РНК реализует своё влияние, группа сравнила активность генов и профиль белков в предшественниках остеокластов и в зрелых остеокластах у нормальных и нокаутных мышей. Они нашли не только усиленные программы остеокластогенеза, но и заметные изменения в путях, контролирующих использование, хранение и транспорт железа. Один секретируемый белок, липокалин‑2 (Lcn2), который может переносить железо внутрь и наружу из клеток, выделялся особенно сильно при отсутствии lincRNA‑EPS, особенно после воспалительной стимуляции. Дальнейшие тесты показали, что в тканях и культурах клеток без lincRNA‑EPS уровни Lcn2 оставались высокими, белки, участвующие в обращении с железом, дольше оставались включёнными, а подвижное (лабораторно измеряемое) железо внутри остеокластов сохранялось повышенным — все признаки чрезмерной «железной экономики», подпитывающей энергоёмких разрушителей кости.
Настройка железного «пассажира», чтобы успокоить повреждение кости
Ученые затем напрямую манипулировали Lcn2, чтобы выяснить, как он влияет на систему. Снижение Lcn2 в нормальных предшественниках ослабляло механизмы транспорта железа и меняло форму остеокластов, давая более мелкие клетки с меньшим числом ядер, хотя их количество могло возрасти. Добавление дополнительного Lcn2 имело противоположный эффект, способствуя слиянию клеток в более крупные, более мощные единицы, резорбирующие кость. У мышей с заболеванием дёсен снижение Lcn2 в тканях вокруг зубов уменьшало потерю кости и активность остеокластов, но только при наличии lincRNA‑EPS. Когда lincRNA‑EPS отсутствовала, изменение уровней Lcn2 или добавление его избытка имело более слабые и замедленные эффекты на уровни железа и поведение остеокластов, что указывает на то, что эта РНК необходима для быстрой и устойчивой настройки обмена железа при воспалении.
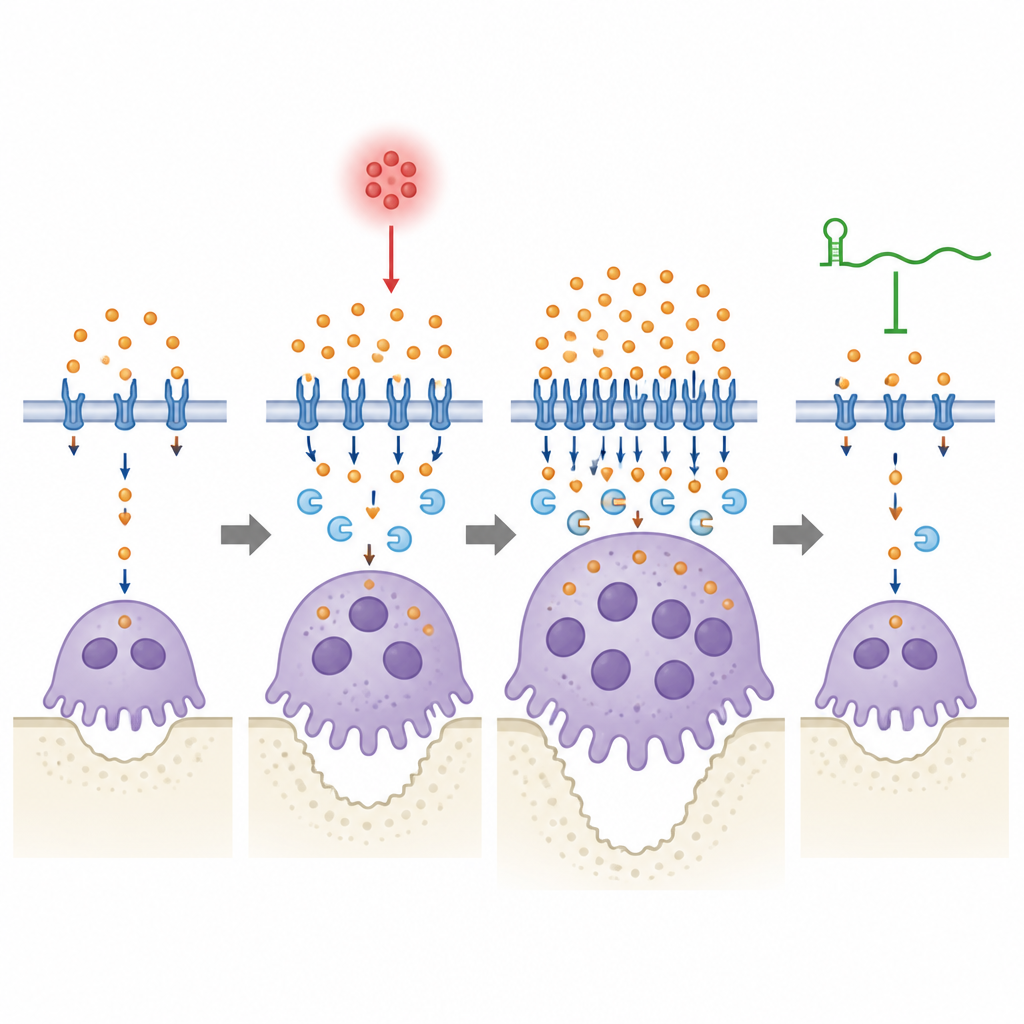
Тонкая настройка баланса между железом и костью
С точки зрения неспециалиста, эта работа показывает, что регуляторная РНК lincRNA‑EPS помогает челюстной кости пережить инфекцию дёсен, предотвращая «пожирание» железа остеокластами и их длительную гиперактивность. При воспалённой ротовой полости Lcn2 повышается и способствует притоку железа в остеокласты, помогая им расти и разъедать кость; lincRNA‑EPS помогает этим клеткам почувствовать и скорректировать этот всплеск, чтобы потребление железа вернулось к безопасному уровню. При отсутствии РНК этот предохранительный клапан не срабатывает, обращение с железом остаётся чрезмерным и потеря кости усугубляется. Хотя исследование доклиническое, оно подчёркивает регуляцию железа и пару lincRNA‑EPS–Lcn2 как потенциальные мишени для будущих терапий, направленных на защиту зубов путём мягкого замедления резорбции кости, а не полного её подавления.
Цитирование: Wang, J., Wang, Y., Zhang, Z. et al. LincRNA-EPS alleviates osteoclastogenesis under inflammatory microenvironment through preventing excessive iron metabolism. Cell Death Dis 17, 444 (2026). https://doi.org/10.1038/s41419-026-08716-y
Ключевые слова: пародонтит, остеокласты, обмен железа, липокалин‑2, длинная некодирующая РНК