Clear Sky Science · ar
يخفف lincRNA-EPS تكون الخلايا الهادمة للعظم في بيئة التهابية عن طريق منع فرط استقلاب الحديد
لماذا يهم هذا للثة المؤلمة والأسنان الهشة
يعاني كثير من البالغين من نزف اللثة وتساقط الأسنان بسبب التهاب دواعم السن، وهو عدوى مزمنة تلتهم بهدوء العظم الذي يثبت الأسنان في مكانها. تبحث هذه الدراسة داخل هذه العملية وتكشف كيف يساعد جزيء RNA غير معروف على نطاق واسع في الحفاظ على توازن خلايا آكلة العظم واستخدام الحديد، مما يشير إلى سبل جديدة لحماية عظم الفك أثناء مرض اللثة.
آكلة العظم تعمل في اللثة الملتهبة
في التهاب دواعم السن، تُحرض البكتيريا حول الأسنان استجابة مناعية قوية في اللثة. يوقظ هذا الالتهاب خلايا خاصة هادمة للعظم تُسمى الخلايا الهادمة للعظم، التي تحفر ثقوبًا في عظم الفك وقد تؤدي في النهاية إلى فقدان الأسنان. استخدم المؤلفون نموذج فأر لمرض اللثة نُشئ بمكونات بكتيرية مربوطة حول الأسنان، وأكدوا بواسطة مسح ثلاثي الأبعاد أن الالتهاب أدى إلى فقدان واضح للعظم. ركزوا على جزيء اسمه lincRNA-EPS، وهو RNA غير مشفر معروف بالفعل بتهدئة الإشارات الالتهابية في أنسجة أخرى، ليروا ما إذا كان يقيّم نشاط الخلايا الهادمة للعظم في هذه البيئة القاسية.
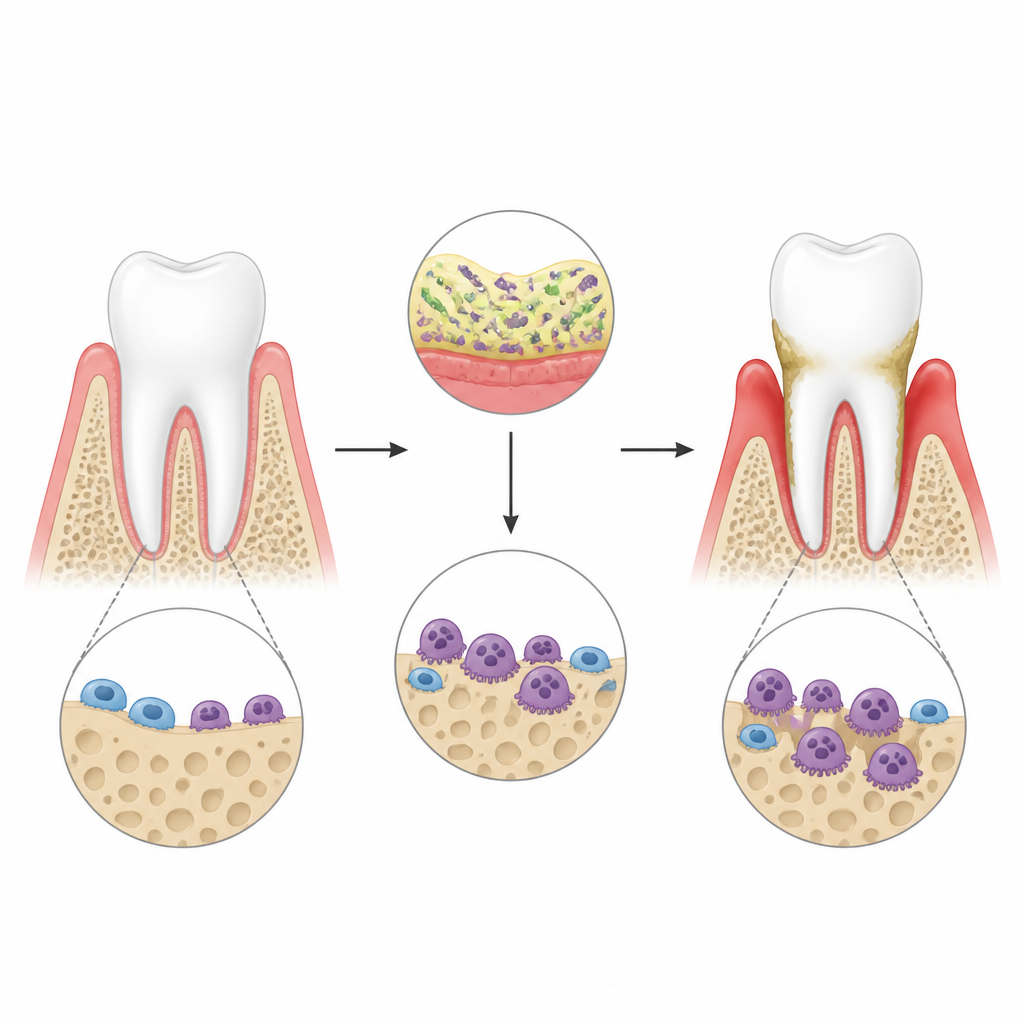
RNA واقٍ يحد من فقدان العظم
عندما أزال الباحثون lincRNA-EPS من الفئران، ساء فقدان العظم حول الأسنان بوضوح بعد عدوى اللثة. أظهرت سطحية عظم الفك خلايا هادمة للعظم أكثر وحجمًا أكبر، وكانت الحفريات التي حفروها في شرائح العظم في المختبر أعمق وأوسع. في ثقافات خلوية، حُفِّزت خلايا نخاع العظم من حيوانات طبيعية ومعدلة أولاً لتتحول إلى خلايا هادمة للعظم، ثم تعرَّضت لمسبب التهابي يحاكي السموم البكتيرية. الخلايا التي تفتقر إلى lincRNA-EPS تحولت إلى خلايا هادمة أكثر عدوانية بسهولة أكبر وشغلت جينات وبروتينات هادمة للعظم بمستويات أعلى. تشير هذه النتائج إلى أن lincRNA-EPS يعمل عادة كمكبح لنمو ووظيفة الخلايا الهادمة للعظم تحت الضغط الالتهابي.
المعالجة الحديدية كحلقة وصل خفية
لفهم كيف يمارس هذا الـ RNA تأثيره، قارنت المجموعة نشاط الجينات ونماذج البروتين في الخلايا السلف والخلايا الهادمة الناضجة من فئران عادية ومعدلة. وجدوا ليس فقط برامج أقوى للخلايا الهادمة للعظم، بل أيضًا تغيرات لافتة في المسارات التي تتحكم في استخدام الحديد وتخزينه ونقله. برز بروتين سكري مُفرَز واحد، ليبوكانين-2 (Lcn2)، الذي يمكنه نقل الحديد داخل الخلايا وخارجها، بزيادة قوية عند فقدان lincRNA-EPS، خصوصًا بعد التحفيز الالتهابي. أظهرت اختبارات إضافية أنه في الأنسجة والخلايا المستزرعة بدون lincRNA-EPS، ظلت مستويات Lcn2 مرتفعة، وبقيت بروتينات معالجة الحديد مفعلة لفترة أطول، وظل الحديد المتحرك داخل الخلايا الهادمة مرتفعًا — كلها دلائل على اقتصاد حديد مفرط يغذي الخلايا الهادمة الطموحة للطاقة.
تعديل ناقل الحديد لتهدئة تلف العظم
ثم عبث العلماء مباشرةً بـ Lcn2 ليروا كيف يؤثر على هذا النظام. أدى تقليل Lcn2 في الخلايا السلفية الطبيعية إلى خفض آلية نقل الحديد وتغيير شكل الخلايا الهادمة للعظم، مفرزًا خلايا أصغر بعدد أنوية أقل، رغم أن أعدادها قد ترتفع. أما إضافة Lcn2 إضافي فكان له التأثير المعاكس، فساعد الخلايا على الاندماج لتشكيل وحدات أكبر وأكثر قوة قادرة على هدم العظم. في الفئران المصابة بمرض اللثة، خفض Lcn2 في الأنسجة المحيطة بالأسنان قلل فقدان العظم ونشاط الخلايا الهادمة، ولكن فقط عندما كان lincRNA-EPS موجودًا. عندما غاب lincRNA-EPS، كانت لتغييرات مستويات Lcn2 أو إضافة Lcn2 تأثيرات أضعف وأبطأ على مستويات الحديد وسلوك الخلايا الهادمة، ما يوحي بأن هذا الـ RNA مطلوب لضبط سريع ومستقر لاستقلاب الحديد أثناء الالتهاب.
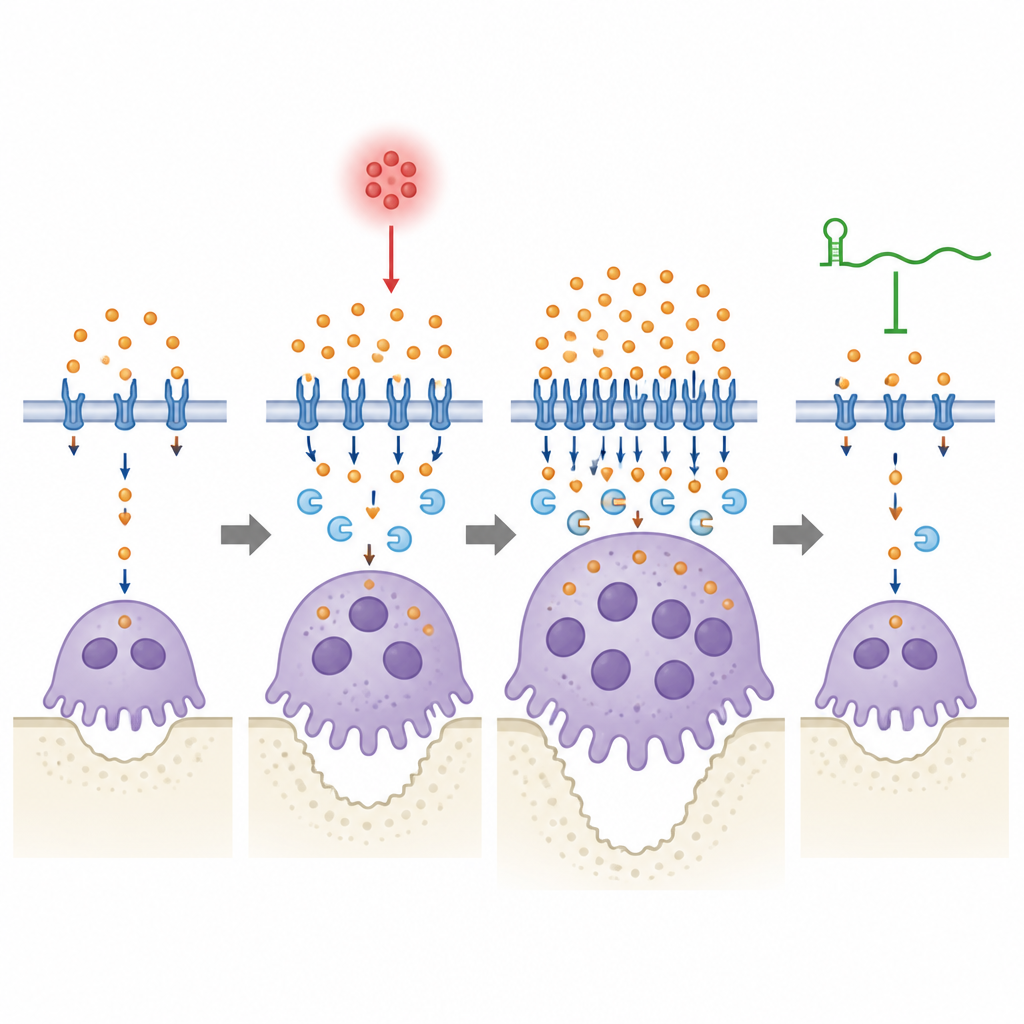
توازن دقيق بين الحديد والعظم
من منظور شعبي، تُظهر هذه الدراسة أن RNA تنظيميًا، lincRNA-EPS، يساعد عظم الفك على النجاة من عدوى اللثة عن طريق منع خلايا آكلة العظم من الإفراط في استهلاك الحديد والبقاء مفرطة النشاط لفترة أطول من اللازم. في فم ملتهب، يرتفع مستوى Lcn2 ويدفع مزيدًا من الحديد إلى الخلايا الهادمة، مما يساعدها على النمو ومضغ العظم؛ يساعد lincRNA-EPS هذه الخلايا على استشعار وتصحيح تلك الزيادة ليعود استخدام الحديد إلى مستوى آمن. عندما يختفي هذا الـ RNA، تفشل صمام الأمان هذا، يبقى التعامل مع الحديد مفرطًا، ويتفاقم فقدان العظم. على الرغم من أن الدراسة ما تزال قبل سريرية، فإنها تبرز تنظيم الحديد وزوج lincRNA-EPS–Lcn2 كأهداف محتملة لعلاجات مستقبلية تهدف إلى حماية الأسنان عن طريق إبطاء إزالة العظم بلطف بدلاً من إيقافها تمامًا.
الاستشهاد: Wang, J., Wang, Y., Zhang, Z. et al. LincRNA-EPS alleviates osteoclastogenesis under inflammatory microenvironment through preventing excessive iron metabolism. Cell Death Dis 17, 444 (2026). https://doi.org/10.1038/s41419-026-08716-y
الكلمات المفتاحية: التهاب دواعم السن, الخلايا الهادمة للعظم (osteoclasts), استقلاب الحديد, ليبوكانين-2, حمض نووي ريبوزي طويل غير مشفر