Clear Sky Science · it
Il lincRNA-EPS attenua l'osteoclastogenesi in un microambiente infiammatorio impedendo il metabolismo del ferro eccessivo
Perché è importante per gengive doloranti e denti fragili
Molti adulti convivono con gengive sanguinanti e denti mobili a causa della parodontite, un'infezione cronica che lentamente erode l'osso che sostiene i denti. Questo studio indaga quel processo e scopre come una molecola di RNA poco nota contribuisca a mantenere in equilibrio le cellule che consumano osso e l'uso del ferro, suggerendo nuove strategie per proteggere la mandibola durante la malattia gengivale.
Gli "mangiatori di osso" al lavoro nelle gengive infiammate
Nella parodontite, i batteri intorno ai denti scatenano una forte risposta immunitaria nelle gengive. Questa infiammazione attiva cellule specializzate che consumano osso, chiamate osteoclasti, che scavano solchi nell'osso mandibolare e possono portare alla perdita dei denti. Gli autori hanno usato un modello murino di malattia gengivale creato con componenti batteriche legate attorno ai denti e, confermato con scansioni 3D, hanno mostrato che l'infiammazione causa una perdita ossea evidente. Si sono concentrati su una molecola chiamata lincRNA-EPS, un RNA non codificante già noto per attenuare segnali infiammatori in altri tessuti, per verificare se frenasse anche l'attività degli osteoclasti in questo ambiente ostile.
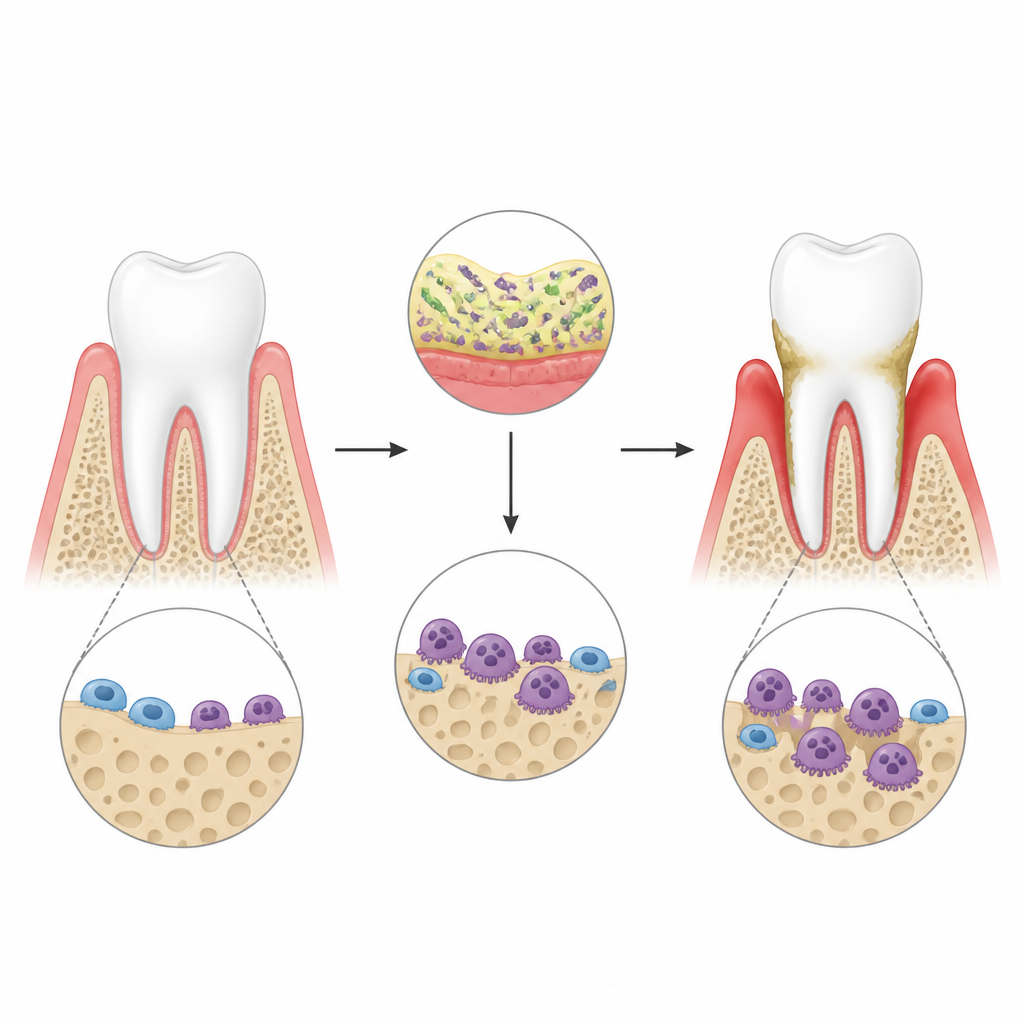
Un RNA protettivo che limita la perdita ossea
Quando i ricercatori hanno rimosso il lincRNA-EPS nei topi, la perdita ossea intorno ai denti è risultata decisamente peggiorata dopo l'infezione gengivale. La superficie della mandibola presentava osteoclasti più numerosi e più grandi, e i solchi che questi scavavano nelle sezioni ossee in laboratorio erano più profondi e larghi. in coltura cellulare, le cellule del midollo osseo di animali normali e knockout sono state prima indirizzate verso la differenziazione in osteoclasti e poi esposte a uno stimolo infiammatorio che imita le tossine batteriche. Le cellule prive di lincRNA-EPS si sono trasformate più facilmente in osteoclasti aggressivi e hanno attivato a livelli più elevati geni e proteine responsabili del riassorbimento osseo. Questi risultati suggeriscono che il lincRNA-EPS agisca normalmente come un freno sulla crescita e la funzione degli osteoclasti sotto stress infiammatorio.
La gestione del ferro come legame nascosto
Per capire come questo RNA esercitasse il suo effetto, il team ha confrontato l'attività genica e i profili proteici nei precursori e negli osteoclasti maturi di topi normali e knockout. Hanno riscontrato non solo programmi osteoclastici potenziati, ma anche cambiamenti marcati nelle vie che controllano l'uso, l'immagazzinamento e il trasporto del ferro. Una proteina secreta, la lipocalina-2 (Lcn2), che può trasportare ferro dentro e fuori dalle cellule, è emersa come fortemente aumentata in assenza di lincRNA-EPS, specialmente dopo stimolazione infiammatoria. Ulteriori test hanno mostrato che nei tessuti e nelle cellule coltivate privi di lincRNA-EPS, i livelli di Lcn2 restavano elevati, le proteine di gestione del ferro rimanevano attivate più a lungo e il ferro mobile all'interno degli osteoclasti restava alto, tutti segni di un'economia del ferro iperattiva che alimenta i voraci consumatori di osso.
Regolare un trasporto del ferro per calmare il danno osseo
Gli scienziati hanno poi manipolato direttamente Lcn2 per vedere come influenzi questo sistema. Ridurre Lcn2 nei precursori normali attenuava i meccanismi di trasporto del ferro e modificava la forma degli osteoclasti, producendo cellule più piccole con meno nuclei, anche se il loro numero poteva aumentare. Aggiungere Lcn2 in eccesso aveva l'effetto opposto, favorendo la fusione in unità più grandi e più potenti nel riassorbimento osseo. Nei topi con malattia gengivale, abbassare Lcn2 nei tessuti intorno ai denti riduceva la perdita ossea e l'attività degli osteoclasti, ma solo quando il lincRNA-EPS era presente. Quando il lincRNA-EPS mancava, cambiare i livelli di Lcn2 o aggiungere Lcn2 supplementare aveva effetti più deboli e lenti sui livelli di ferro e sul comportamento degli osteoclasti, suggerendo che questo RNA è necessario per un aggiustamento rapido e stabile del metabolismo del ferro durante l'infiammazione.
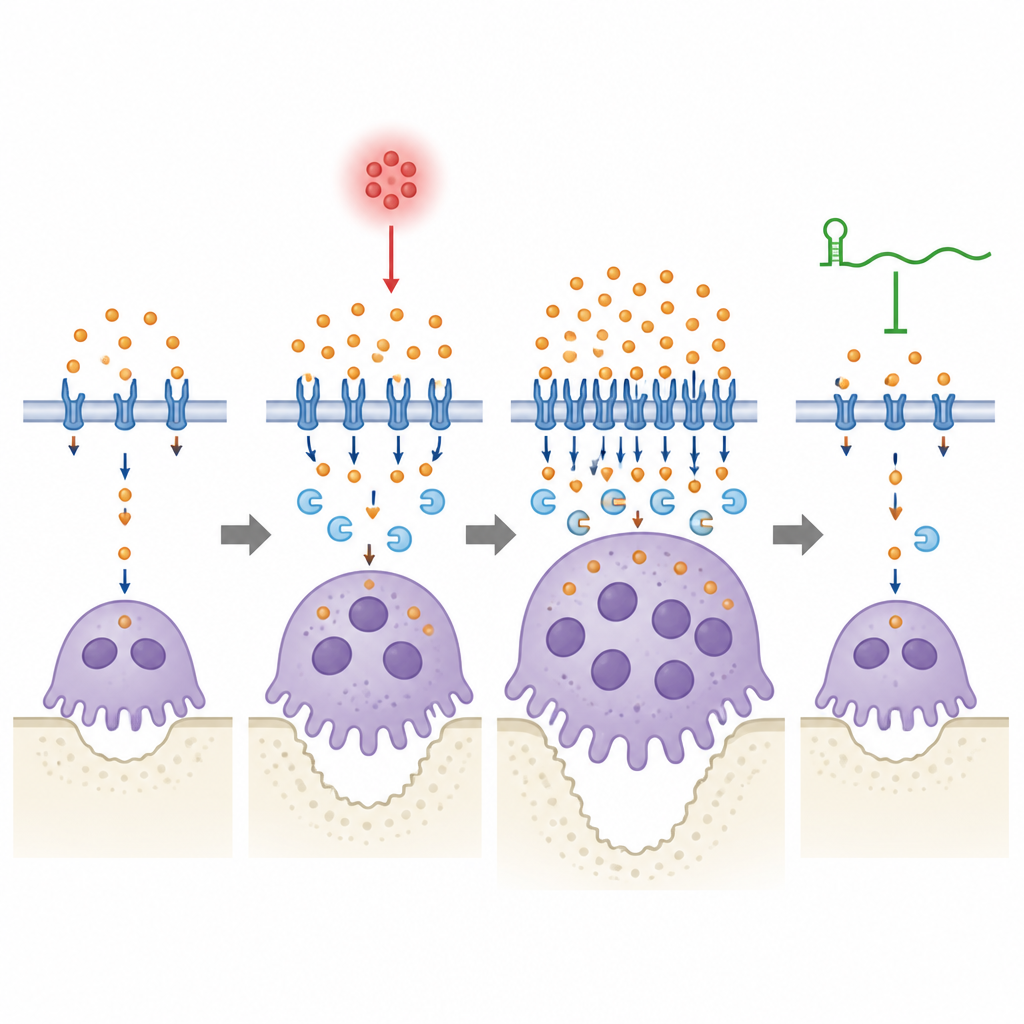
Un equilibrio finemente sintonizzato tra ferro e osso
Dal punto di vista divulgativo, questo lavoro mostra che un RNA regolatorio, il lincRNA-EPS, aiuta l'osso mandibolare a resistere all'infezione gengivale impedendo che gli osteoclasti si abbuffino di ferro e rimangano iperattivi troppo a lungo. In una bocca infiammata, Lcn2 aumenta e spinge più ferro negli osteoclasti, favorendone la crescita e la degradazione ossea; il lincRNA-EPS aiuta queste cellule a percepire e correggere quell'impennata affinché l'uso del ferro torni a livelli sicuri. Quando l'RNA manca, questa valvola di sicurezza fallisce, la gestione del ferro rimane eccessiva e la perdita ossea peggiora. Sebbene lo studio sia preclinico, mette in evidenza la regolazione del ferro e la coppia lincRNA-EPS–Lcn2 come potenziali bersagli per future terapie volte a proteggere i denti rallentando delicatamente il riassorbimento osseo anziché bloccandolo del tutto.
Citazione: Wang, J., Wang, Y., Zhang, Z. et al. LincRNA-EPS alleviates osteoclastogenesis under inflammatory microenvironment through preventing excessive iron metabolism. Cell Death Dis 17, 444 (2026). https://doi.org/10.1038/s41419-026-08716-y
Parole chiave: parodontite, osteoclasti, metabolismo del ferro, lipocalina-2, RNA lungo non codificante