Clear Sky Science · zh
LRRK2介导的cGAS‑STING/HMGB1细胞衰老促进骨关节炎软骨退化
为何磨损的关节很重要
酸痛的膝盖和僵硬的髋关节常被视为不可避免的衰老表现,但骨关节炎并非简单的“磨损”。它涉及软骨内的活细胞发生逐步变化,停止修复组织,并开始释放导致关节炎症的求救信号。本研究揭示了一个新的分子元凶,推动这些细胞进入过早衰老状态,为理解并可能减缓骨关节炎进展提供了新的视角。
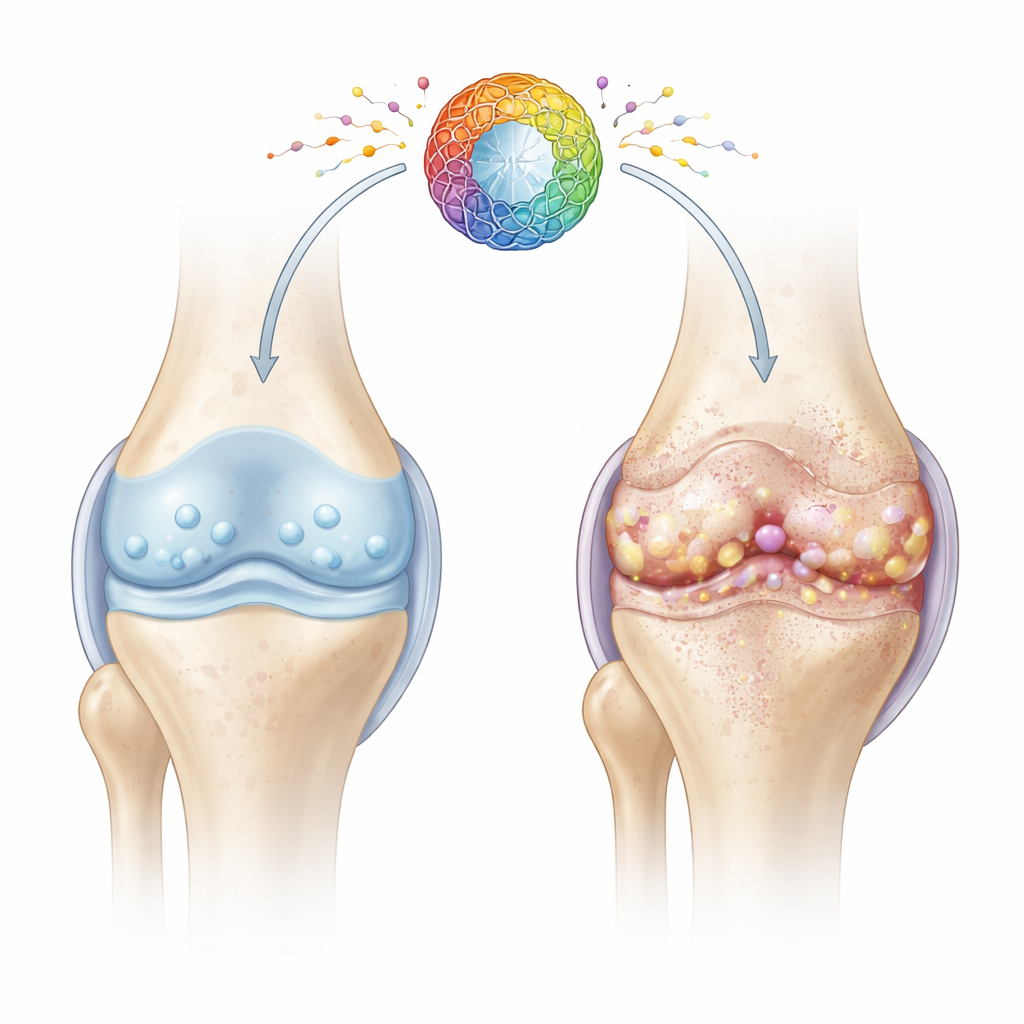
仔细观察疲惫的关节细胞
软骨是覆盖在骨端的光滑弹性组织,其健康依赖于软骨细胞——这些在几十年中默默维持基质的专门细胞。随着年龄或损伤,许多软骨细胞进入一种称为细胞衰老的状态:它们停止分裂,丧失修复能力,并释放一组炎性和破坏组织的分子。作者关注的是细胞能源工厂——线粒体出现问题如何驱动这种有害的衰老状态并加速关节退化。
一种与帕金森相关的酶出现在疼痛关节中
研究团队利用来自人类软骨的公开基因表达数据,寻找同时与骨关节炎和细胞衰老相关的基因。其中一个基因尤为突出:LRRK2,一种更为人所知的与遗传性帕金森病和炎症性疾病相关的大型酶。与健康组织相比,骨关节炎软骨中LRRK2水平明显升高。在大鼠膝关节骨关节炎模型中,关节软骨和滑膜细胞中LRRK2也呈上调。当研究者在大鼠软骨细胞中人为提高LRRK2表达时,数百个其他基因发生了变化,尤其是那些参与细胞衰老和炎性信号的基因,表明LRRK2不仅是旁观者,而且是驱动疾病过程的活跃因子。
内部警报如何将压力转化为损伤
研究进一步聚焦于细胞内的一个分子报警系统——cGAS–STING通路,该通路检测细胞质中错位的DNA——这是线粒体损伤常见的后果之一——并触发炎症。体外实验显示,过量的LRRK2与并激活该通路在软骨细胞中结合。该通路的激活又提高并改变了HMGB1的水平和行为,HMGB1通常在细胞核中帮助组织DNA,但当释放到细胞外环境时可作为强烈的危险信号。高LRRK2的软骨细胞表现出肿胀且功能异常的线粒体、更多的活性氧(有害的氧代谢产物)、能量生成减少以及明显的衰老标志。阻断STING或抑制LRRK2的活性或其GTP酶功能,可降低HMGB1水平、缓解氧化应激并减少这些细胞的衰老标志。
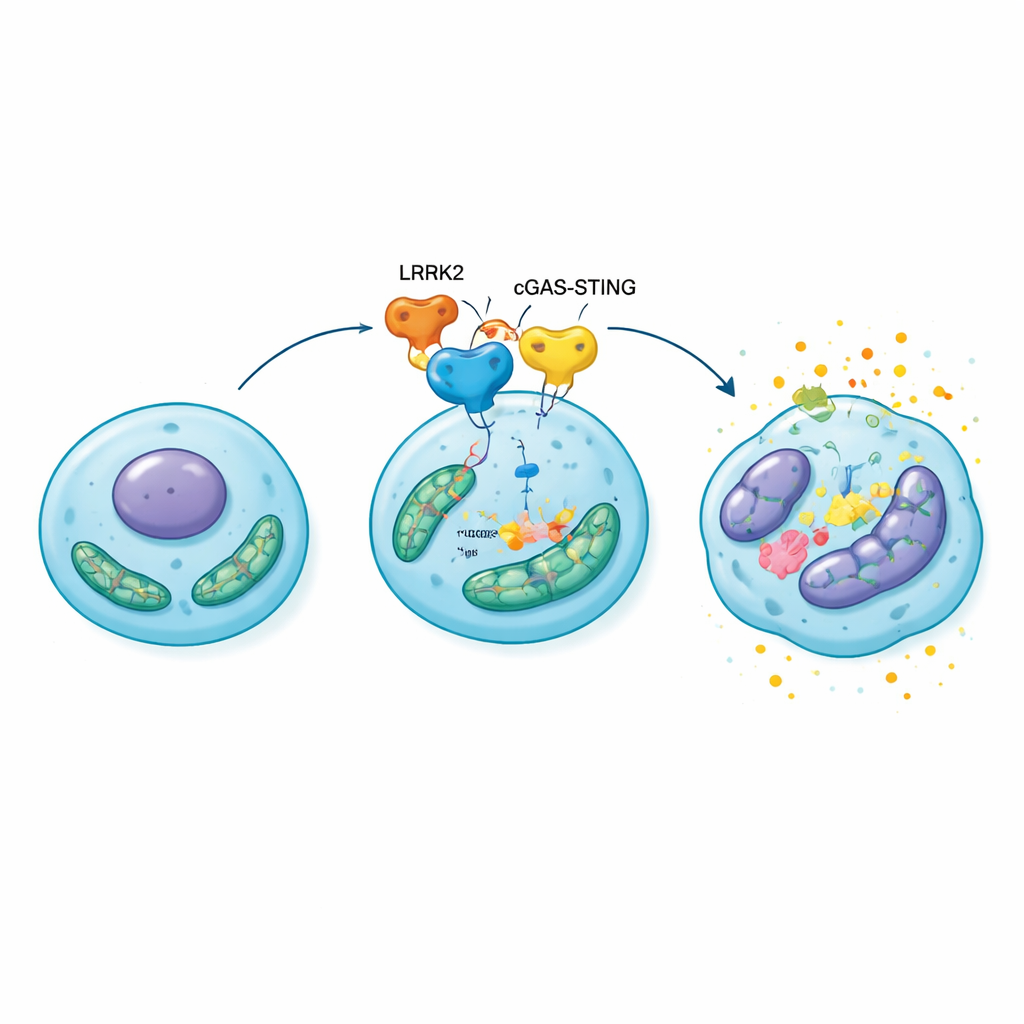
从受压细胞到崩解的软骨
为验证这一分子连锁反应对整个关节的影响,研究者在手术诱导的骨关节炎大鼠膝关节中直接过表达LRRK2。与对照动物相比,这些大鼠出现更薄、更侵蚀的软骨,关节下骨的改变更明显,且更多的软骨细胞处于衰老状态并携带炎性和基质降解分子。当同样的动物接受STING阻断药物治疗时,关节损伤和细胞衰老明显减少,线粒体功能也部分恢复。这些结果将LRRK2–cGAS–STING–HMGB1通路置于一个自我强化回路的中心:线粒体应激激活报警系统,提升HMGB1和炎症,反过来加深线粒体损伤并促使更多软骨细胞进入衰老。
这对未来关节护理意味着什么
简而言之,作者表明LRRK2如同一个故障开关,将软骨细胞锁定在衰老与疲惫状态,并加速关节组织的分解。通过开启cGAS–STING–HMGB1报警网络,高LRRK2活性将细胞内应激与慢性炎症和结构性损伤联系起来。这项工作提示,旨在降低LRRK2活性或中断cGAS–STING通路的药物,可能有助于延长软骨细胞功能时间,从而潜在地减缓骨关节炎的进展,而不仅仅是缓解症状。
引用: Zhang, Y., Zhu, Z., Ji, P. et al. cGAS-STING/HMGB1-mediated senescence induced by LRRK2 accelerates cartilage degeneration in osteoarthritis. Cell Death Dis 17, 377 (2026). https://doi.org/10.1038/s41419-026-08651-y
关键词: 骨软骨退化, 细胞衰老, 线粒体功能障碍, 炎性信号, LRRK2通路