Clear Sky Science · sv
cGAS-STING/HMGB1-medierad senescens inducerad av LRRK2 påskyndar brosknedbrytning vid artros
Varför utslitna leder spelar roll
Värkande knän och stela höfter avfärdas ofta som en oundviklig del av åldrandet, men artros är mer än enkel ”slitage”. Det handlar om levande celler i brosket som gradvis förändras, slutar reparera vävnad och börjar sända nödsignaler som orsakar inflammation i leden. Den här studien avslöjar en ny molekylär bov som bidrar till att driva dessa celler in i ett för tidigt åldrande tillstånd, vilket ger en ny ingång för att förstå — och potentiellt bromsa — artrosens utveckling.
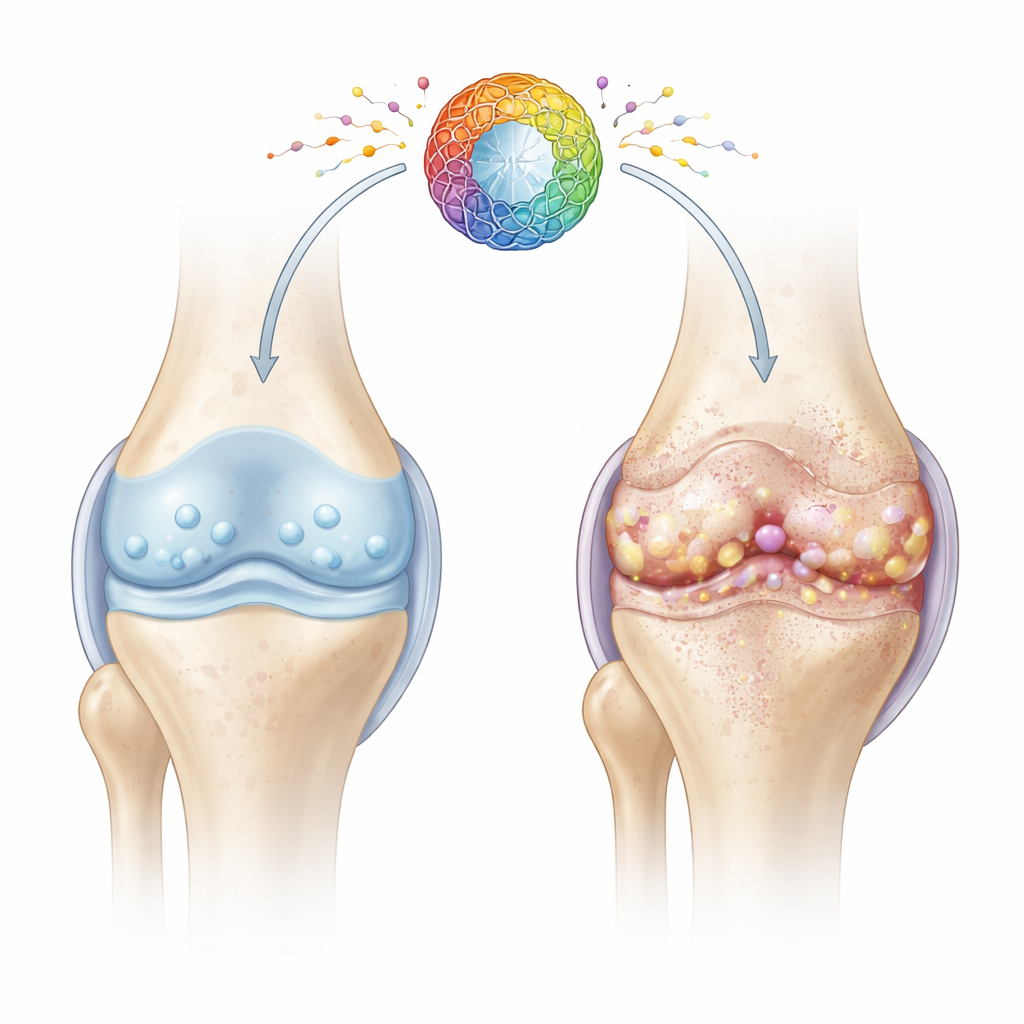
En närmare titt på utmattade ledeceller
Brosk är den släta, gummiartade vävnaden som dämpar benslut. Dess hälsa är beroende av kondrocyter, specialiserade celler som under lång tid underhåller broskets matrix. Med ålder och skada går många kondrocyter in i ett tillstånd som kallas cellulär senescens: de slutar dela sig, förlorar reparationsförmåga och frigör en blandning av inflammatoriska och vävnadsskadande molekyler. Författarna fokuserade på hur problem i cellernas energiverk — mitokondrierna — kan driva detta skadliga åldrandetillstånd och påskynda ledförfallet.
En Parkinsonkopplad enzym visar sig i ömma leder
Med hjälp av publika genuttrycksdata från mänskligt brosk sökte teamet efter gener kopplade till både artros och cellulärt åldrande. En stod ut: LRRK2, ett stort enzym bättre känt för sin roll i ärftlig Parkinsons sjukdom och inflammatoriska störningar. LRRK2-nivåerna var markant högre i artrotiskt brosk jämfört med frisk vävnad. I en råttmodell för knäartros var LRRK2 likaledes uppreglerat i ledbrosk och synovialceller. När forskarna artificiellt ökade LRRK2 i råttkondrocyter skiftade hundratals andra gener, särskilt de som är involverade i cellulärt åldrande och inflammatorisk signalering, vilket tyder på att LRRK2 inte bara är en åskådare utan en aktiv drivkraft i sjukdomsprocessen.
Hur interna larm förvandlar stress till skada
Studien zoomade därefter in på ett molekylärt larmsystem inne i cellerna kallat cGAS–STING-vägen, som upptäcker felplacerat DNA i cytoplasman — en vanlig konsekvens av mitokondrieskada — och utlöser inflammation. Laboratorieexperiment visade att överskott av LRRK2 binder till och aktiverar denna väg i kondrocyter. Aktivering ökade i sin tur nivåerna av och förändrade beteendet hos HMGB1, ett protein som normalt hjälper till att organisera DNA i cellkärnan men som kan fungera som en stark faresignal när det släpps ut i omgivningen. Kondrocyter med högt LRRK2 uppvisade svullna, felande mitokondrier, mer reaktiva syreradikaler (skadliga syreprodukter), minskad energiproduktion och tydliga kännetecken på senescens. Att blockera STING eller hämma LRRK2:s aktivitet eller dess GTPas-funktion dämpade HMGB1, lättade oxidativ stress och minskade åldersmarkörer i dessa celler.
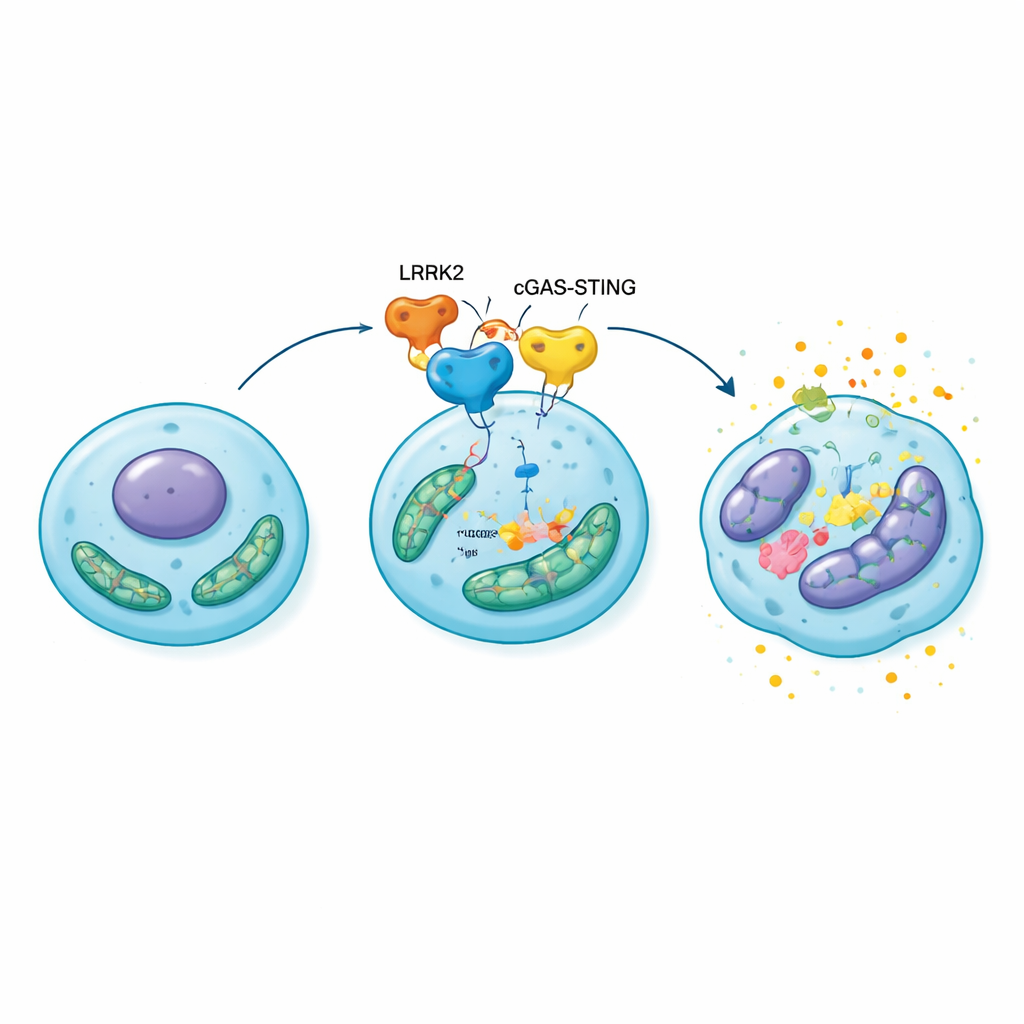
Från stressade celler till smulande brosk
För att se om denna molekylära kedjereaktion påverkade hela leder överuttryckte forskarna LRRK2 direkt i knän hos råttor med kirurgiskt inducerad artros. Jämfört med kontroll-djur utvecklade dessa råttor tunnare, mer eroderat brosk, större benförändringar under ledytan och fler senescenta kondrocyter fyllda med inflammatoriska och matrixnedbrytande molekyler. När samma råttor behandlades med ett läkemedel som blockerar STING minskade ledskadan och cellåldrandet tydligt, och mitokondriell funktion återhämtade sig delvis. Resultaten placerar LRRK2–cGAS–STING–HMGB1-axeln i centrum för en självförstärkande loop: mitokondriell stress aktiverar larmsystemet, vilket ökar HMGB1 och inflammation, vilket i sin tur fördjupar mitokondrieskadan och driver fler kondrocyter in i senescens.
Vad detta innebär för framtida ledvård
Enkelt uttryckt visar författarna att LRRK2 fungerar som en felaktig strömbrytare som låser broskceller i ett gammalt, utmattat tillstånd och påskyndar nedbrytningen av ledvävnad. Genom att slå på cGAS–STING–HMGB1-larmnätverket förenar hög LRRK2-aktivitet intern cellulär stress med kronisk inflammation och strukturell skada vid artros. Detta arbete tyder på att läkemedel som syftar till att dämpa LRRK2 eller avbryta cGAS–STING-vägen skulle kunna hjälpa till att hålla kondrocyterna funktionella längre och potentiellt sakta artrosens progression snarare än att enbart lindra symtomen.
Citering: Zhang, Y., Zhu, Z., Ji, P. et al. cGAS-STING/HMGB1-mediated senescence induced by LRRK2 accelerates cartilage degeneration in osteoarthritis. Cell Death Dis 17, 377 (2026). https://doi.org/10.1038/s41419-026-08651-y
Nyckelord: osteokondral degeneration, cellulär senescens, mitokondriell dysfunktion, inflammatorisk signalering, LRRK2-väg