Clear Sky Science · pl
Starzenie komórkowe indukowane przez LRRK2 za pośrednictwem szlaku cGAS-STING/HMGB1 przyspiesza degenerację chrząstki w chorobie zwyrodnieniowej stawów
Dlaczego zużyte stawy mają znaczenie
Bóle kolan i sztywne biodra bywają często bagatelizowane jako nieuchronna część starzenia się, ale choroba zwyrodnieniowa stawów to coś więcej niż „zużycie”. Dotyczy żywych komórek w chrząstce, które stopniowo się zmieniają, przestają naprawiać tkankę i zaczynają wysyłać sygnały alarmowe wywołujące zapalenie stawu. Badanie odkrywa nowego molekularnego sprawcę, który przyspiesza przechodzenie tych komórek w przedwcześnie postarzały stan, oferując nowe spojrzenie na zrozumienie — i potencjalne spowolnienie — postępu choroby zwyrodnieniowej stawów.
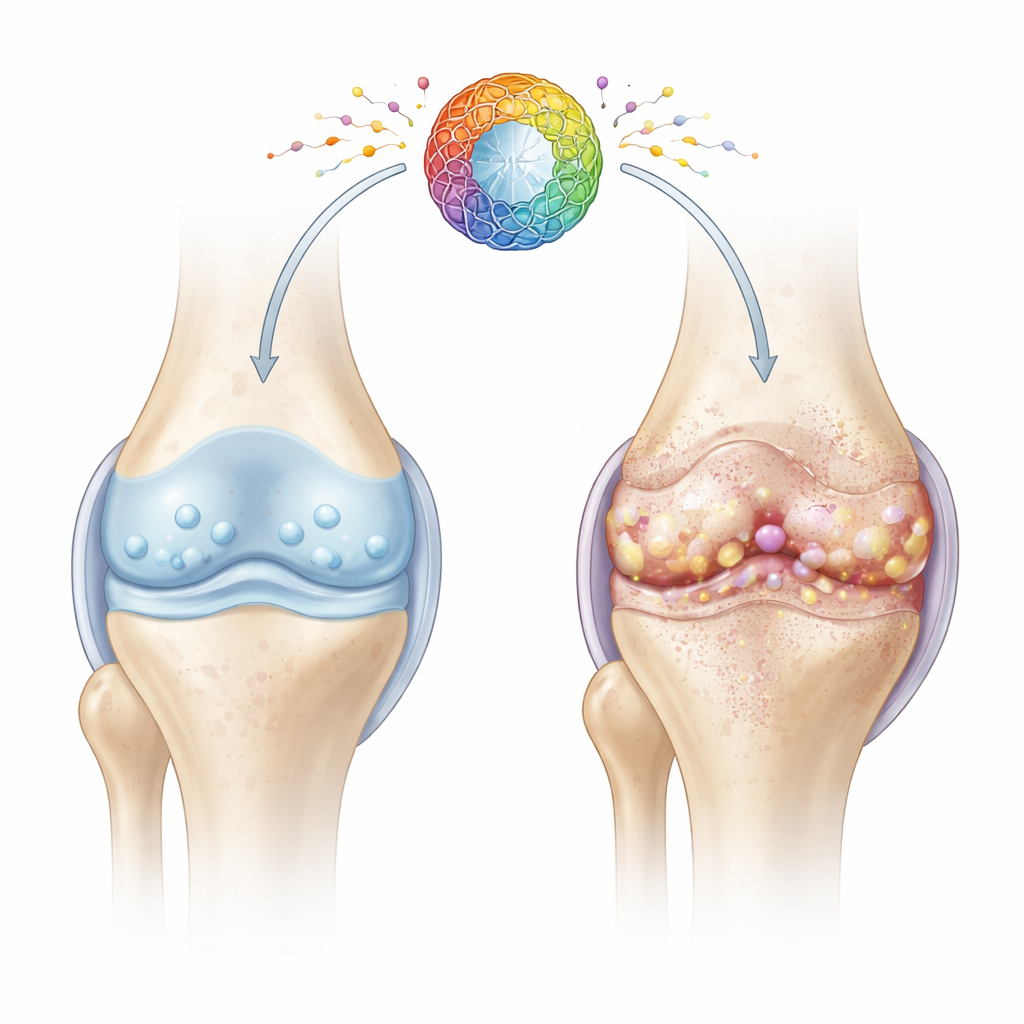
Bliższe spojrzenie na zmęczone komórki stawowe
Chrząstka to gładka, sprężysta tkanka amortyzująca końce kości. Jej zdrowie zależy od chondrocytów, wyspecjalizowanych komórek, które przez dekady utrzymują macierz chrząstki. Wraz z wiekiem i urazami wiele chondrocytów wchodzi w stan zwany starzeniem komórkowym: przestają się dzielić, tracą zdolność naprawczą i uwalniają koktajl czynników zapalnych oraz uszkadzających tkankę. Autorzy skoncentrowali się na tym, jak zaburzenia w „elektrowniach” komórkowych — mitochondriach — mogą napędzać ten szkodliwy stan starzenia i przyspieszać degenerację stawu.
Enzym związany z chorobą Parkinsona pojawia się w bolących stawach
Korzystając z publicznych danych o ekspresji genów w ludzkiej chrząstce, zespół poszukiwał genów powiązanych zarówno z chorobą zwyrodnieniową stawów, jak i ze starzeniem komórkowym. Jeden gen wyraźnie się wyróżniał: LRRK2, duży enzym lepiej znany z roli w dziedzicznej postaci choroby Parkinsona i zaburzeniach zapalnych. Poziomy LRRK2 były znacznie wyższe w chrząstce dotkniętej chorobą zwyrodnieniową w porównaniu ze zdrową tkanką. W modelu szczura z chorobą zwyrodnieniową kolana LRRK2 był podobnie podwyższony w chrząstce i wyściółce stawu. Gdy badacze sztucznie zwiększyli ekspresję LRRK2 w chondrocytach szczura, zmieniła się ekspresja setek innych genów, szczególnie tych związanych ze starzeniem komórek i sygnalizacją zapalną, co sugeruje, że LRRK2 nie jest tylko przypadkowym obserwatorem, lecz aktywnym czynnikiem napędzającym proces chorobowy.
Jak wewnętrzne alarmy zmieniają stres w uszkodzenie
Badanie przyjrzało się następnie molekularnemu systemowi alarmowemu wewnątrz komórek — szlakowi cGAS–STING, który wyczuwa przemieszczenie DNA w cytoplazmie — częsty skutek uszkodzeń mitochondriów — i uruchamia odpowiedź zapalną. Eksperymenty laboratoryjne wykazały, że nadmiar LRRK2 wiąże się z tym szlakiem i go aktywuje w chondrocytach. Aktywacja zwiększała poziomy i zmieniała zachowanie HMGB1, białka, które zwykle porządkuje DNA w jądrze, ale po uwolnieniu do otoczenia komórki działa jako silny sygnał niebezpieczeństwa. Chondrocyty z wysokim LRRK2 miały spuchnięte, dysfunkcyjne mitochondria, więcej reaktywnych form tlenu (szkodliwych produktów ubocznych utleniania), zmniejszoną produkcję energii i wyraźne cechy starzenia. Blokowanie STING, hamowanie aktywności LRRK2 lub jego funkcji GTPazy osłabiało HMGB1, łagodziło stres oksydacyjny i zmniejszało markery starzenia w tych komórkach.
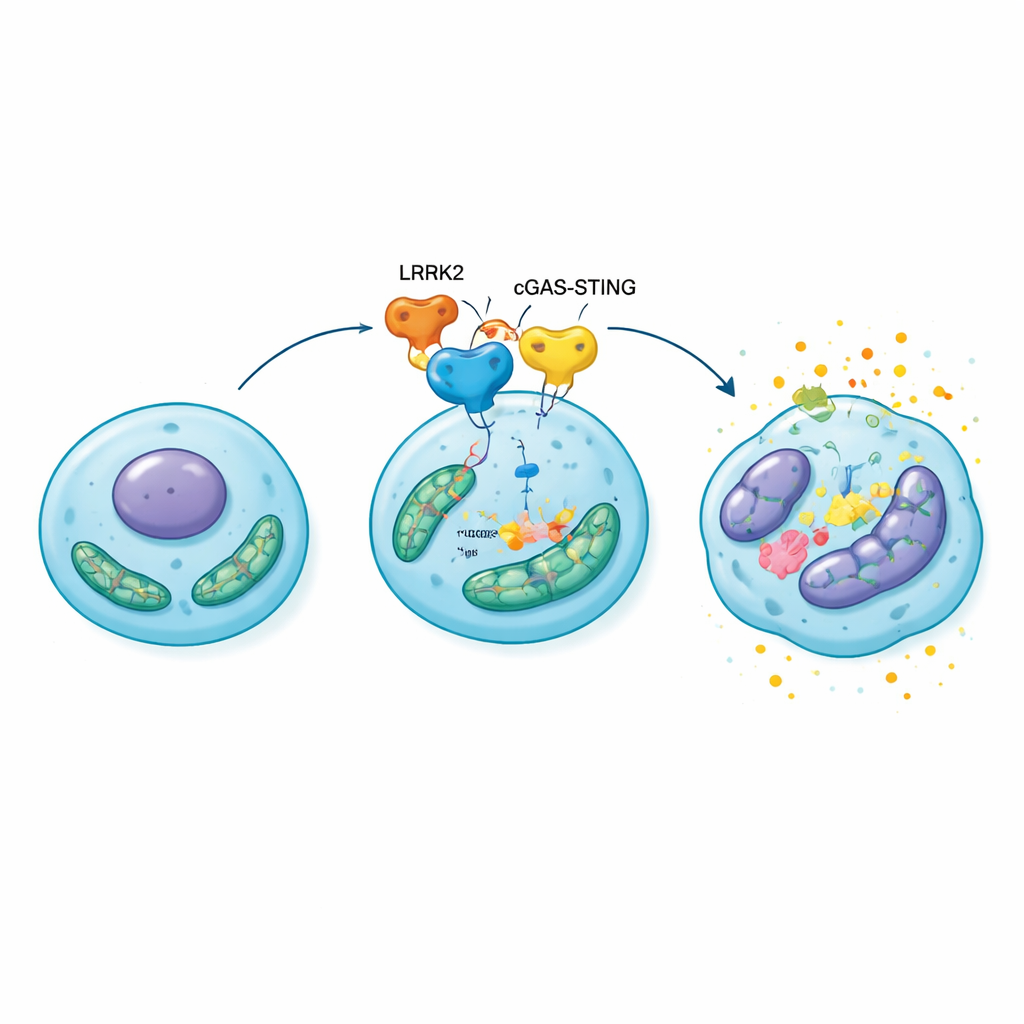
Od zestresowanych komórek do rozpadającej się chrząstki
Aby sprawdzić, czy ta molekularna kaskada ma znaczenie dla całych stawów, badacze przeszczepili nadmierną ekspresję LRRK2 bezpośrednio do kolan szczurów z chirurgicznie wywołaną chorobą zwyrodnieniową. W porównaniu z kontrolą zwierzęta te rozwijały cieńszą, bardziej erodowaną chrząstkę, większe zmiany kostne pod powierzchnią stawu oraz więcej senescentnych chondrocytów pełnych czynników zapalnych i enzymów degradujących macierz. Gdy tym samym zwierzętom podano lek blokujący STING, uszkodzenie stawu i starzenie komórek były wyraźnie ograniczone, a funkcja mitochondriów częściowo się poprawiła. Wyniki te umieszczają szlak LRRK2–cGAS–STING–HMGB1 w centrum samonapędzającej się pętli: stres mitochondrialny aktywuje system alarmowy, co zwiększa HMGB1 i stan zapalny, co z kolei pogłębia uszkodzenie mitochondriów i popycha kolejne chondrocyty w kierunku starzenia.
Co to oznacza dla przyszłej opieki nad stawami
Mówiąc prosto, autorzy pokazują, że LRRK2 działa jak wadliwy przełącznik, który blokuje komórki chrząstki w stare, wyczerpane stanie i przyspiesza rozpad tkanki stawowej. Przez uruchomienie sieci alarmowej cGAS–STING–HMGB1 wysoka aktywność LRRK2 łączy wewnętrzny stres komórkowy z przewlekłym zapaleniem i uszkodzeniem strukturalnym w chorobie zwyrodnieniowej stawów. Praca sugeruje, że leki mające na celu obniżenie aktywności LRRK2 lub przerwanie szlaku cGAS–STING mogłyby pomóc utrzymać funkcję chondrocytów na dłużej, potencjalnie spowalniając postęp choroby zamiast jedynie łagodzić jej objawy.
Cytowanie: Zhang, Y., Zhu, Z., Ji, P. et al. cGAS-STING/HMGB1-mediated senescence induced by LRRK2 accelerates cartilage degeneration in osteoarthritis. Cell Death Dis 17, 377 (2026). https://doi.org/10.1038/s41419-026-08651-y
Słowa kluczowe: degeneracja osteochondralna, starzenie komórkowe, dysfunkcja mitochondriów, sygnalizacja zapalna, szlak LRRK2