Clear Sky Science · fr
La sénescence médiée par cGAS-STING/HMGB1 induite par LRRK2 accélère la dégénérescence du cartilage dans l’arthrose
Pourquoi les articulations usées importent
Les genoux douloureux et les hanches raides sont souvent considérés comme une conséquence inévitable du vieillissement, mais l’arthrose dépasse le simple « usage ». Elle implique des cellules vivantes du cartilage qui se modifient progressivement, cessent de réparer les tissus et émettent des signaux de détresse qui enflamment l’articulation. Cette étude met en lumière un nouveau coupable moléculaire qui favorise l’entrée de ces cellules dans un état de vieillissement prématuré, offrant une perspective nouvelle pour comprendre — et potentiellement ralentir — la progression de l’arthrose.
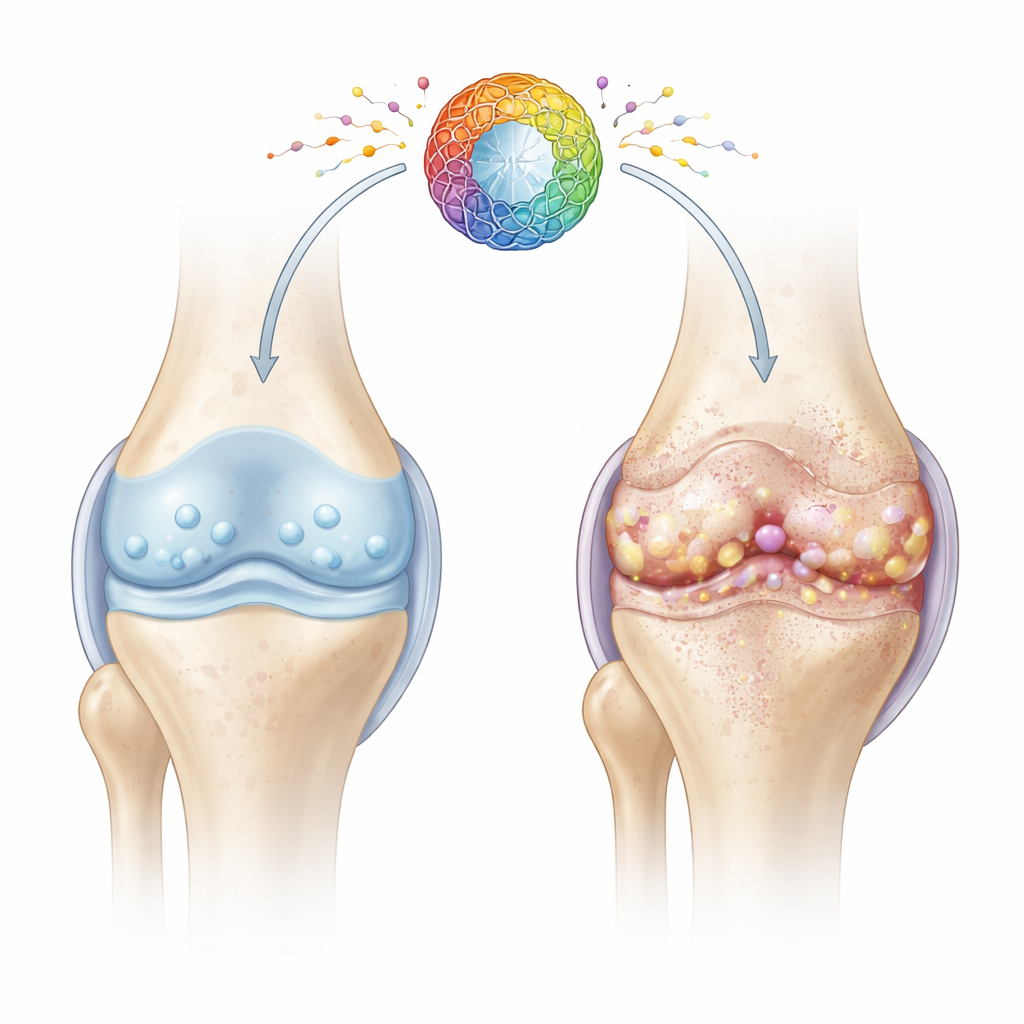
Un examen des cellules articulaires fatiguées
Le cartilage est le tissu lisse et élastique qui amortit les extrémités des os. Sa santé dépend des chondrocytes, cellules spécialisées qui maintiennent silencieusement la matrice cartilagineuse pendant des décennies. Avec l’âge et après une blessure, de nombreux chondrocytes entrent dans un état appelé sénescence cellulaire : ils cessent de se diviser, perdent leur capacité de réparation et libèrent un cocktail de molécules inflammatoires et délétères pour les tissus. Les auteurs se sont intéressés à la manière dont des dysfonctionnements des centrales énergétiques cellulaires — les mitochondries — pourraient entraîner cet état de vieillissement nuisible et accélérer la dégénérescence articulaire.
Une enzyme liée à Parkinson apparaît dans les articulations endolories
En utilisant des données publiques d’expression génique issues de cartilage humain, l’équipe a recherché des gènes associés à la fois à l’arthrose et au vieillissement cellulaire. Un gène a émergé : LRRK2, une grande enzyme mieux connue pour son rôle dans la maladie de Parkinson héréditaire et dans des troubles inflammatoires. Les niveaux de LRRK2 étaient nettement plus élevés dans le cartilage arthrosique que dans le tissu sain. Dans un modèle de rat d’arthrose du genou, LRRK2 était également augmenté dans le cartilage et la membrane synoviale. Lorsque les chercheurs ont surexprimé artificiellement LRRK2 dans des chondrocytes de rat, des centaines d’autres gènes ont été modifiés, en particulier ceux impliqués dans le vieillissement cellulaire et la signalisation inflammatoire, ce qui suggère que LRRK2 n’est pas un simple spectateur mais un moteur actif du processus pathologique.
Comment les alertes internes transforment le stress en dommage
L’étude s’est ensuite concentrée sur un système d’alarme moléculaire intracellulaire appelé voie cGAS–STING, qui détecte de l’ADN déplacé dans le cytosol — une conséquence fréquente des lésions mitochondriales — et déclenche l’inflammation. Des expériences en laboratoire ont montré qu’un excès de LRRK2 se lie à cette voie et l’active dans les chondrocytes. Cette activation augmentait et modifiait le comportement de HMGB1, une protéine qui aide normalement à organiser l’ADN dans le noyau mais qui peut agir comme un puissant signal de danger lorsqu’elle est libérée autour de la cellule. Les chondrocytes surexprimant LRRK2 présentaient des mitochondries gonflées et dysfonctionnelles, davantage d’espèces réactives de l’oxygène (sous-produits oxydants délétères), une production d’énergie réduite et des signes clairs de sénescence. Bloquer STING, ou inhiber l’activité de LRRK2 ou sa fonction GTPase, atténuait HMGB1, réduisait le stress oxydatif et diminuait les marqueurs de vieillissement dans ces cellules.
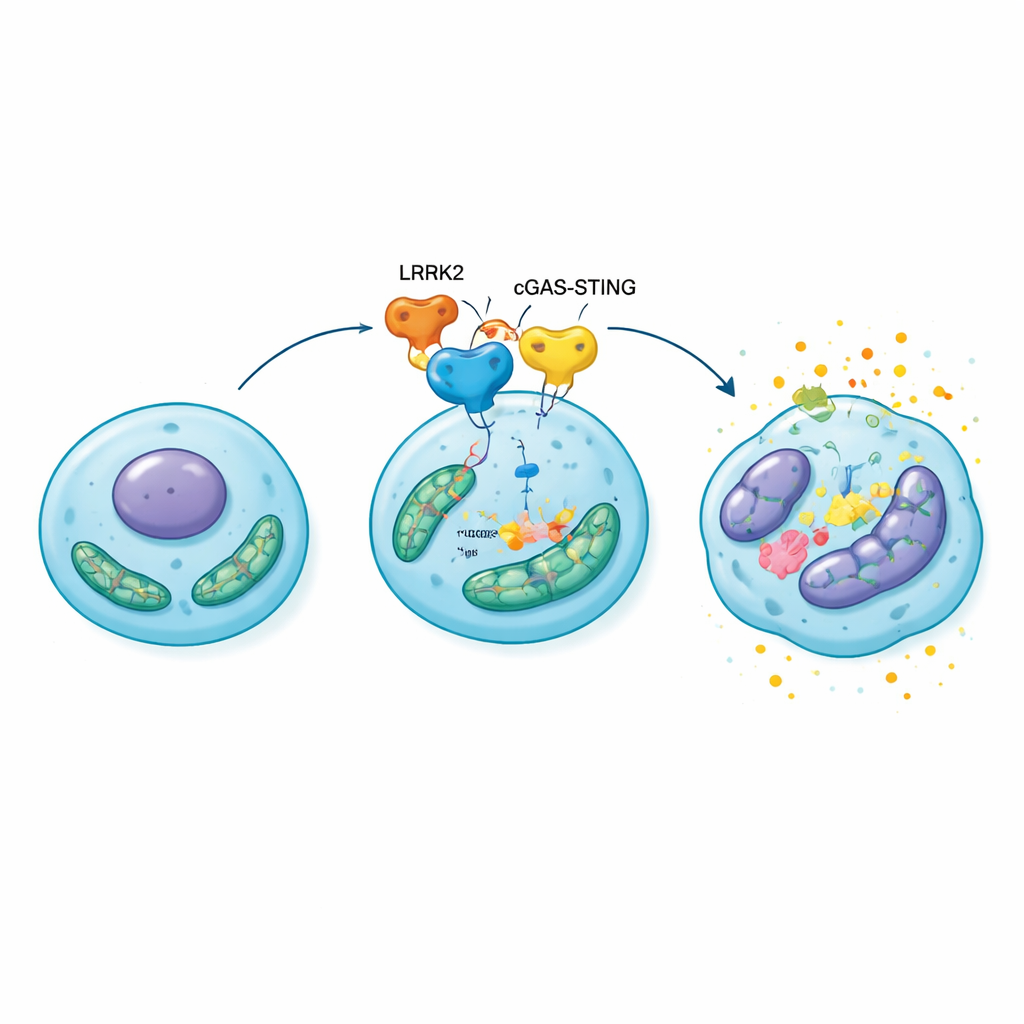
Des cellules stressées au cartilage qui s’effrite
Pour évaluer si cette chaîne moléculaire avait un impact sur l’articulation entière, les chercheurs ont surexprimé LRRK2 directement dans les genoux de rats porteurs d’une arthrose chirurgicalement induite. Par rapport aux animaux témoins, ces rats ont développé un cartilage plus mince et plus érodé, des modifications osseuses accrues sous la surface articulaire et davantage de chondrocytes sénescents chargés de molécules inflammatoires et dégradant la matrice. Lorsque les mêmes rats ont été traités par un médicament bloquant STING, les lésions articulaires et la sénescence cellulaire ont été sensiblement réduites, et la fonction mitochondriale s’est partiellement rétablie. Ces résultats placent la voie LRRK2–cGAS–STING–HMGB1 au centre d’une boucle autorenforçante : le stress mitochondrial active le système d’alarme, qui augmente HMGB1 et l’inflammation, ce qui aggrave à son tour les lésions mitochondriales et pousse davantage de chondrocytes vers la sénescence.
Ce que cela signifie pour les soins articulaires futurs
Concrètement, les auteurs montrent que LRRK2 agit comme un interrupteur défaillant qui enferme les cellules cartilagineuses dans un état vieux et épuisé et accélère la dégradation du tissu articulaire. En activant le réseau d’alarme cGAS–STING–HMGB1, une activité élevée de LRRK2 relie le stress intracellulaire à l’inflammation chronique et aux lésions structurelles de l’arthrose. Ce travail suggère que des médicaments visant à diminuer LRRK2 ou à interrompre la voie cGAS–STING pourraient aider à maintenir les chondrocytes fonctionnels plus longtemps, ralentissant potentiellement la progression de l’arthrose plutôt que de se limiter à en soulager les symptômes.
Citation: Zhang, Y., Zhu, Z., Ji, P. et al. cGAS-STING/HMGB1-mediated senescence induced by LRRK2 accelerates cartilage degeneration in osteoarthritis. Cell Death Dis 17, 377 (2026). https://doi.org/10.1038/s41419-026-08651-y
Mots-clés: dégénérescence ostéochondrale, sénescence cellulaire, dysfonction mitochondriale, signalisation inflammatoire, voie LRRK2