Clear Sky Science · nl
cGAS-STING/HMGB1-gemedieerde senescentie geïnduceerd door LRRK2 versnelt kraakbeenafbraak bij artrose
Waarom versleten gewrichten ertoe doen
Pijnlijke knieën en stijve heupen worden vaak afgedaan als onvermijdelijke kenmerken van ouder worden, maar artrose is meer dan simpele "slijtage." Het betreft levende cellen in het kraakbeen die geleidelijk veranderen, stoppen met het herstellen van weefsel en distresssignalen uitsturen die het gewricht ontsteken. Deze studie onthult een nieuwe moleculaire boosdoener die helpt deze cellen voortijdig in een verouderde staat te duwen, en biedt een nieuw perspectief om de progressie van artrose te begrijpen — en mogelijk te vertragen.
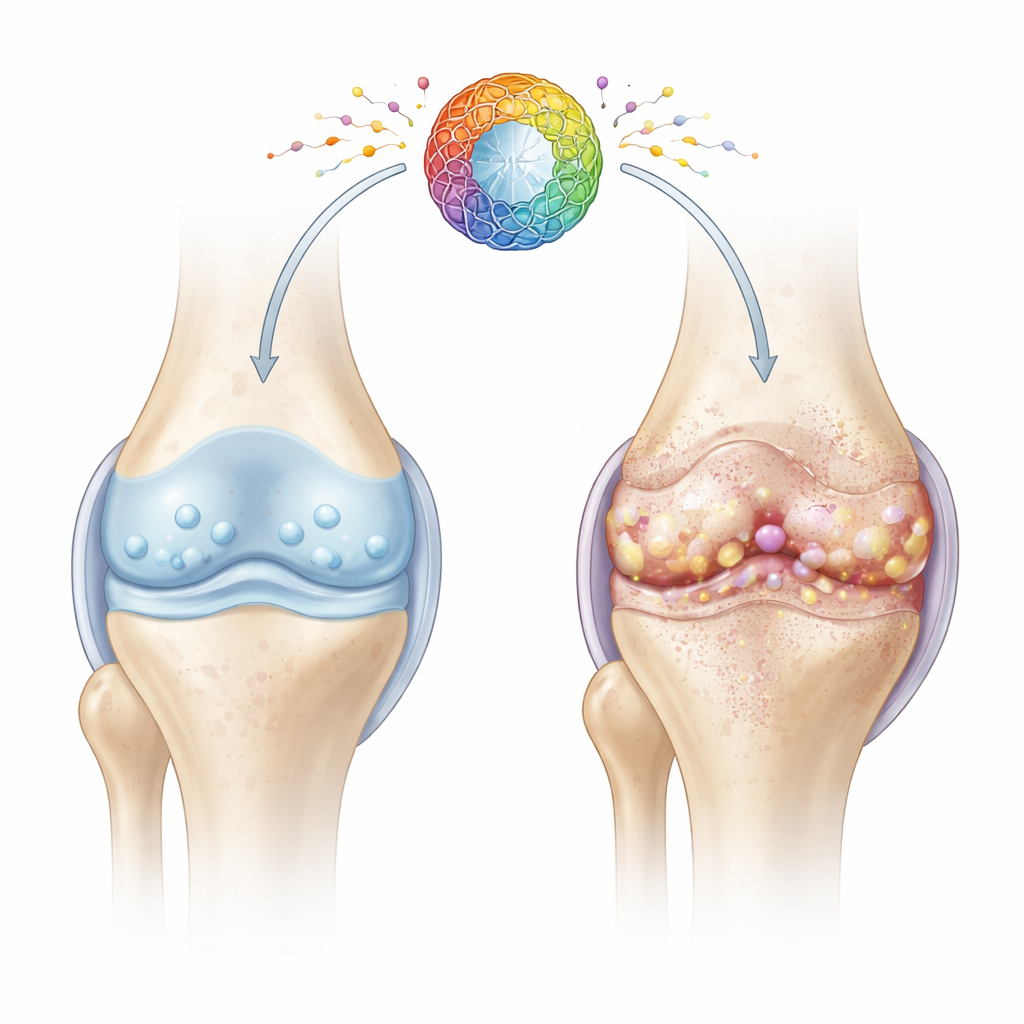
Een nadere blik op uitgeputte gewrichtscellen
Kraakbeen is het gladde, veerkrachtige weefsel dat de uiteinden van botten dempt. De gezondheid ervan hangt af van chondrocyten, gespecialiseerde cellen die decennialang stilletjes de kraakbeenmatrix onderhouden. Met leeftijd en letsel komen veel chondrocyten in een toestand die cellulaire senescentie wordt genoemd: ze stoppen met delen, verliezen hun herstelcapaciteit en scheiden een cocktail uit van ontstekingsbevorderende en weefselbeschadigende moleculen. De auteurs richtten zich op hoe problemen in de energiecentrales van de cellen — mitochondriën — deze schadelijke verouderingstoestand kunnen aansturen en de gewrichtsdegeneratie kunnen versnellen.
Een met Parkinson geassocieerd enzym duikt op in pijnlijke gewrichten
Aan de hand van openbare genexpressiegegevens uit menselijk kraakbeen zocht het team naar genen die zowel met artrose als met cellulaire veroudering verbonden zijn. Eén gen stak eruit: LRRK2, een groot enzym dat beter bekend is vanwege zijn rol bij erfelijke ziekte van Parkinson en ontstekingsstoornissen. De LRRK2-niveaus waren duidelijk hoger in artrotisch kraakbeen vergeleken met gezond weefsel. In een rattenmodel van knieartrose was LRRK2 vergelijkbaar verhoogd in gewrichtskraakbeen en bekledingscellen. Toen de onderzoekers LRRK2 kunstmatig verhoogden in rattenchondrocyten, verschoof de expressie van honderden andere genen, vooral die betrokken bij celveroudering en inflammatoire signalering, wat erop wijst dat LRRK2 geen bijstander is maar een actieve aanjager van het ziekteproces.
Hoe interne alarmen stress omzetten in schade
De studie zoomde vervolgens in op een moleculair alarmsysteem in cellen, het cGAS–STING-pad, dat verkeerd geplaatste DNA-fragmenten in het celvocht detecteert — een veelvoorkomend gevolg van mitochondriale schade — en ontsteking activeert. Laboratoriumexperimenten lieten zien dat overtollig LRRK2 zich bindt aan en dit pad activeert in chondrocyten. Activatie verhoogde op zijn beurt de niveaus en veranderde het gedrag van HMGB1, een eiwit dat normaal helpt DNA in de kern te organiseren maar dat, wanneer het in de omgeving van de cel vrijkomt, als krachtig alarmsignaal kan fungeren. Chondrocyten met hoge LRRK2 vertoonden opgezwollen, slecht functionerende mitochondriën, meer reactieve zuurstofsoorten (schadelijke zuurstofbijproducten), verminderde energieproductie en duidelijke kenmerken van senescentie. Het blokkeren van STING, of het remmen van LRRK2-activiteit of diens GTPase-functie, dempte HMGB1, verminderde oxidatieve stress en verlaagde verouderingsmarkers in deze cellen.
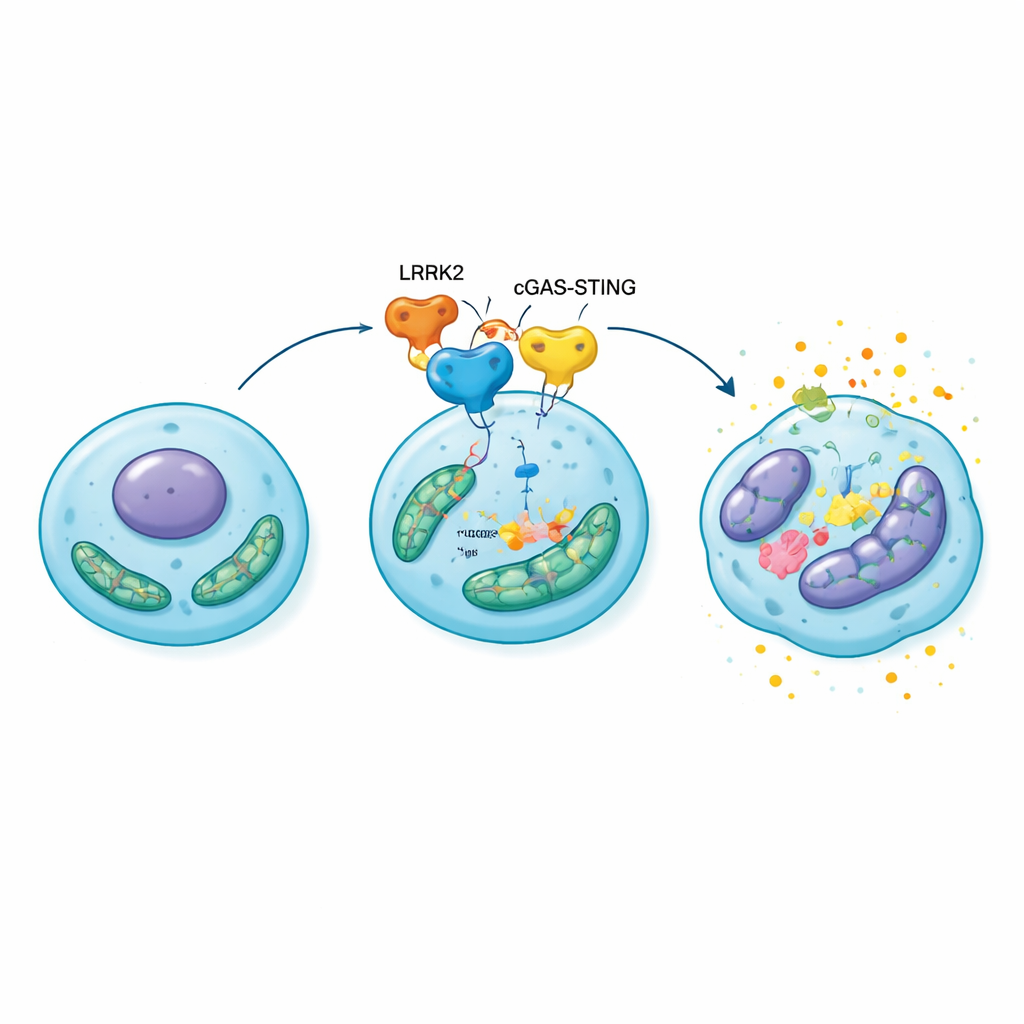
Van gestreste cellen naar afbrokkelend kraakbeen
Om te onderzoeken of deze moleculaire kettingreactie van belang is voor hele gewrichten, overexprimeerden de onderzoekers LRRK2 direct in de knieën van ratten met chirurgisch geïnduceerde artrose. In vergelijking met controledieren ontwikkelden deze ratten dunner, meer geërodeerd kraakbeen, grotere botveranderingen onder het gewrichtsoppervlak en meer senescente chondrocyten vol ontstekings- en matrix afbrekende moleculen. Toen dezelfde ratten werden behandeld met een STING-blokkerende stof, namen gewrichtsschade en celveroudering merkbaar af en herstelde de mitochondriale functie gedeeltelijk. Deze resultaten plaatsen de LRRK2–cGAS–STING–HMGB1-route in het centrum van een zichzelf versterkende lus: mitochondriale stress activeert het alarmsysteem, dat HMGB1 en ontsteking verhoogt, wat op zijn beurt mitochondriale schade verdiept en meer chondrocyten in senescentie duwt.
Wat dit betekent voor toekomstige zorg voor gewrichten
In eenvoudige bewoordingen tonen de auteurs aan dat LRRK2 fungeert als een defecte schakelaar die kraakbeencellen vastzet in een oude, uitgeputte staat en de afbraak van gewrichtsweefsel versnelt. Door het cGAS–STING–HMGB1-alarmnetwerk in te schakelen, koppelt hoge LRRK2-activiteit interne cellulaire stress aan chronische ontsteking en structurele schade bij artrose. Dit werk suggereert dat geneesmiddelen gericht op het verlagen van LRRK2 of het onderbreken van het cGAS–STING-pad kunnen helpen chondrocyten langer functioneel te houden en mogelijk de progressie van artrose te vertragen in plaats van alleen de symptomen te verlichten.
Bronvermelding: Zhang, Y., Zhu, Z., Ji, P. et al. cGAS-STING/HMGB1-mediated senescence induced by LRRK2 accelerates cartilage degeneration in osteoarthritis. Cell Death Dis 17, 377 (2026). https://doi.org/10.1038/s41419-026-08651-y
Trefwoorden: osteochondrale degeneratie, cellulaire senescentie, mitochondriale dysfunctie, inflammatoire signalering, LRRK2-route