Clear Sky Science · he
הזדקנות תאית מתווכת cGAS-STING/HMGB1 המושרת על ידי LRRK2 מאיצה את שיתוק הסחוס בדלקת מפרקים ניוונית
מדוע מפרקים שחוקים חשובים
ברכיים כואבות ומותנים נוקשים נוטים להיתפס כחלק בלתי נמנע מהזדקנות, אבל דלקת מפרקים ניוונית היא יותר מ"בלאי" פשוט. המעורבים בזה הם תאים חיים בתוך הסחוס שמשתנים בהדרגה, מפסיקים לתקן רקמות ומתחילים לשדר אותות מצוקה שמגרים את המפרק. המחקר הזה חושף גורם מולקולרי חדש שמזרז את כניסת התאים למצב הזדקנות מוקדמת, ומעניק זווית חדשה להבנת — ואולי להאטת — התקדמות הדלקת המפרקית.
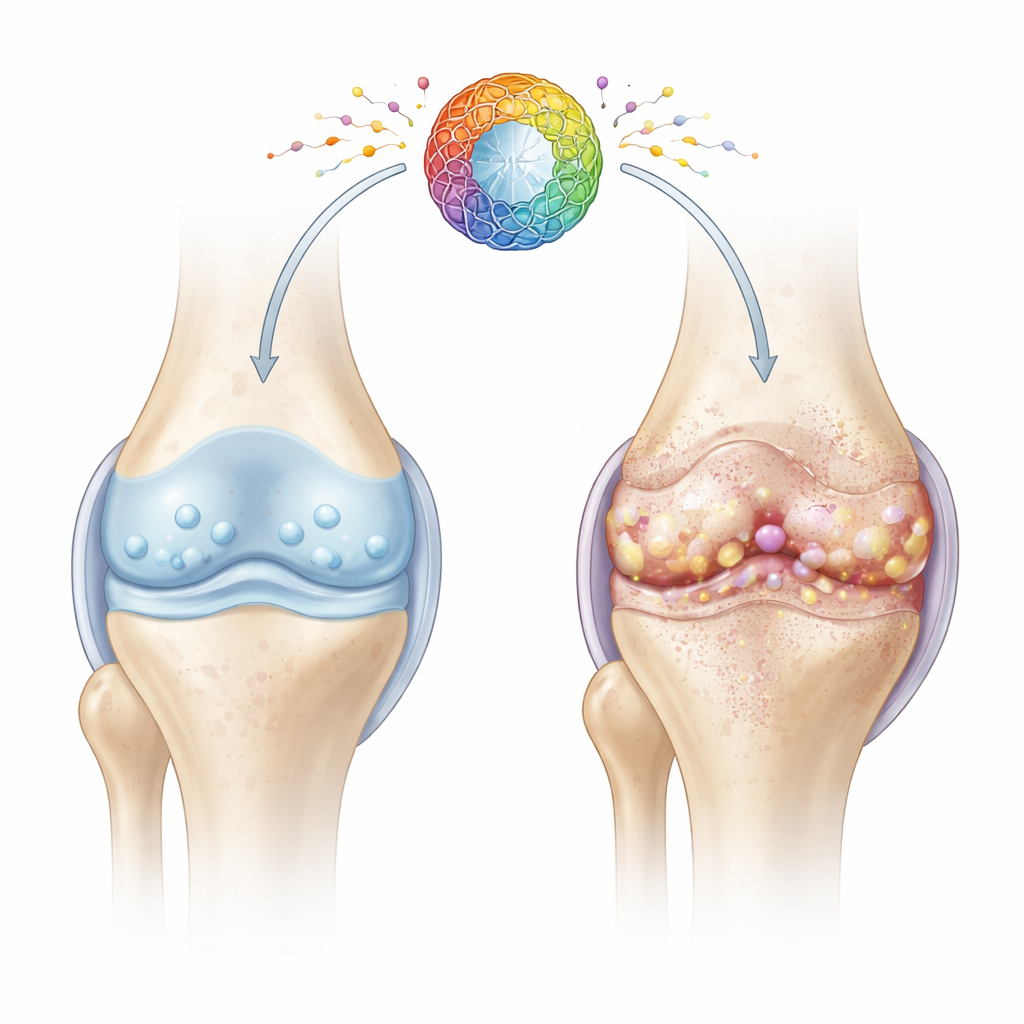
מבט קרוב יותר על תאי מפרק עייפים
הסחוס הוא רקמה חלקה וגמישה שמרפדת את קצות העצמות. בריאותו תלויה בתאי כונדרוציטים, תאים מיוחדים שמתחזקים את מטריקס הסחוס במשך עשרות שנים. עם הגיל ועם פגיעה, רבים מהכונדרוציטים נכנסים למצב שנקרא הזדקנות תאית: הם מפסיקים להתחלק, מאבדים את יכולת התיקון ומשחררים תערובת של מולקולות דלקתיות והרסניות לרקמה. הכותבים התמקדו באופן שבו ליקויים במפעלי האנרגיה של התא — המיטוכונדריה — עשויים להניע את מצב ההזדקנות המזיק הזה ולהאיץ את דגרדציית המפרק.
אנזים מקושר לפרקינסון מופיע במפרקים כואבים
בהסתכלות על נתוני הבעת גנים ציבוריים מרקמת סחוס אנושית, הצוות חיפש גנים המקושרים גם לדלקת מפרקים ניוונית וגם להזדקנות תאית. אחד בלט: LRRK2, אנזים גדול המוכר בעיקר מתפקידו במחלת פרקינסון תורשתית וממחלות דלקתיות. רמות LRRK2 היו גבוהות באופן מובהק בסחוס ניווני לעומת רקמה בריאה. במודל חולדה של דלקת מפרקים ברך ה-LRRK2 אף הוא היה מוגבר בתאי הסחוס ושכבת הריפוד של המפרק. כשחוקרים הגבירו באופן מלאכותי את ביטוי LRRK2 בכונדרוציטים של חולדות, מאות גנים אחרים השתנו, במיוחד אלו המעורבים בהזדקנות ובאיתות דלקתי, מה שמרמז ש-LRRK2 אינו רק עד, אלא מניע פעיל בתהליך המחלה.
איך אזעקות פנימיות הופכות מתח לנזק
המחקר כיוון את מבטו למערכת אזעקה מולקולרית בתוך התאים שנקראת נתיב cGAS–STING, אשר מזהה DNA שאינו במקום — לעתים קרובות תוצאה של נזק מיטוכונדריאלי — ומפעילה תגובה דלקתית. ניסויים במעבדה הראו ש-LRRK2 עודף נקשר ומפעיל את הנתיב הזה בכונדרוציטים. ההפעלה העלתה את הרמות ושינתה את ההתנהגות של HMGB1, חלבון שבדרך כלל מסדר את ה-DNA בגרעין אך יכול לשמש כאות סכנה חזק כשהוא משתחרר לסביבה התאית. בכונדרוציטים בעלי ביטוי־יתר של LRRK2 נצפו מיטוכונדריות נפוחות ופגומות, רמות גבוהות יותר של רדיקלים חופשיים של חמצן (תוצרי לוואי מזיקים של חמצון), הפחתת ייצור אנרגיה וסימני הזדקנות ברורים. חסימת STING, או עיכוב פעילות LRRK2 או תפקוד ה-GTPase שלו, הקטינה את HMGB1, הקלה על לחץ חמצוני והפחיתה סמני הזדקנות בתאים אלה.
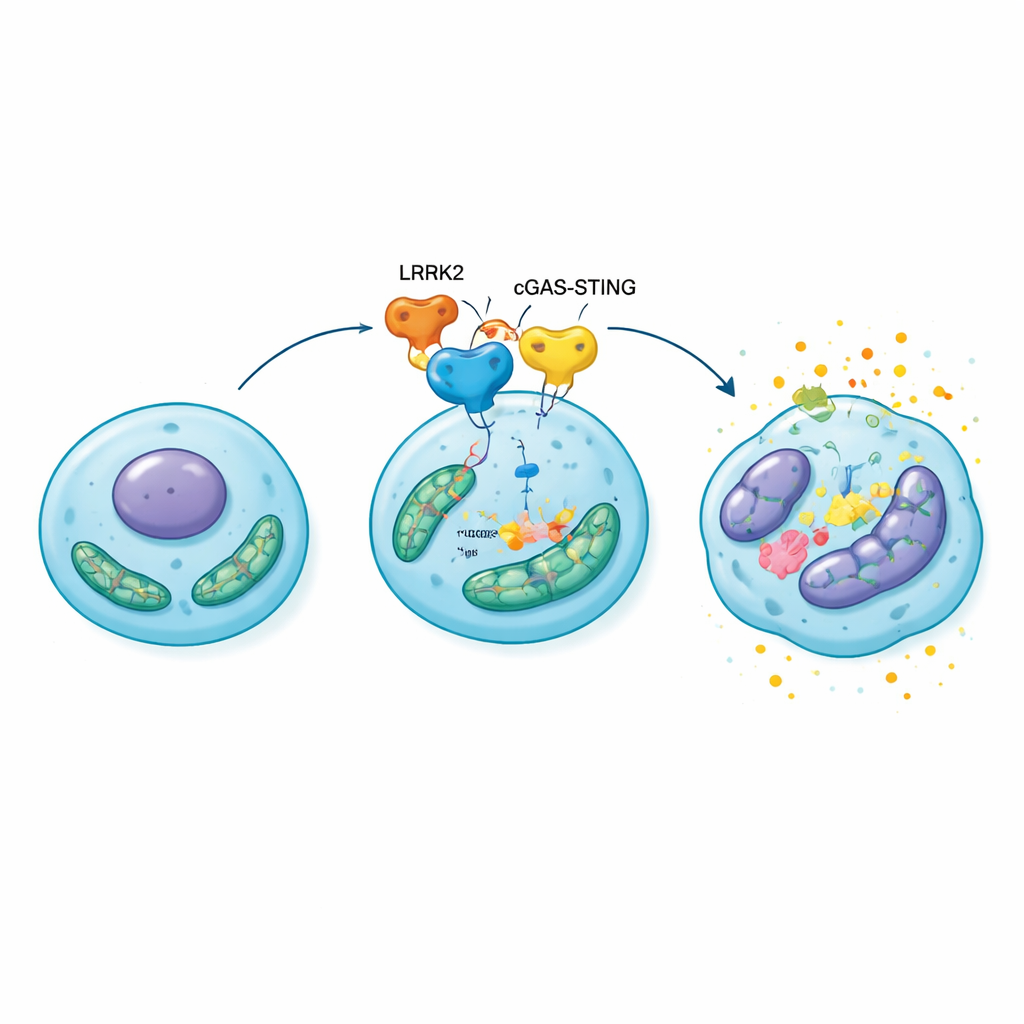
מתאים טרודים לסחוס מתמוטט
כדי לבדוק האם שרשרת מולקולרית זו חשובה עבור המפרק כולו, החוקרים ביטאו באופן מופרז את LRRK2 ישירות בברכיים של חולדות עם דלקת מפרקים ניוונית שנגרמה בניתוח. בהשוואה לבעלי חיים בקבוצת הביקורת, חולדות אלה פיתחו סחוס דק יותר ומאוכל בחומרה רבה יותר, שינויים עצמיים מתחת לפני המפרק ותאים כונדרוציטים מזדקנים יותר שהכילו מולקולות דלקתיות ומפרקות מטריקס. כאשר אותן חולדות טופלו בתרופה החוסמת את STING, הנזק למפרק וההזדקנות התאית פחתו באופן ניכר, ותפקוד המיטוכונדריה התאושש חלקית. ממצאים אלה מציבים את מסלול LRRK2–cGAS–STING–HMGB1 במרכז לולאה מחזקת עצמי: מתח מיטוכונדריאלי מפעיל את מערכת האזעקה, שמגבירה את HMGB1 והדלקת, מה שמחדד את הפגיעה במיטוכונדריה ודוחף עוד כונדרוציטים להזדקנות.
מה משמעות הדבר לטיפול עתידי במפרקים
במילים פשוטות, המחברים מראים כי LRRK2 מתפקד כמפסק תקול שנועל את תאי הסחוס במצב מיושן ועייף ומאיץ את פירוק רקמת המפרק. על ידי הדלקת רשת האזעקה cGAS–STING–HMGB1, פעילות גבוהה של LRRK2 מקשרת מתח פנימי תאי לדלקת כרונית ונזק מבני בדלקת מפרקים ניוונית. עבודה זו מציעה כי תרופות המכוונות להחליש את LRRK2 או להפריע לנתיב cGAS–STING עשויות לסייע בשמירה על תפקוד הכונדרוציטים למשך זמן רב יותר — ובכך להאט את התקדמות הדלקת המפרקית במקום רק להקל על התסמינים.
ציטוט: Zhang, Y., Zhu, Z., Ji, P. et al. cGAS-STING/HMGB1-mediated senescence induced by LRRK2 accelerates cartilage degeneration in osteoarthritis. Cell Death Dis 17, 377 (2026). https://doi.org/10.1038/s41419-026-08651-y
מילות מפתח: ניוון עצם-סחוס, הזדקנות תאית, תפקוד מיטוכונדריאלי לקוי, איתות דלקתי, מסלול LRRK2