Clear Sky Science · it
La senescenza mediata da cGAS-STING/HMGB1 indotta da LRRK2 accelera la degenerazione della cartilagine nell’osteoartrite
Perché le articolazioni consumate contano
Ginocchia doloranti e anche rigide vengono spesso liquidate come un inevitabile effetto dell’invecchiamento, ma l’osteoartrite è più di un semplice “consumo”. Coinvolge cellule viventi nella cartilagine che gradualmente cambiano, smettono di riparare il tessuto e iniziano a inviare segnali di allarme che infiammano l’articolazione. Questo studio identifica un nuovo colpevole molecolare che spinge queste cellule verso uno stato di invecchiamento prematuro, offrendo una prospettiva nuova per comprendere—e potenzialmente rallentare—la progressione dell’osteoartrite.
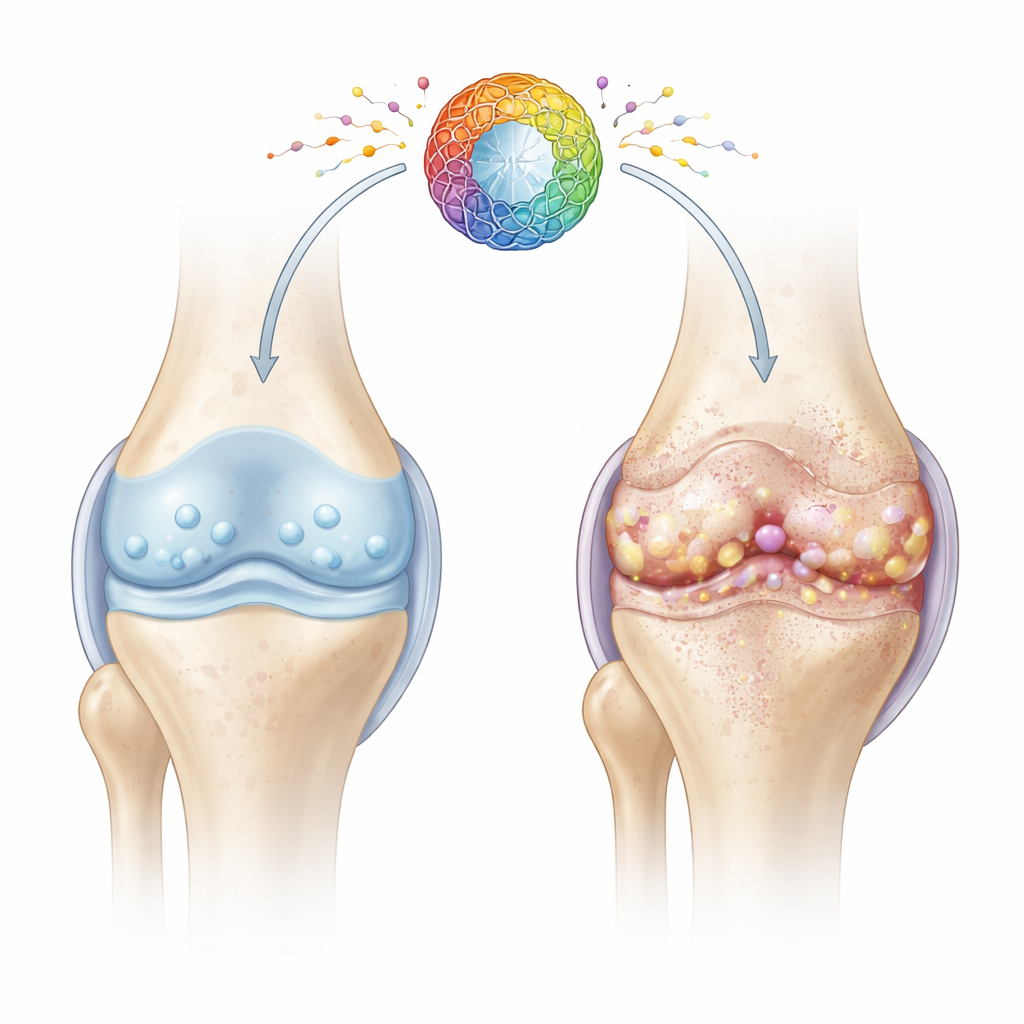
Uno sguardo ravvicinato alle cellule articolari esauste
La cartilagine è il tessuto liscio e gommoso che ammortizza le estremità delle ossa. La sua salute dipende dai condrociti, cellule specializzate che mantengono silenziosamente la matrice cartilaginea per decenni. Con l’età e i traumi, molti condrociti entrano in uno stato chiamato senescenza cellulare: smettono di dividersi, perdono la capacità di riparare e rilasciano un cocktail di molecole infiammatorie e dannose per il tessuto. Gli autori si sono concentrati su come i problemi nelle “centrali energetiche” delle cellule—i mitocondri—possano guidare questo stato di invecchiamento dannoso e accelerare la degenerazione articolare.
Un enzima collegato al Parkinson compare nelle articolazioni doloranti
Analizzando dati pubblici di espressione genica della cartilagine umana, il gruppo ha cercato geni associati sia all’osteoartrite sia all’invecchiamento cellulare. Uno è emerso con evidenza: LRRK2, un grande enzima noto soprattutto per il suo ruolo nel morbo di Parkinson ereditario e in disturbi infiammatori. I livelli di LRRK2 risultavano significativamente più alti nella cartilagine osteoartritica rispetto al tessuto sano. In un modello murino della patologia al ginocchio, LRRK2 era elevato in modo simile nella cartilagine e nelle cellule della membrana sinoviale. Quando i ricercatori aumentarono artificialmente LRRK2 nei condrociti di ratto, centinaia di altri geni mutarono la loro espressione, in particolare quelli coinvolti nell’invecchiamento cellulare e nella segnalazione infiammatoria, suggerendo che LRRK2 non è un mero spettatore ma un promotore attivo del processo patologico.
Come gli allarmi interni trasformano lo stress in danno
Lo studio ha poi inquadrato un sistema d’allarme molecolare interno chiamato via cGAS–STING, che rileva DNA fuori posto nel fluido cellulare—conseguenza frequente del danno mitocondriale—e scatena l’infiammazione. Esperimenti di laboratorio hanno mostrato che l’eccesso di LRRK2 si lega e attiva questa via nei condrociti. L’attivazione, a sua volta, aumentava i livelli e modificava il comportamento di HMGB1, una proteina che normalmente organizza il DNA nel nucleo ma che può agire come potente segnale di pericolo quando rilasciata nell’ambiente cellulare. I condrociti con elevati livelli di LRRK2 presentavano mitocondri gonfi e malfunzionanti, maggior produzione di specie reattive dell’ossigeno (sottoprodotti ossidativi dannosi), ridotta produzione energetica e chiare caratteristiche di senescenza. Bloccare STING, o inibire l’attività di LRRK2 o la sua funzione GTPasica, riduceva HMGB1, attenuava lo stress ossidativo e diminuiti i marcatori di invecchiamento in queste cellule.
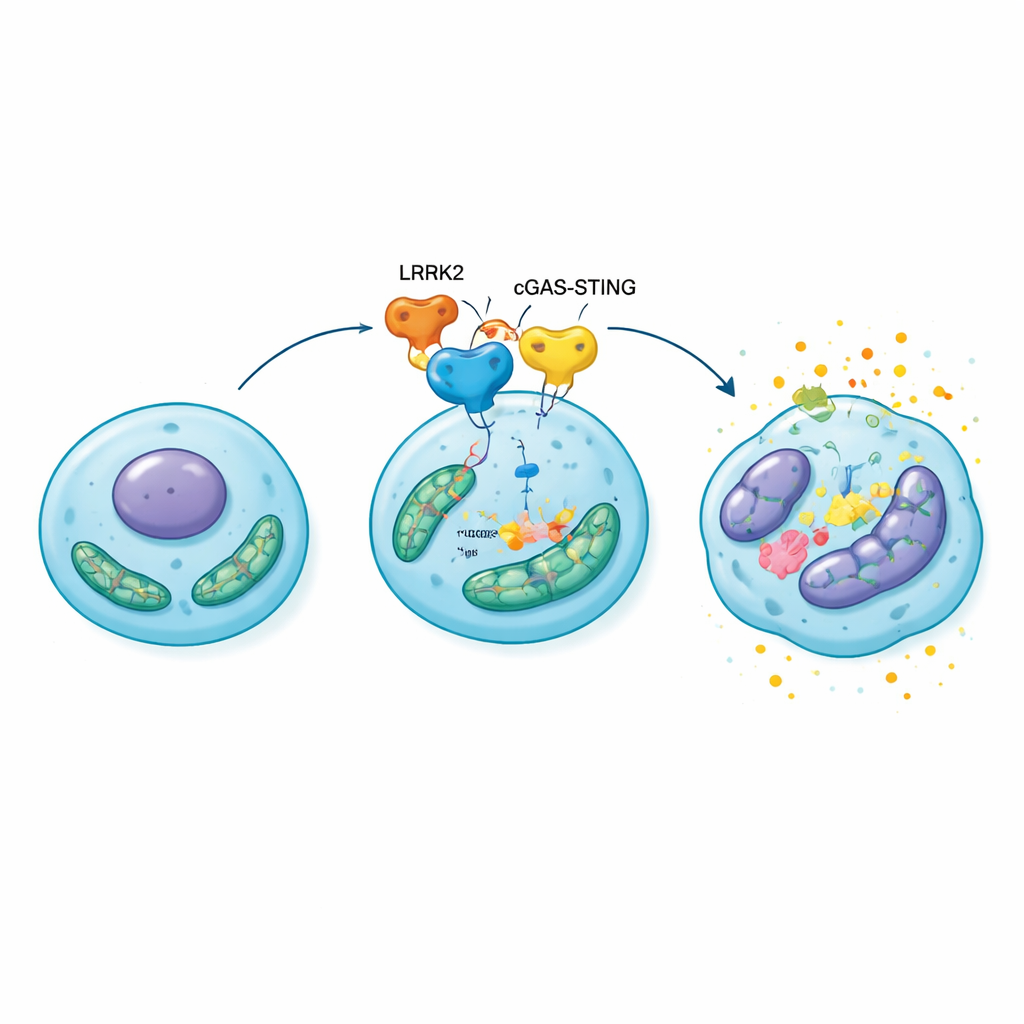
Dalle cellule sotto stress alla cartilagine che crolla
Per verificare se questa catena molecolare avesse rilevanza per l’intera articolazione, i ricercatori sovraesprimerono LRRK2 direttamente nei ginocchia di ratti con osteoartrite indotta chirurgicamente. Rispetto ai controlli, questi animali svilupparono cartilagine più sottile e erosioni maggiori, cambiamenti ossei più pronunciati sotto la superficie articolare e un maggior numero di condrociti senescenti carichi di molecole infiammatorie e degradative della matrice. Quando gli stessi ratti vennero trattati con un farmaco che blocca STING, il danno articolare e la senescenza cellulare risultarono sensibilmente ridotti e la funzione mitocondriale si riprese parzialmente. Questi risultati collocano la via LRRK2–cGAS–STING–HMGB1 al centro di un circuito autorinforzante: lo stress mitocondriale attiva l’allarme, che aumenta HMGB1 e l’infiammazione, peggiorando a sua volta il danno mitocondriale e spingendo più condrociti verso la senescenza.
Cosa significa per la cura delle articolazioni in futuro
In termini concreti, gli autori dimostrano che LRRK2 funziona come un interruttore difettoso che blocca le cellule della cartilagine in uno stato vecchio ed esausto e accelera il degrado del tessuto articolare. Attivando la rete d’allarme cGAS–STING–HMGB1, l’elevata attività di LRRK2 collega lo stress cellulare interno all’infiammazione cronica e al danno strutturale nell’osteoartrite. Questo lavoro suggerisce che farmaci mirati ad abbassare l’attività di LRRK2 o a interrompere la via cGAS–STING potrebbero contribuire a mantenere i condrociti funzionali più a lungo, rallentando potenzialmente la progressione dell’osteoartrite anziché limitarsi ad alleviarne i sintomi.
Citazione: Zhang, Y., Zhu, Z., Ji, P. et al. cGAS-STING/HMGB1-mediated senescence induced by LRRK2 accelerates cartilage degeneration in osteoarthritis. Cell Death Dis 17, 377 (2026). https://doi.org/10.1038/s41419-026-08651-y
Parole chiave: degenerazione osteocondrale, senescenza cellulare, disfunzione mitocondriale, segnalazione infiammatoria, via LRRK2