Clear Sky Science · pt
senescência mediada por cGAS-STING/HMGB1 induzida por LRRK2 acelera a degeneração da cartilagem na osteoartrite
Por que articulações desgastadas importam
Joelhos doloridos e quadris rígidos costumam ser descartados como uma parte inevitável do envelhecimento, mas a osteoartrite é mais do que simples "desgaste." Envolve células vivas dentro da cartilagem que mudam gradualmente, deixam de reparar o tecido e começam a emitir sinais de socorro que inflamam a articulação. Este estudo revela um novo culpado molecular que ajuda a empurrar essas células para um estado de envelhecimento prematuro, oferecendo um ângulo novo para entender — e potencialmente retardar — a progressão da osteoartrite.
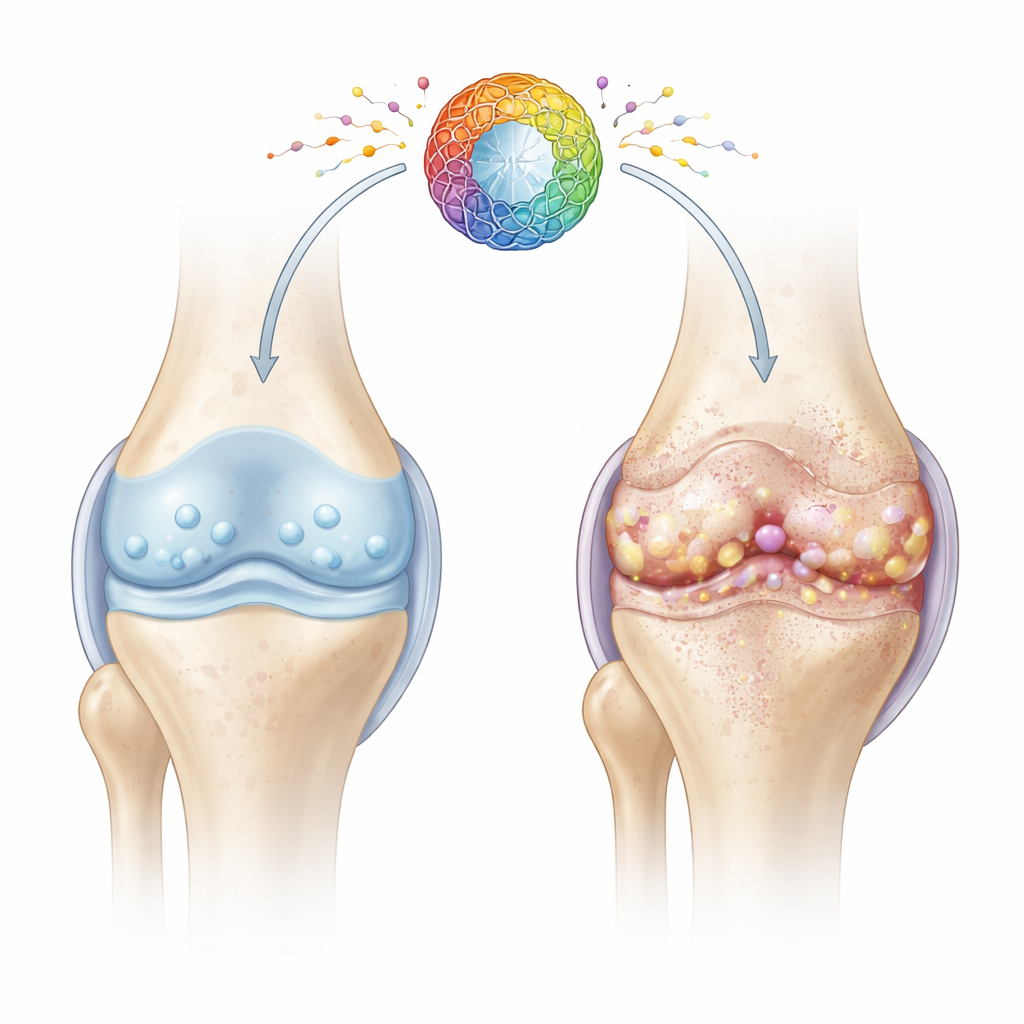
Um olhar mais atento às células articulars cansadas
A cartilagem é o tecido liso e elástico que amortiza as extremidades dos ossos. Sua saúde depende dos condrócitos, células especializadas que mantêm silenciosamente a matriz cartilaginosa por décadas. Com a idade e lesões, muitos condrócitos entram em um estado chamado senescência celular: param de se dividir, perdem a capacidade de reparo e liberam um coquetel de moléculas inflamatórias e degradantes do tecido. Os autores focaram em como problemas nas fábricas de energia das células — as mitocôndrias — podem conduzir esse estado de envelhecimento prejudicial e acelerar a degeneração da articulação.
Uma enzima ligada ao Parkinson aparece em articulações doloridas
Usando dados públicos de expressão gênica da cartilagem humana, a equipe procurou genes ligados tanto à osteoartrite quanto ao envelhecimento celular. Um se destacou: LRRK2, uma grande enzima mais conhecida por seu papel no mal de Parkinson hereditário e em desordens inflamatórias. Os níveis de LRRK2 estavam marcadamente mais altos na cartilagem osteoartrítica em comparação com o tecido saudável. Em um modelo de rato com osteoartrite de joelho, LRRK2 também foi elevado nas células da cartilagem e na membrana sinovial. Quando os pesquisadores aumentaram artificialmente LRRK2 em condrócitos de rato, centenas de outros genes mudaram sua expressão, especialmente aqueles envolvidos no envelhecimento celular e na sinalização inflamatória, sugerindo que LRRK2 não é apenas um espectador, mas um motor ativo do processo da doença.
Como alarmes internos convertem estresse em dano
O estudo então concentrou-se em um sistema de alarme molecular dentro das células chamado via cGAS–STING, que detecta DNA fora do lugar no citosol — uma consequência frequente de dano mitocondrial — e desencadeia inflamação. Experimentos em laboratório mostraram que o excesso de LRRK2 se liga e ativa essa via em condrócitos. A ativação, por sua vez, aumentou os níveis e alterou o comportamento da HMGB1, uma proteína que normalmente ajuda a organizar o DNA no núcleo, mas que pode atuar como um potente sinal de perigo quando liberada para o entorno celular. Condrócitos com alto LRRK2 exibiram mitocôndrias inchadas e disfuncionais, mais espécies reativas de oxigênio (subprodutos tóxicos do oxigênio), produção de energia reduzida e claros sinais de senescência. Bloquear STING, ou inibir a atividade de LRRK2 ou sua função GTPase, reduziu HMGB1, aliviou o estresse oxidativo e diminuiu marcadores de envelhecimento nessas células.
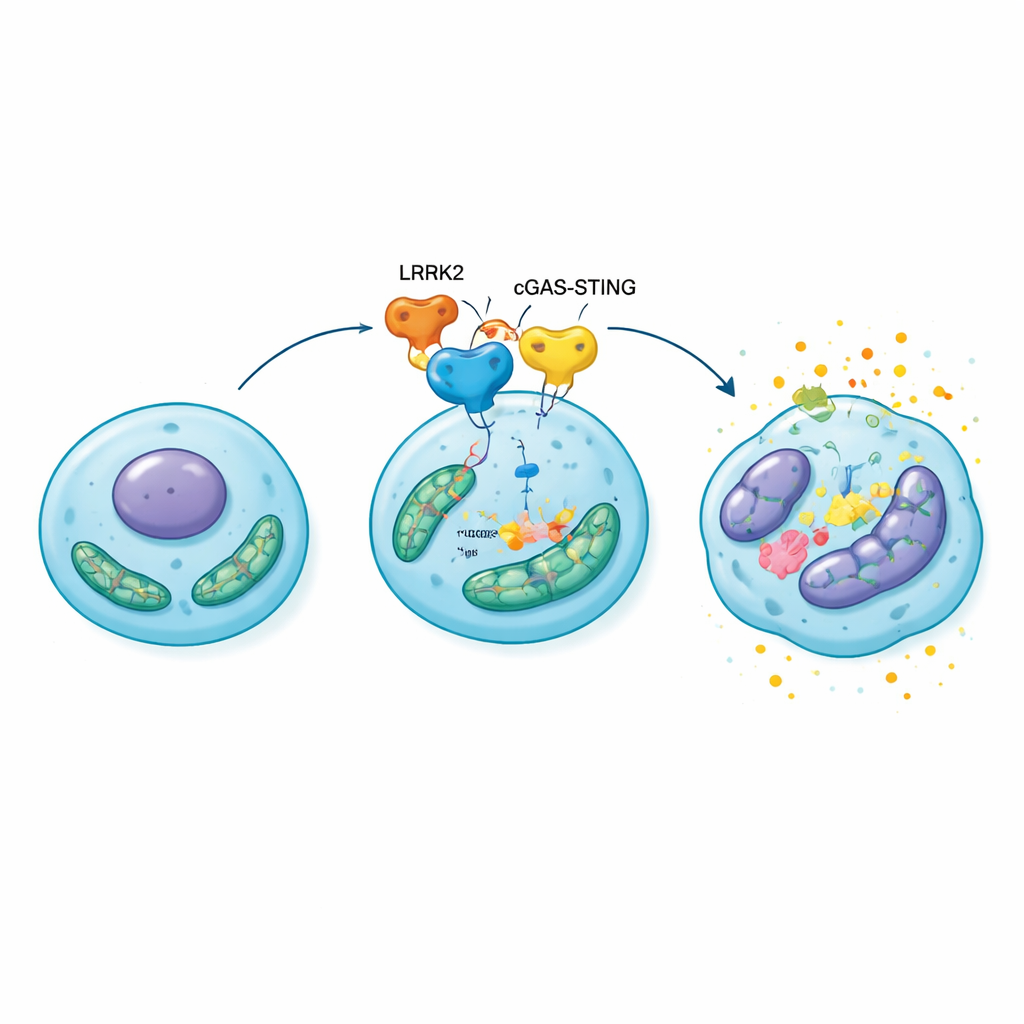
De células estressadas à cartilagem em colapso
Para avaliar se essa reação em cadeia molecular importava para articulações inteiras, os pesquisadores superexpressaram LRRK2 diretamente nos joelhos de ratos com osteoartrite induzida cirurgicamente. Em comparação com os animais controle, esses ratos desenvolveram cartilagem mais fina e erodida, maiores alterações ósseas sob a superfície articular e mais condrócitos senescentes carregados de moléculas inflamatórias e degradantes da matriz. Quando os mesmos ratos foram tratados com um fármaco que bloqueia STING, o dano articular e o envelhecimento celular foram reduzidos de forma perceptível, e a função mitocondrial se recuperou parcialmente. Esses resultados colocam a via LRRK2–cGAS–STING–HMGB1 no centro de um circuito auto-reforçador: o estresse mitocondrial ativa o sistema de alarme, que aumenta HMGB1 e a inflamação, o que por sua vez aprofunda o dano mitocondrial e empurra mais condrócitos para a senescência.
O que isso significa para o cuidado das articulações no futuro
Em termos diretos, os autores mostram que LRRK2 age como um interruptor defeituoso que trava as células da cartilagem em um estado velho e exaurido e acelera a degradação do tecido articular. Ao ativar a rede de alarme cGAS–STING–HMGB1, a alta atividade de LRRK2 conecta o estresse celular interno à inflamação crônica e ao dano estrutural na osteoartrite. Este trabalho sugere que fármacos destinados a reduzir a atividade de LRRK2 ou interromper a via cGAS–STING poderiam ajudar a manter os condrócitos funcionais por mais tempo, potencialmente retardando a progressão da osteoartrite em vez de apenas aliviar seus sintomas.
Citação: Zhang, Y., Zhu, Z., Ji, P. et al. cGAS-STING/HMGB1-mediated senescence induced by LRRK2 accelerates cartilage degeneration in osteoarthritis. Cell Death Dis 17, 377 (2026). https://doi.org/10.1038/s41419-026-08651-y
Palavras-chave: degeneração osteocondral, senescência celular, disfunção mitocondrial, sinalização inflamatória, via LRRK2