Clear Sky Science · de
cGAS-STING/HMGB1-vermittelte Seneszenz, ausgelöst durch LRRK2, beschleunigt den Knorpelabbau bei Osteoarthritis
Warum abgenutzte Gelenke wichtig sind
Schmerzende Knie und steife Hüften werden oft als unvermeidlicher Bestandteil des Älterwerdens abgetan, doch Osteoarthritis ist mehr als bloßer „Verschleiß“. Beteiligte sind lebende Zellen im Knorpel, die sich allmählich verändern, die Reparatur einstellen und Stresssignale aussenden, die das Gelenk entzünden. Diese Studie enthüllt ein neues molekulares Element, das diese Zellen in einen vorzeitig gealterten Zustand treibt, und liefert damit eine neue Perspektive für das Verständnis — und möglicherweise das Verlangsamen — des Fortschreitens der Osteoarthritis.
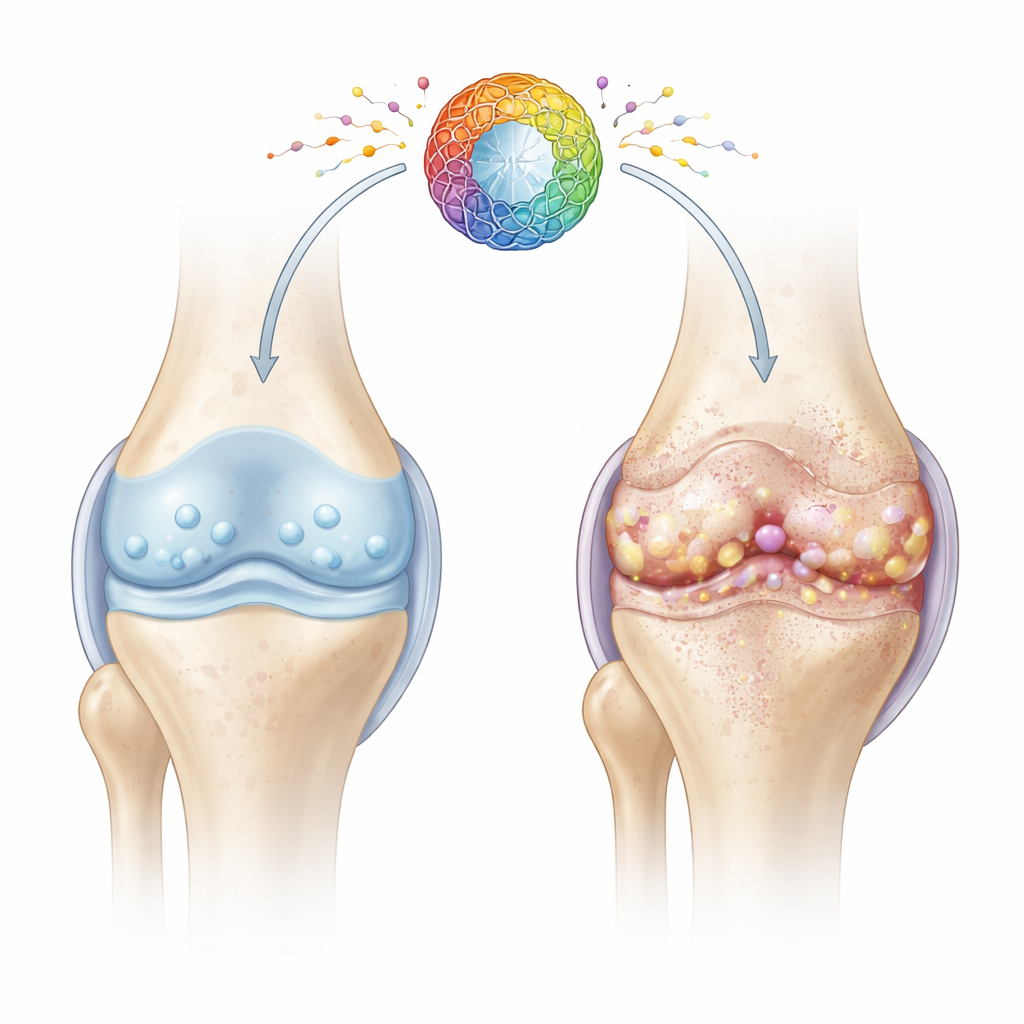
Ein genauerer Blick auf erschöpfte Gelenkzellen
Knorpel ist das glatte, gummiartige Gewebe, das die Enden der Knochen polstert. Seine Gesundheit hängt von Chondrozyten ab, spezialisierten Zellen, die über Jahrzehnte die Knorpelmatrix instand halten. Mit dem Alter und nach Verletzungen geraten viele Chondrozyten in einen Zustand, der als zelluläre Seneszenz bezeichnet wird: Sie teilen sich nicht mehr, verlieren ihre Reparaturfähigkeit und setzen ein Gemisch aus entzündungsfördernden und gewebeschädigenden Molekülen frei. Die Autor:innen konzentrierten sich darauf, wie Probleme in den Energiezentralen der Zellen — den Mitochondrien — diesen schädlichen Alterungszustand antreiben und die Gelenkdegeneration beschleunigen könnten.
Ein mit Parkinson verknüpftes Enzym taucht in schmerzenden Gelenken auf
Mithilfe öffentlicher Genexpressionsdaten aus menschlichem Knorpel suchte das Team nach Genen, die sowohl mit Osteoarthritis als auch mit zellulärem Altern verbunden sind. Eines stach hervor: LRRK2, ein großes Enzym, das vor allem für seine Rolle bei vererbter Parkinson-Erkrankung und entzündlichen Störungen bekannt ist. Die LRRK2-Spiegel waren im osteoarthritischen Knorpel deutlich höher als im gesunden Gewebe. In einem Rattenmodell der Kniearthrose war LRRK2 ebenfalls in Knorpel- und Gelenkschleimhautzellen erhöht. Wenn die Forschenden LRRK2 in Ratten-Chondrozyten künstlich hochregulierten, veränderten sich Hunderte anderer Gene, insbesondere solche, die an Zellalterung und entzündlicher Signalgebung beteiligt sind, was darauf hindeutet, dass LRRK2 nicht nur ein beiläufiger Faktor, sondern ein aktiver Treiber des Krankheitsprozesses ist.
Wie interne Warnsysteme Stress in Schaden verwandeln
Die Studie fokussierte dann ein molekulares Alarmsystem in der Zelle, den cGAS–STING-Weg, der fehlplatziertes DNA im Zellplasma erkennt — eine häufige Folge mitochondrialer Schäden — und Entzündung auslöst. Laborversuche zeigten, dass überschüssiges LRRK2 an diesen Weg bindet und ihn in Chondrozyten aktiviert. Die Aktivierung erhöhte wiederum die Menge und veränderte das Verhalten von HMGB1, einem Protein, das normalerweise die DNA im Zellkern organisiert, aber als starkes Gefahrensignal wirkt, wenn es in die Umgebung der Zelle freigesetzt wird. Chondrozyten mit hohem LRRK2 zeigten aufgequollene, fehlfunktionierende Mitochondrien, mehr reaktive Sauerstoffspezies (schädliche Sauerstoffnebenprodukte), reduzierte Energieproduktion und klare Kennzeichen der Seneszenz. Das Blockieren von STING oder das Hemmen der LRRK2-Aktivität bzw. seiner GTPase-Funktion dämpfte HMGB1, verringerte oxidativen Stress und reduzierte Alterungsmarker in diesen Zellen.
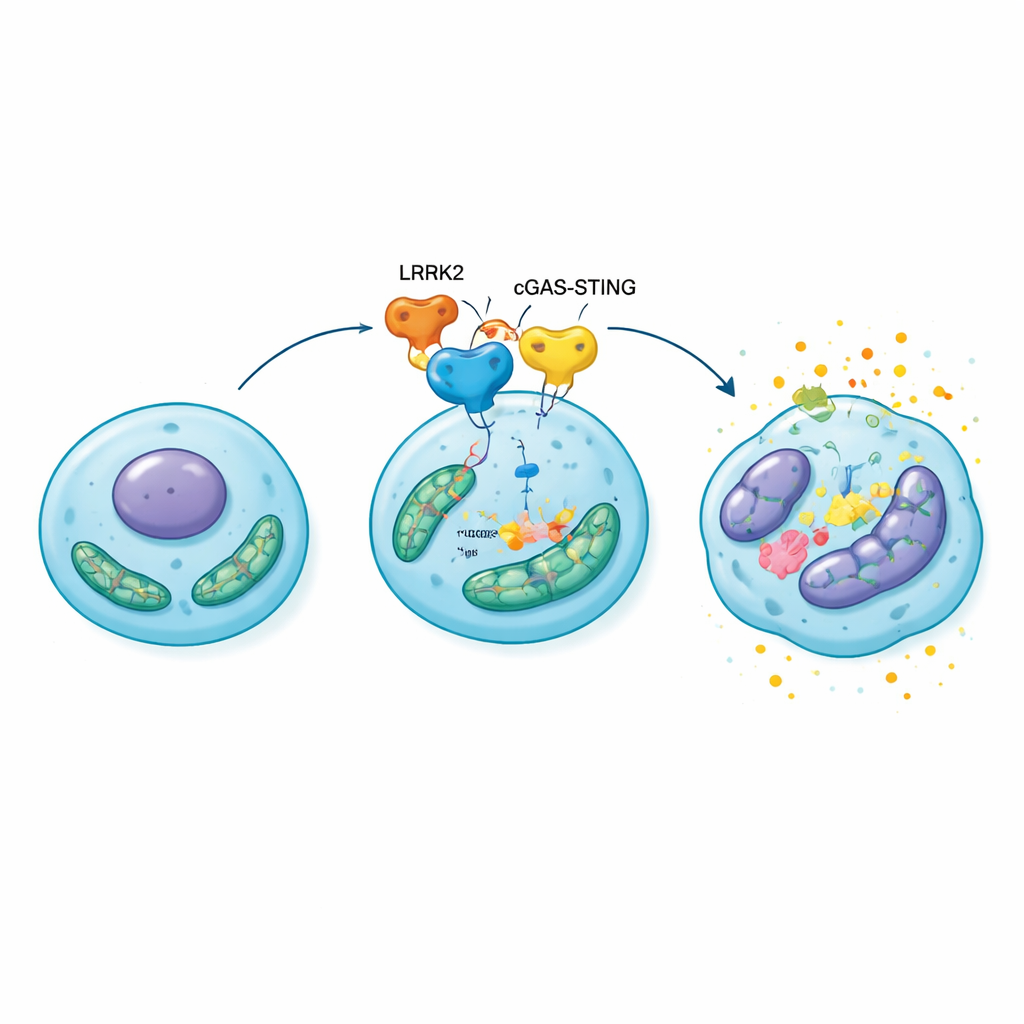
Von gestressten Zellen zu bröckelndem Knorpel
Um zu prüfen, ob diese molekulare Kaskade für ganze Gelenke relevant ist, überexprimierten die Forschenden LRRK2 direkt in den Knien von Ratten mit chirurgisch induzierter Osteoarthritis. Im Vergleich zu Kontrolltieren entwickelten diese Ratten dünneren, stärker erodierten Knorpel, ausgeprägtere knöcherne Veränderungen unter der Gelenkoberfläche und mehr seneszente Chondrozyten, die mit entzündlichen und matrixabbauenden Molekülen beladen waren. Wurden dieselben Ratten mit einem STING-blockierenden Medikament behandelt, waren Gelenkschäden und Zellalterung deutlich reduziert und die mitochondriale Funktion teilweise wiederhergestellt. Diese Ergebnisse stellen den LRRK2–cGAS–STING–HMGB1-Weg in den Mittelpunkt einer selbstverstärkenden Schleife: Mitochondriale Belastung aktiviert das Alarmsystem, das HMGB1 und Entzündung steigert, wodurch mitochondriale Schäden zunehmen und mehr Chondrozyten in die Seneszenz getrieben werden.
Was das für die künftige Gelenkbehandlung bedeutet
Einfach ausgedrückt zeigen die Autor:innen, dass LRRK2 wie ein fehlerhafter Schalter wirkt, der Knorpelzellen in einen alten, erschöpften Zustand verriegelt und den Abbau des Gelenkgewebes beschleunigt. Indem es das cGAS–STING–HMGB1-Alarmsystem aktiviert, verbindet hohe LRRK2-Aktivität zellulären Stress mit chronischer Entzündung und strukturellem Schaden bei Osteoarthritis. Die Arbeit legt nahe, dass Wirkstoffe, die darauf abzielen, LRRK2 zu dämpfen oder den cGAS–STING-Weg zu unterbrechen, dazu beitragen könnten, Chondrozyten länger funktionsfähig zu halten und womöglich das Fortschreiten der Osteoarthritis zu verlangsamen, statt nur ihre Symptome zu lindern.
Zitation: Zhang, Y., Zhu, Z., Ji, P. et al. cGAS-STING/HMGB1-mediated senescence induced by LRRK2 accelerates cartilage degeneration in osteoarthritis. Cell Death Dis 17, 377 (2026). https://doi.org/10.1038/s41419-026-08651-y
Schlüsselwörter: osteochondrale Degeneration, zelluläre Seneszenz, mitochondriale Dysfunktion, entzündliche Signalgebung, LRRK2-Signalweg