Clear Sky Science · ru
Ускоренное разрушение хряща при остеоартрите: сенесценция, опосредованная cGAS-STING/HMGB1, индуцированная LRRK2
Почему изношенные суставы имеют значение
Ноющие колени и скованные бедра часто списывают как неизбежную часть старения, но остеоартрит — это не просто «износ». Вовлечены живые клетки в хряще, которые со временем меняются, теряют способность восстанавливать ткань и начинают посылать сигналы бедствия, вызывающие воспаление в суставе. В этом исследовании выявлен новый молекулярный виновник, который способствует преждевременному старению этих клеток, предлагая новый угол для понимания — и потенциального замедления — прогрессирования остеоартрита.
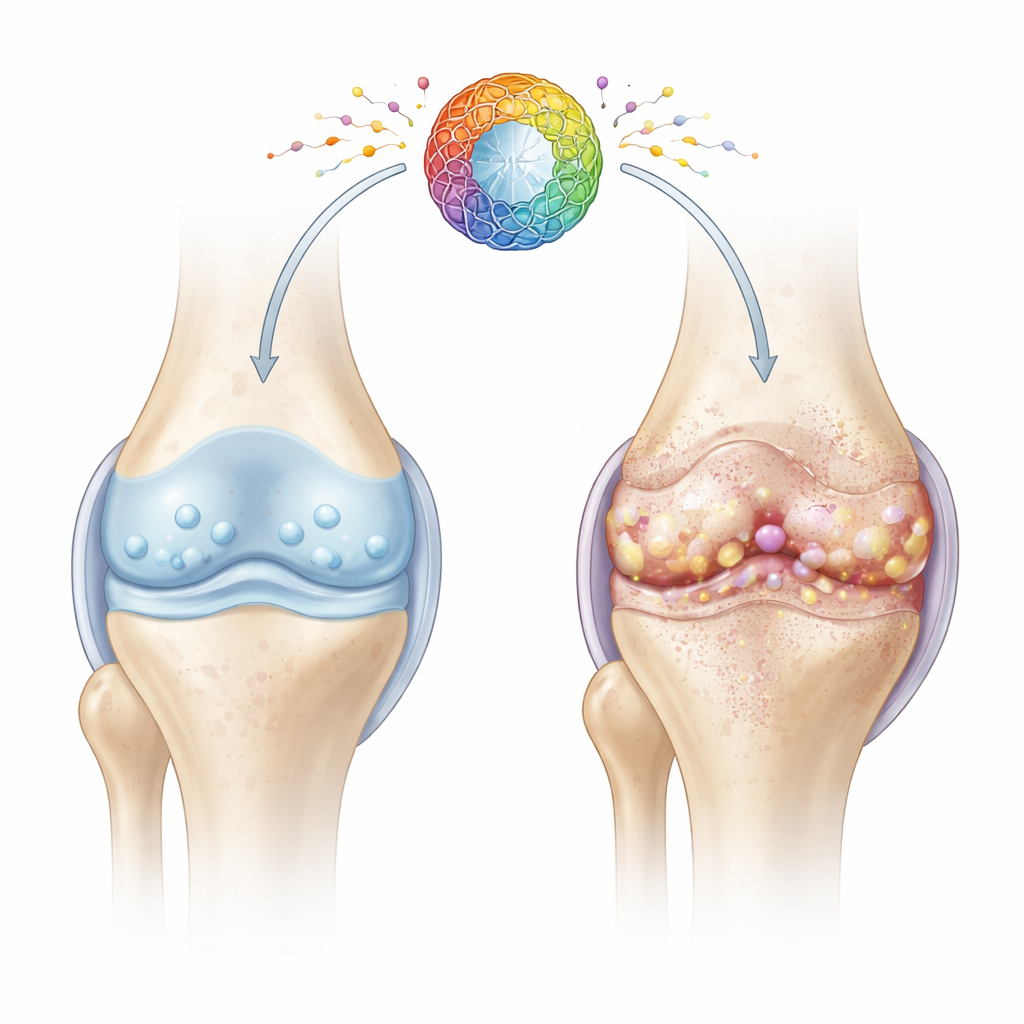
Ближе к уставшим клеткам сустава
Хрящ — это гладкая, упругая ткань, смягчающая концы костей. Его здоровье зависит от хондроцитов — специализированных клеток, которые в течение десятилетий поддерживают матрицу хряща. С возрастом и при повреждении многие хондроциты входят в состояние, называемое клеточной сенесценцией: они перестают делиться, теряют репаративную способность и выделяют коктейль провоспалительных и разрушающих ткань молекул. Авторы сосредоточились на том, как проблемы в энергетических «фабриках» клетки — митохондриях — могут запустить это вредоносное старение и ускорить дегенерацию сустава.
Фермент, связанный с болезнью Паркинсона, обнаружен в больных суставах
Используя общедоступные данные экспрессии генов человека в хряще, команда искала гены, связанные одновременно с остеоартритом и клеточным старением. Выделился один ген: LRRK2 — крупный фермент, более известный по своей роли в наследственном болезни Паркинсона и воспалительных расстройствах. Уровни LRRK2 были заметно выше в остеоартритическом хряще по сравнению со здоровой тканью. В модели остеоартрита колена у крыс LRRK2 также повышался в клетках хряща и синовиальной выстилки. Когда исследователи искусственно повышали экспрессию LRRK2 в хондроцитах крыс, сотни других генов меняли свою активность, особенно те, что вовлечены в клеточное старение и воспалительную сигнализацию, что говорит о том, что LRRK2 не просто наблюдатель, а активный драйвер процесса болезни.
Как внутренние сигнализации превращают стресс в повреждение
Дальше исследование сосредоточилось на молекулярной системе тревоги внутри клетки — пути cGAS–STING, который обнаруживает неправильно локализованную ДНК в цитоплазме — частое следствие повреждения митохондрий — и запускает воспаление. Лабораторные эксперименты показали, что избыток LRRK2 связывается с этой системой и активирует её в хондроцитах. Активация, в свою очередь, повышала уровни и меняла поведение HMGB1 — белка, который обычно помогает организовывать ДНК в ядре, но может выступать мощным сигналом опасности при выходе в окружение клетки. Хондроциты с высоким уровнем LRRK2 имели вздутые, нефункционирующие митохондрии, больше реактивных форм кислорода (повреждающих побочных продуктов кислородного метаболизма), снижённое производство энергии и явные признаки сенесценции. Блокирование STING, либо ингибирование активности LRRK2 или его GTPазной функции уменьшало HMGB1, ослабляло оксидативный стресс и снижало маркёры старения в этих клетках.
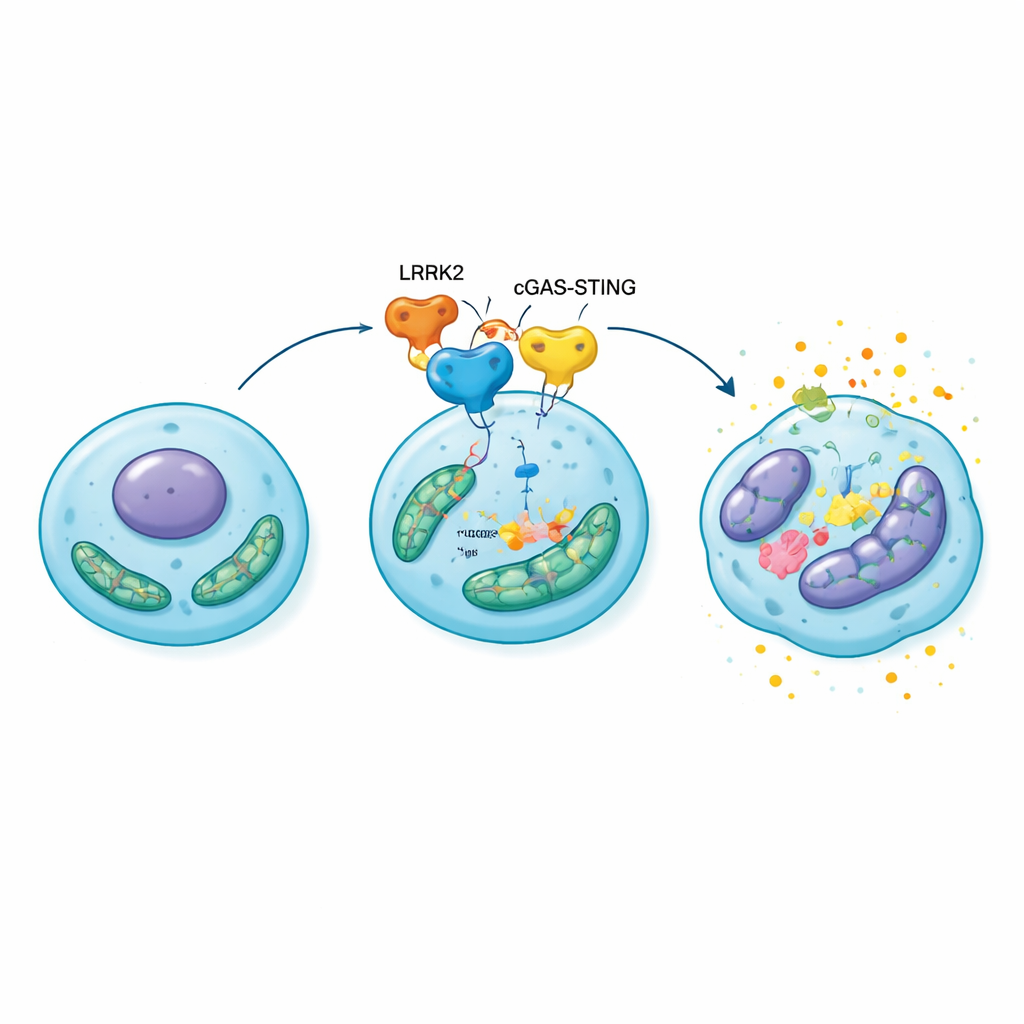
От напряжённых клеток к разрушающемуся хрящу
Чтобы выяснить, имеет ли эта молекулярная цепочка значение для целых суставов, исследователи переэкспрессировали LRRK2 непосредственно в коленях крыс с хирургически индуцированным остеоартритом. По сравнению с контрольными животными у этих крыс развивался более тонкий, сильнее эрозированный хрящ, более выраженные изменения кости под суставной поверхностью и больше сенесцентных хондроцитов, загруженных провоспалительными и разрушающими матрицу молекулами. Когда те же животные получали препарат, блокирующий STING, повреждение сустава и старение клеток заметно уменьшались, а функция митохондрий частично восстанавливалась. Эти результаты ставят путь LRRK2–cGAS–STING–HMGB1 в центр самоподдерживающейся петли: митохондриальный стресс активирует систему тревоги, что повышает HMGB1 и воспаление, которые в свою очередь усиливают митохондриальные повреждения и переводят всё больше хондроцитов в состояние сенесценции.
Что это означает для будущего ухода за суставами
Проще говоря, авторы показывают, что LRRK2 действует как неисправный переключатель, который фиксирует клетки хряща в старом, истощённом состоянии и ускоряет разрушение суставной ткани. Включая сеть сигналов cGAS–STING–HMGB1, повышенная активность LRRK2 связывает внутренний клеточный стресс с хроническим воспалением и структурными повреждениями при остеоартрите. Эта работа указывает на то, что препараты, направленные на снижение активности LRRK2 или на разрыв пути cGAS–STING, могут помочь дольше сохранять функциональность хондроцитов и потенциально замедлять прогрессирование остеоартрита, а не только облегчать его симптомы.
Цитирование: Zhang, Y., Zhu, Z., Ji, P. et al. cGAS-STING/HMGB1-mediated senescence induced by LRRK2 accelerates cartilage degeneration in osteoarthritis. Cell Death Dis 17, 377 (2026). https://doi.org/10.1038/s41419-026-08651-y
Ключевые слова: остеохондральная дегенерация, клеточная сенесценция, митохондриальная дисфункция, воспалительная сигнализация, путь LRRK2