Clear Sky Science · tr
LRRK2 tarafından indüklenen cGAS-STING/HMGB1 aracılı senesans osteoartritte kıkırdak dejenerasyonunu hızlandırıyor
Aşınmış eklemler neden önemli
Ağrılı dizler ve sert kalçalar genellikle yaşlanmanın kaçınılmaz bir parçası olarak görülür, ama osteoartrit basit bir "aşınma"dan daha fazlasıdır. Eklem kıkırdağı içindeki canlı hücreler zamanla değişir, doku onarımını durdurur ve eklemi iltihaplandıran alarm sinyalleri göndermeye başlar. Bu çalışma, bu hücreleri erken yaşlanma durumuna iten yeni bir moleküler suçluyu ortaya koyuyor ve osteoartritin ilerleyişini anlamak—ve potansiyel olarak yavaşlatmak—için yeni bir bakış açısı sunuyor.
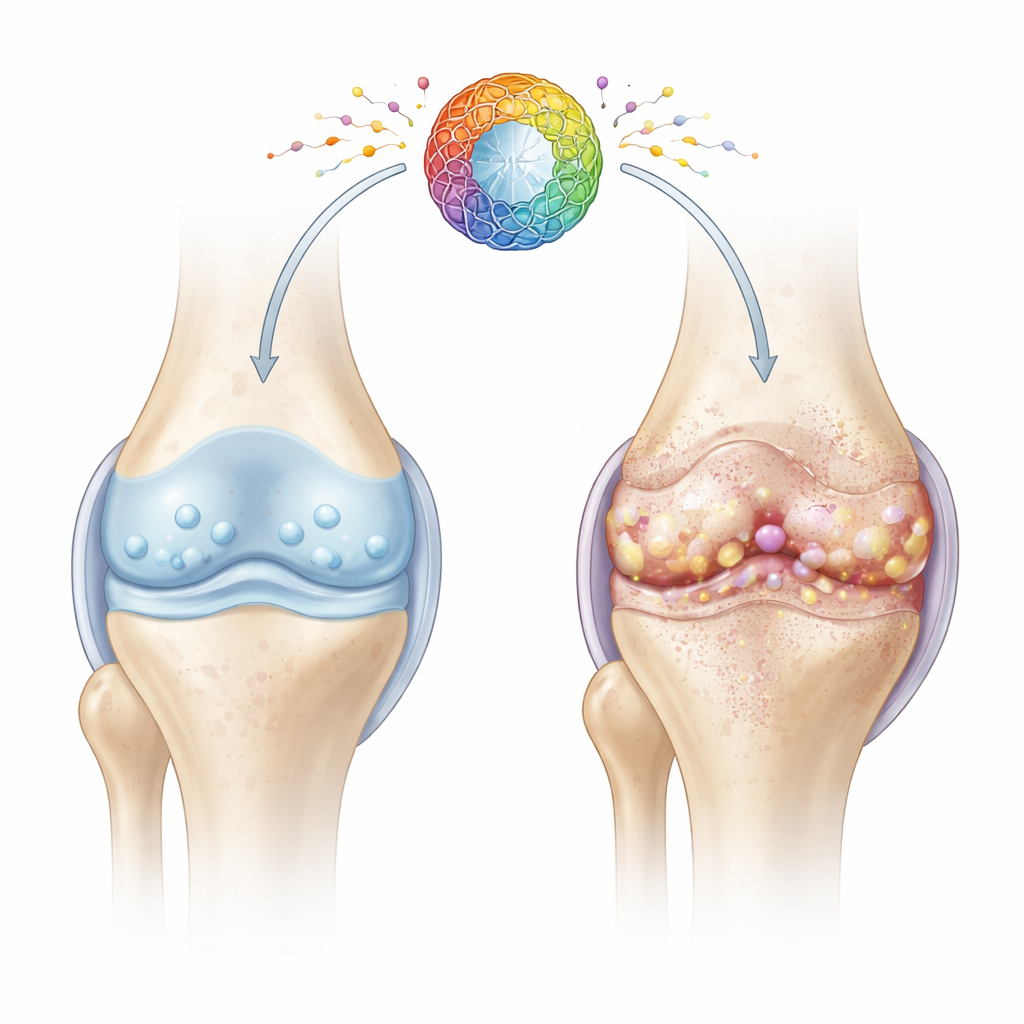
Yorgun eklem hücrelerine daha yakından bakış
Kıkırdak, kemik uçlarını yastıklayan pürüzsüz, esnek bir dokudur. Sağlığı, kıkırdak matrisini onlarca yıl boyunca sessizce koruyan kondrosit adı verilen özelleşmiş hücrelere bağlıdır. Yaş ve yaralanma ile birçok kondrosit hücresel senesans adı verilen bir duruma girer: bölünmeyi durdurur, onarım kapasitesini kaybeder ve inflamasyon ile doku hasarına yol açan moleküllerin bir kokteylini salar. Yazarlar, hücrelerin enerji fabrikalarındaki—mitokondrilerdeki—sorunların bu zararlı yaşlanma durumunu tetikleyip eklem dejenerasyonunu hızlandırıp hızlandırmadığına odaklandı.
Parkinson ile bağlantılı bir enzim ağrılı eklemlerde ortaya çıktı
İnsan kıkırdağından elde edilen halka açık gen ekspresyon verilerini kullanarak ekip, hem osteoartrit hem de hücresel yaşlanma ile ilişkili genleri aradı. Öne çıkan bir gen vardı: LRRK2, miras alınan Parkinson hastalığındaki ve inflamatuar bozukluklardaki rolüyle daha çok bilinen büyük bir enzim. LRRK2 düzeyleri, sağlıklı dokuya kıyasla osteoartritik kıkırdakta belirgin şekilde daha yüksekti. Diz osteoartriti rat modelinde de LRRK2, eklem kıkırdağında ve yüzey hücrelerinde benzer şekilde artmıştı. Araştırmacılar rat kondrositlerinde yapay olarak LRRK2’yi artırdıklarında yüzlerce başka gen değişti; özellikle hücresel yaşlanma ve inflamatuar sinyalizasyonla ilgili genler etkilendi, bu da LRRK2’nin sadece bir gözlemci değil, hastalık sürecinin aktif bir itici gücü olduğunu düşündürüyor.
İçsel alarmlar stresin hasara dönüşmesini nasıl sağlıyor
Çalışma daha sonra hücre içindeki cGAS–STING adlı moleküler bir alarm sistemine odaklandı; bu yol, hücre sıvısına yanlış yerde bulunan DNA’yı algılar—bu genellikle mitokondri hasarının bir sonucudur—ve inflamasyonu tetikler. Laboratuvar deneyleri, aşırı LRRK2’nin kondrositlerde bu yolu bağladığını ve aktive ettiğini gösterdi. Yolu aktive etmek, genellikle çekirdekte DNA’yı düzenlemeye yardım eden fakat çevreye salındığında güçlü bir tehlike sinyali olarak davranabilen HMGB1 proteininin seviyelerini artırdı ve davranışını değiştirdi. Yüksek LRRK2’ye sahip kondrositler şişmiş, işlevsiz mitokondriler, artmış reaktif oksijen türleri (zararlı oksijen yan ürünleri), azalmış enerji üretimi ve belirgin senesans işaretleri gösterdi. STING’in bloke edilmesi ya da LRRK2’nin aktivitesinin veya GTPaz fonksiyonunun inhibe edilmesi HMGB1’i düşürdü, oksidatif stresi hafifletti ve bu hücrelerdeki yaşlanma belirteçlerini azalttı.
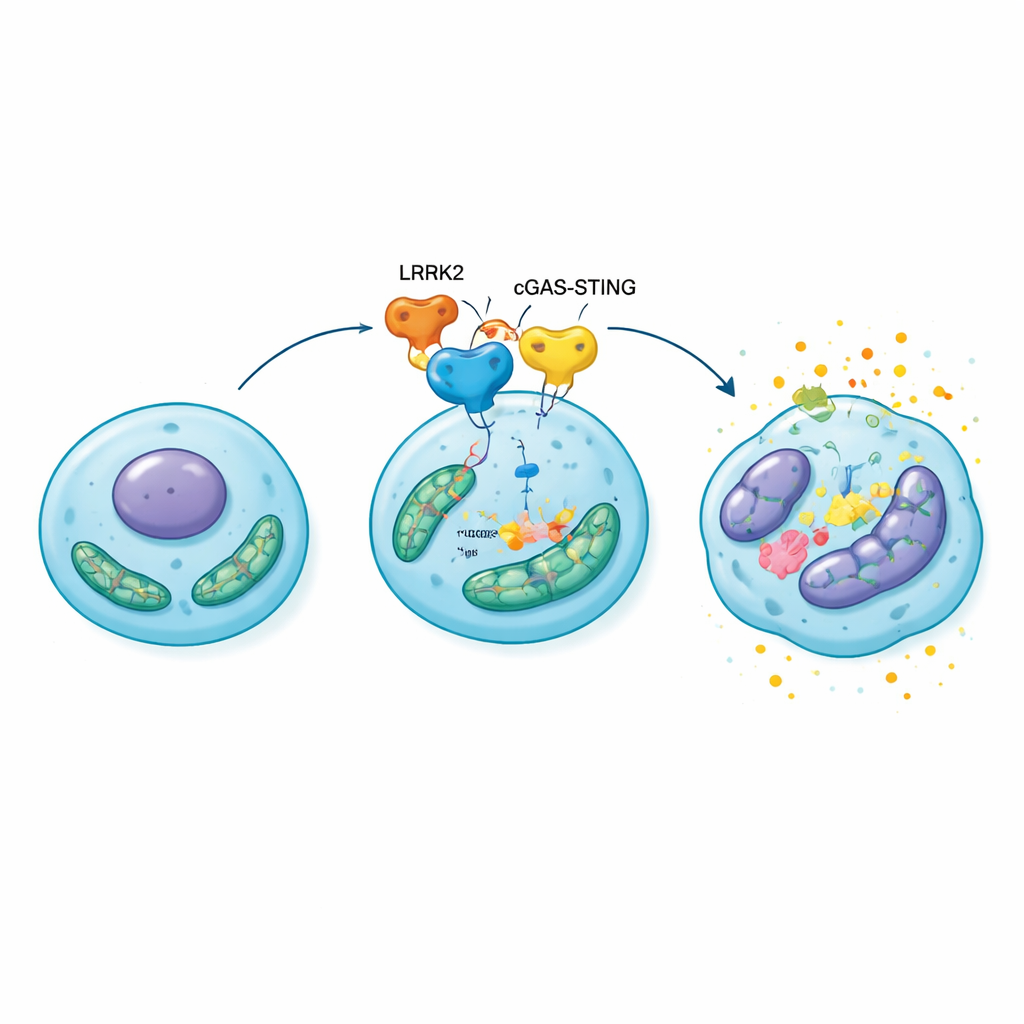
Stresli hücrelerden çöken kıkırdağa
Bu moleküler zincirleme reaksiyonun tüm eklemler için önemli olup olmadığını görmek için araştırmacılar, cerrahi olarak indüklenmiş osteoartritli ratlerin dizlerine doğrudan LRRK2 aşırı ifadeyi aktarımını yaptılar. Kontrol hayvanlara kıyasla bu ratlerde daha ince, daha aşınmış kıkırdak, eklem yüzeyinin altındaki kemikte daha fazla değişiklik ve inflamatuar ile matrisi parçalayan moleküllerle yüklü daha fazla senescent kondrosit gelişti. Aynı ratlere STING’i bloke eden bir ilaç verildiğinde eklem hasarı ve hücresel yaşlanma belirgin şekilde azaldı ve mitokondri fonksiyonu kısmen toparlandı. Bu sonuçlar LRRK2–cGAS–STING–HMGB1 yolunu kendini güçlendiren bir döngünün merkezine yerleştiriyor: mitokondri stresi alarm sistemini aktive ediyor, bu HMGB1’i ve inflamasyonu artırıyor, bu da mitokondri hasarını derinleştiriyor ve daha fazla kondrositi senesansa itiyor.
Geleceğin eklem bakımına etkileri
Açıkça söylemek gerekirse, yazarlar LRRK2’nin kıkırdak hücrelerini yaşlı, tükenmiş bir duruma kilitleyen hatalı bir anahtar gibi davrandığını ve eklem dokusunun yıkımını hızlandırdığını gösteriyor. Yüksek LRRK2 aktivitesi cGAS–STING–HMGB1 alarm ağını açarak hücresel iç stres ile kronik inflamasyon ve osteoartritteki yapısal hasar arasında bir bağ kuruyor. Bu çalışma, LRRK2’yi azaltmayı veya cGAS–STING yolunu kesmeyi hedef alan ilaçların kondrositleri daha uzun süre fonksiyonel tutmaya yardımcı olabileceğini ve böylece osteoartritin ilerleyişini semptomları hafifletmenin ötesinde yavaşlatma potansiyeli taşıdığını öne sürüyor.
Atıf: Zhang, Y., Zhu, Z., Ji, P. et al. cGAS-STING/HMGB1-mediated senescence induced by LRRK2 accelerates cartilage degeneration in osteoarthritis. Cell Death Dis 17, 377 (2026). https://doi.org/10.1038/s41419-026-08651-y
Anahtar kelimeler: osteokondral dejenerasyon, hücresel senesans, mitokondriyal disfonksiyon, inflamatuar sinyalizasyon, LRRK2 yolu