Clear Sky Science · es
Senescencia mediada por cGAS-STING/HMGB1 inducida por LRRK2 acelera la degeneración del cartílago en la osteoartritis
Por qué importan las articulaciones desgastadas
Las rodillas doloridas y las caderas rígidas suelen atribuirse a una consecuencia inevitable del envejecimiento, pero la osteoartritis es más que un simple "desgaste". Implica células vivas dentro del cartílago que cambian gradualmente, dejan de reparar el tejido y comienzan a emitir señales de alarma que inflaman la articulación. Este estudio descubre un nuevo culpable molecular que impulsa a estas células hacia un estado de envejecimiento prematuro, ofreciendo una nueva perspectiva para entender—y potencialmente ralentizar—la progresión de la osteoartritis.
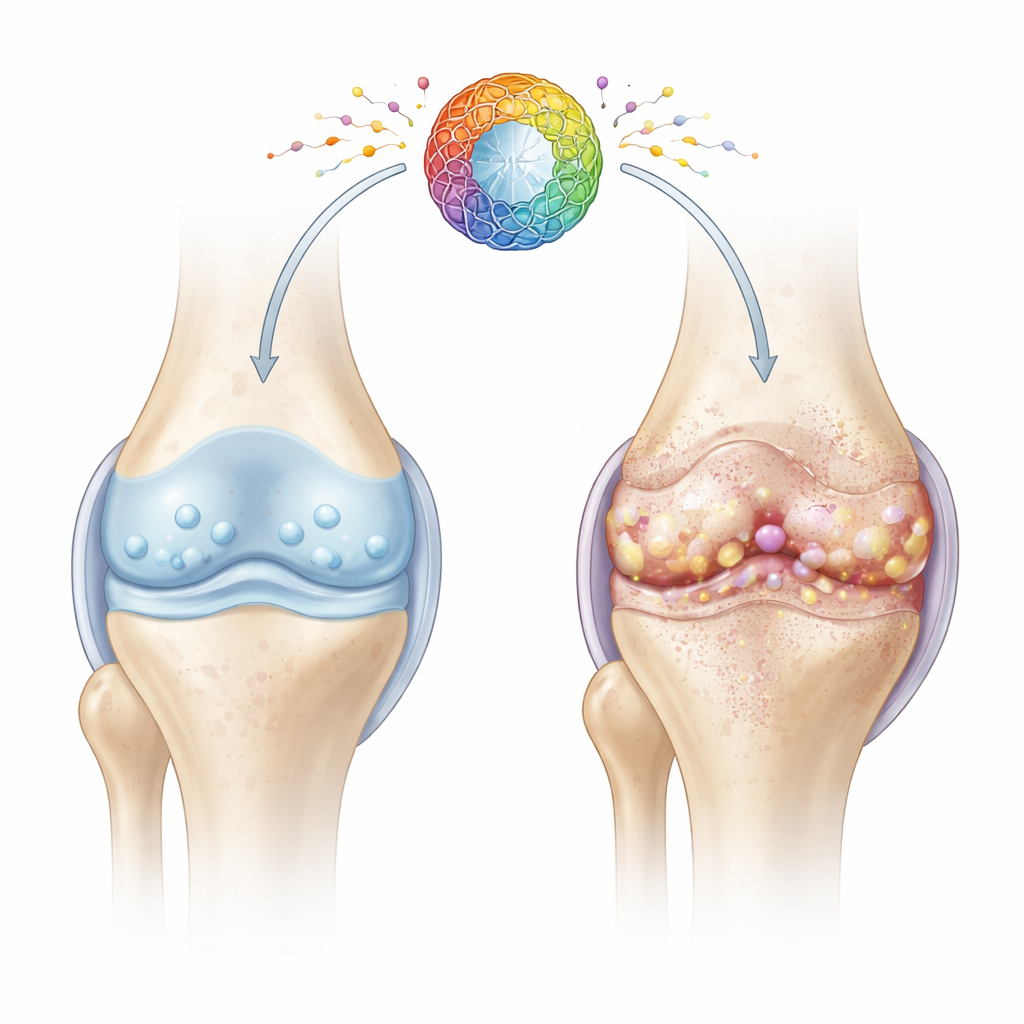
Una mirada más cercana a las células articulares fatigadas
El cartílago es el tejido liso y elástico que amortigua los extremos de los huesos. Su salud depende de los condrocitos, células especializadas que mantienen discretamente la matriz del cartílago durante décadas. Con la edad y las lesiones, muchos condrocitos entran en un estado llamado senescencia celular: dejan de dividirse, pierden su capacidad de reparación y liberan un cóctel de moléculas inflamatorias y dañinas para el tejido. Los autores se centraron en cómo los problemas en las fábricas de energía de las células—las mitocondrias—podrían impulsar este estado de envejecimiento perjudicial y acelerar la degeneración articular.
Una enzima vinculada al Parkinson aparece en articulaciones doloridas
Empleando datos públicos de expresión génica de cartílago humano, el equipo buscó genes asociados tanto con la osteoartritis como con el envejecimiento celular. Uno destacó: LRRK2, una enzima grande más conocida por su papel en la enfermedad de Parkinson hereditaria y en trastornos inflamatorios. Los niveles de LRRK2 eran notablemente más altos en el cartílago osteoartrítico en comparación con el tejido sano. En un modelo de ratas con osteoartritis de rodilla, LRRK2 también estaba elevado en el cartílago y en las células sinoviales. Cuando los investigadores aumentaron artificialmente LRRK2 en condrocitos de rata, cientos de otros genes cambiaron, especialmente los implicados en el envejecimiento celular y la señalización inflamatoria, lo que sugiere que LRRK2 no es solo un espectador sino un impulsor activo del proceso de la enfermedad.
Cómo las alarmas internas convierten el estrés en daño
El estudio se centró luego en un sistema de alarma molecular dentro de las células llamado vía cGAS–STING, que detecta ADN fuera de lugar en el citoplasma—una consecuencia frecuente del daño mitocondrial—y desencadena inflamación. Experimentos de laboratorio mostraron que el exceso de LRRK2 se une y activa esta vía en los condrocitos. La activación, a su vez, aumentó los niveles y alteró el comportamiento de HMGB1, una proteína que normalmente ayuda a organizar el ADN en el núcleo pero que puede actuar como una señal de peligro potente cuando se libera al entorno celular. Los condrocitos con LRRK2 alto mostraron mitocondrias hinchadas y disfuncionales, más especies reactivas de oxígeno (subproductos oxidativos dañinos), menor producción de energía y claros signos de senescencia. Bloquear STING, inhibir la actividad de LRRK2 o su función GTPasa atenuó HMGB1, alivió el estrés oxidativo y redujo los marcadores de envejecimiento en estas células.
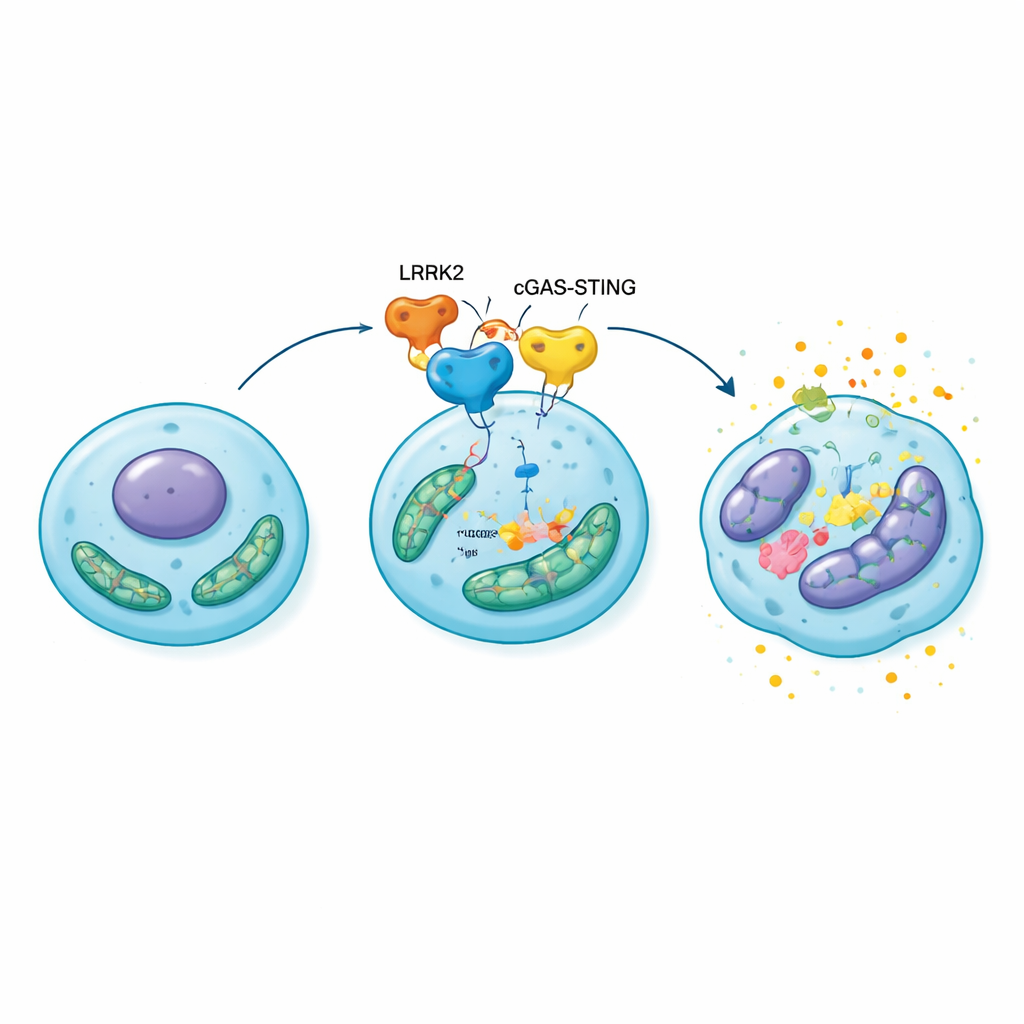
De células estresadas a cartílago que se desmorona
Para ver si esta cadena molecular importaba a nivel de la articulación completa, los investigadores sobreexpresaron LRRK2 directamente en las rodillas de ratas con osteoartritis inducida quirúrgicamente. En comparación con los animales control, estas ratas desarrollaron cartílago más delgado y erosionado, mayores cambios óseos debajo de la superficie articular y más condrocitos senescentes cargados de moléculas inflamatorias y degradadoras de la matriz. Cuando las mismas ratas fueron tratadas con un fármaco que bloquea STING, el daño articular y el envejecimiento celular se redujeron notablemente, y la función mitocondrial se recuperó parcialmente. Estos resultados sitúan la vía LRRK2–cGAS–STING–HMGB1 en el centro de un circuito autorreforzante: el estrés mitocondrial activa el sistema de alarma, que eleva HMGB1 y la inflamación, lo que a su vez profundiza la lesión mitocondrial y empuja a más condrocitos hacia la senescencia.
Qué significa esto para el cuidado futuro de las articulaciones
En términos sencillos, los autores muestran que LRRK2 actúa como un interruptor defectuoso que bloquea a las células del cartílago en un estado viejo y agotado y acelera la degradación del tejido articular. Al activar la red de alarma cGAS–STING–HMGB1, la alta actividad de LRRK2 vincula el estrés celular interno con la inflamación crónica y el daño estructural en la osteoartritis. Este trabajo sugiere que fármacos dirigidos a reducir LRRK2 o interrumpir la vía cGAS–STING podrían ayudar a mantener los condrocitos funcionales durante más tiempo, ralentizando potencialmente la progresión de la osteoartritis en lugar de limitarse a aliviar sus síntomas.
Cita: Zhang, Y., Zhu, Z., Ji, P. et al. cGAS-STING/HMGB1-mediated senescence induced by LRRK2 accelerates cartilage degeneration in osteoarthritis. Cell Death Dis 17, 377 (2026). https://doi.org/10.1038/s41419-026-08651-y
Palabras clave: degeneración osteocondral, senescencia celular, disfunción mitocondrial, señalización inflamatoria, vía LRRK2