Clear Sky Science · zh
急性髓性白血病中BCLAF1剪接的动态表观遗传调控
这对血液癌症意味着什么
急性髓性白血病(AML)是一种侵袭性的血液癌症,未成熟的白细胞异常增生并对多种治疗产生抵抗。本研究揭示了单个基因BCLAF1在白血病细胞内如何通过剪接被切割并产生不同版本——以及作用于细胞“表观遗传”开关的药物如何将这种剪接模式翻转回更接近正常、侵袭性更低的状态。理解这一隐藏的调控层可能开辟新途径,以驯服耐药性白血病,而无需完全依赖新的化疗药物。
同一基因的两个对立版本
BCLAF1是一种多功能蛋白,参与细胞凋亡、DNA修复和应激反应。该基因可以被剪接为全长形式和更短的形式,两者在分子功能上几乎相反。在AML细胞和患者样本中,作者发现明显偏向支持癌细胞生长的全长版本,而较为具有保护性的短版本相对不足。相比之下,在健康的造血干/祖细胞中,两种形式保持平衡。这种白血病特异性的偏向表明,全长BCLAF1既可能作为疾病标志物,也可能驱动恶性行为。
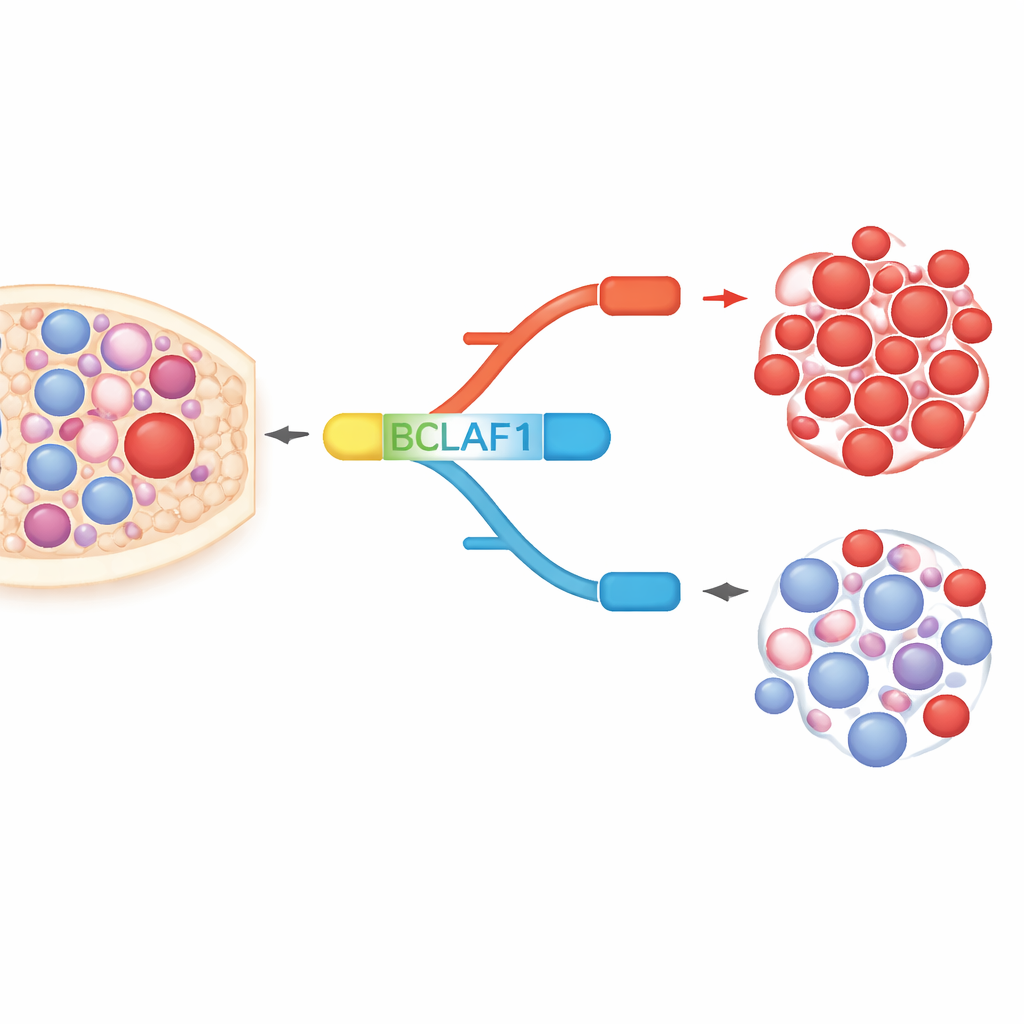
化学开关如何重塑剪接
研究团队接着探讨表观遗传药物——那些改变DNA包装和读取方式的化合物——是否能重置这种不平衡。他们用多种此类药物处理白血病细胞系,包括组蛋白去乙酰化酶抑制剂SAHA(沃利诺司他)和针对DNA甲基化的化合物。出现了明确模式:某些药物减少了全长BCLAF1形式并增加了短形式,而不影响其他BCLAF1变体。细致的染色质研究显示,在典型白血病状态下,两个酶DNMT3A和HDAC1驻留在BCLAF1基因的关键区域,维持一种有利于全长剪接的抑制性构象。SAHA处理松动了这种结构,去除了DNMT3A和HDAC1,增加了激活性组蛋白标记,并使另一个因子MRG15能够结合到外显子5,从而将剪接朝向短形式转变。
两个DNA甲基化酶,截然不同的角色
为了解相关酶DNMT3A和DNMT3B的作用,研究者构建了可特异性关闭每个酶的AML细胞系。敲低DNMT3A会减慢细胞生长,削弱HDAC1在BCLAF1基因上的结合,并推动剪接朝向更短、可能具有抑瘤作用的版本。DNMT3B的行为则截然不同:它在AML患者样本中实际上是减少的,当团队在细胞中进一步降低DNMT3B时,反而出人意料地增加了促进肿瘤的全长BCLAF1同工型。生化实验显示,DNMT3B能够直接与BCLAF1 RNA结合,而不仅仅与DNA结合,并且在SAHA处理或DNMT3A缺失后,它也能与短的RNA形式相互作用。综合来看,这些发现表明DNMT3A主要通过影响染色质结构来塑造BCLAF1剪接,而DNMT3B则通过与RNA本身相互作用对该过程进行微调。
产生后对BCLAF1的精细调控
故事并不在BCLAF1蛋白产生后就结束。作者还研究了翻译后加到BCLAF1上的化学标记——尤其是磷酸化——如何随表观遗传药物变化以及这如何影响蛋白在细胞内的定位。SAHA处理下,他们观察到特定位点的磷酸化发生变化,且BCLAF1在细胞核中或渗入胞质的分布也发生改变。大规模的蛋白组学和磷蛋白组学分析显示,SAHA广泛抑制了与细胞生长、DNA复制和RNA加工相关的通路,包括参与剪接的剪接体机制。这些数据支持这样一种观点:BCLAF1处于连接染色质状态、RNA剪接和细胞周期控制的枢纽位置。
对未来白血病治疗的意义
总体而言,研究揭示AML细胞利用表观遗传机制来偏向产生促进癌变的BCLAF1版本,同时压制更短、更具保护性的形式。通过干预如DNMT3A、HDAC1和DNMT3B等关键酶,表观遗传药物可以重新平衡这一剪接抉择并削弱白血病细胞的生存程序。对非专业读者而言,关键结论是:不仅基因的开关(开或关)重要,基因信息如何被编辑也至关重要。针对这些“编辑者”——而不是直接针对基因本身——可能成为恢复更健康基因使用模式并改善难治性AML患者结局的有力策略。
引用: Sgueglia, G., Massaro, C., Muro, A. et al. Dynamic epigenetic regulation of BCLAF1 splicing in acute myeloid leukemia. Cell Death Dis 17, 344 (2026). https://doi.org/10.1038/s41419-026-08594-4
关键词: 急性髓性白血病, 可变剪接, 表观遗传治疗, BCLAF1, DNMT3A