Clear Sky Science · pt
Regulação epigenética dinâmica do emaranhamento de BCLAF1 na leucemia mieloide aguda
Por que isso importa para o câncer do sangue
A leucemia mieloide aguda (LMA) é um câncer agressivo do sangue em que glóbulos brancos imaturos crescem descontroladamente e resistem a muitos tratamentos. Este estudo revela como um único gene, BCLAF1, é recortado e reorganizado em versões diferentes dentro das células leucêmicas — e como drogas que atuam sobre os “interruptores” epigenéticos da célula podem inverter esse padrão de splicing para um estado mais normal e menos agressivo. Compreender essa camada oculta de controle pode abrir novas vias para domar leucemias resistentes sem depender exclusivamente de quimioterápicos inteiramente novos.
Um gene, duas versões opostas
BCLAF1 é uma proteína multifuncional envolvida na morte celular, reparo do DNA e resposta ao estresse. O gene pode ser processado em uma forma de comprimento total e em uma forma mais curta, que se comportam quase como opostos moleculares. Em células de LMA e amostras de pacientes, os autores encontraram uma forte inclinação para a forma de comprimento total, que favorece o crescimento das células cancerosas, enquanto a forma mais curta, que parece mais protetora, está relativamente sub-representada. Em células-tronco e progenitoras sanguíneas saudáveis, por contraste, as duas formas são mantidas em equilíbrio. Esse viés específico da leucemia sugere que a versão de comprimento total de BCLAF1 pode servir tanto como marcador da doença quanto como motor do comportamento maligno.
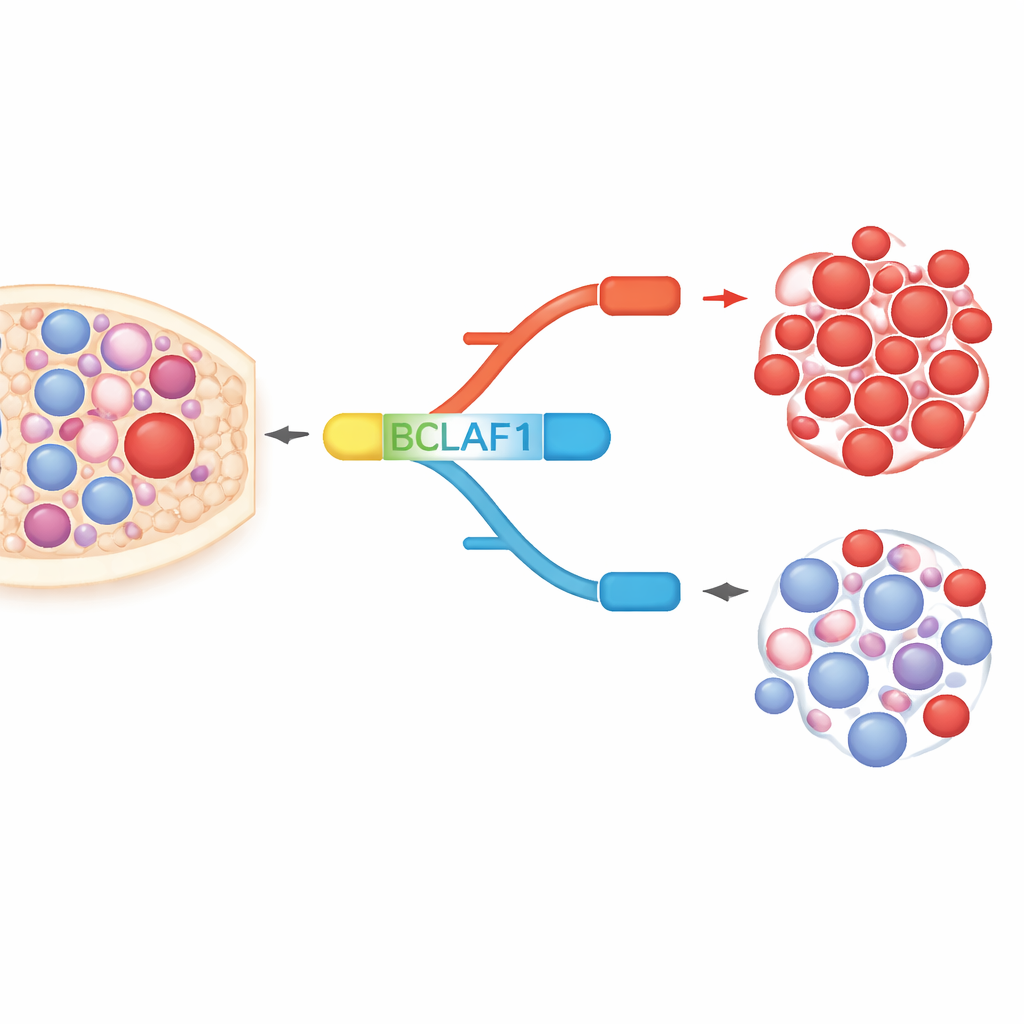
Como os interruptores químicos remodelam o splicing
A equipe então perguntou se drogas epigenéticas — compostos que modificam quão compactado o DNA está e como ele é lido — poderiam resetar esse desequilíbrio. Eles trataram linhagens leucêmicas com vários desses agentes, incluindo o inibidor de desacetilase de histonas SAHA (vorinostat) e compostos que atuam sobre a metilação do DNA. Um padrão claro emergiu: certos fármacos reduziram a forma de comprimento total de BCLAF1 e aumentaram a forma mais curta, sem afetar outras variantes de BCLAF1. Estudos detalhados de cromatina mostraram que, nas condições normais da leucemia, duas enzimas, DNMT3A e HDAC1, se posicionam em regiões-chave do gene BCLAF1 e ajudam a manter uma configuração repressiva que favorece o splice da forma de comprimento total. O tratamento com SAHA afrouxou essa estrutura, removeu DNMT3A e HDAC1, aumentou marcas de histonas ativadoras e permitiu que outro fator, MRG15, se ligasse ao exon 5, deslocando o splicing em direção à versão mais curta.
Duplas enzimáticas de metilação do DNA com papéis opostos
Para dissecar os papéis das enzimas relacionadas DNMT3A e DNMT3B, os pesquisadores criaram células de LMA nas quais cada enzima podia ser especificamente desligada. A redução de DNMT3A retardou o crescimento celular, enfraqueceu a ligação de HDAC1 no gene BCLAF1 e direcionou o splicing para a versão mais curta, provavelmente supressora de tumor. DNMT3B se comportou de forma muito diferente: está, na verdade, reduzida em amostras de pacientes com LMA, e quando a equipe diminuiu ainda mais DNMT3B nas células, isso inesperadamente aumentou o isoforma de comprimento total pró-câncer de BCLAF1. Ensaios bioquímicos revelaram que DNMT3B pode ligar-se diretamente ao RNA de BCLAF1 em vez de apenas ao DNA, e após o tratamento com SAHA ou perda de DNMT3A também se associa à forma de RNA curta. Em conjunto, esses achados sugerem que DNMT3A molda o splicing de BCLAF1 principalmente por meio da estrutura da cromatina, enquanto DNMT3B ajusta o processo ao interagir diretamente com o RNA.
Ajustando BCLAF1 após sua produção
A história não termina quando a proteína BCLAF1 é produzida. Os autores investigaram como marcas químicas adicionadas a BCLAF1 após a tradução — especialmente fosforilação — mudam em resposta a drogas epigenéticas e como isso afeta a localização da proteína na célula. Com o tratamento por SAHA, observaram alterações na fosforilação em sítios específicos e mudanças na distribuição entre núcleo e citoplasma. Análises proteômicas e fosfoproteômicas em grande escala mostraram que o SAHA atenua amplamente vias envolvidas em crescimento celular, replicação do DNA e processamento de RNA, incluindo a maquinaria do spliceossomo que ajuda a cortar e juntar RNAs. Esses dados sustentam a ideia de que BCLAF1 ocupa um ponto de interseção que liga estado da cromatina, splicing de RNA e controle do ciclo celular.
O que isso significa para terapias futuras contra a leucemia
No geral, o estudo revela que células de LMA exploram a maquinaria epigenética para favorecer uma versão de BCLAF1 que promove o câncer, enquanto suprimem uma forma mais curta e protetora. Ao interferir com enzimas-chave como DNMT3A, HDAC1 e DNMT3B, drogas epigenéticas podem reequilibrar essa decisão de splicing e enfraquecer os programas de sobrevivência das células leucêmicas. Para um observador leigo, a conclusão principal é que não apenas quais genes estão ligados ou desligados importa, mas também como a mensagem de cada gene é editada. Alvejar os editores — em vez do próprio gene — pode oferecer uma maneira poderosa de restaurar padrões mais saudáveis de uso gênico e melhorar os desfechos para pacientes com LMA de difícil tratamento.
Citação: Sgueglia, G., Massaro, C., Muro, A. et al. Dynamic epigenetic regulation of BCLAF1 splicing in acute myeloid leukemia. Cell Death Dis 17, 344 (2026). https://doi.org/10.1038/s41419-026-08594-4
Palavras-chave: leucemia mieloide aguda, splicing alternativo, terapia epigenética, BCLAF1, DNMT3A