Clear Sky Science · ar
التنظيم اللاجيني الديناميكي لقصّ BCLAF1 في اللوكيميا النخاعية الحادة
لماذا يهم هذا في سرطان الدم
اللوكيميا النخاعية الحادة (AML) هي سرطان دموي عدواني حيث تنمو خلايا الدم البيضاء غير الناضجة بشكل غير مسيطر عليه وتقاوم العديد من العلاجات. تكشف هذه الدراسة كيف يتم تقطيع جين واحد، BCLAF1، وإعادة تركيبه إلى نسخ مختلفة داخل خلايا اللوكيميا—وكيف أن أدوية تَستهدف مفاتيح "اللاجين" الخلوية يمكن أن تعيد نمط القَصّ هذا إلى حالة أكثر طبيعية وأقل عدوانية. فهم هذه الطبقة الخفيّة من الضبط قد يفتح طرقاً جديدة للسيطرة على اللوكيميات المقاومة دون الحاجة إلى عقاقير كيميائية جديدة تماماً.
جين واحد، نسختان متعارضتان
يعدّ BCLAF1 بروتينًا متعدد الوظائف يشارك في موت الخلية، وإصلاح الحمض النووي، والاستجابة للإجهاد. يمكن قصّ الجين إلى شكل كامل الطول وشكل أقصر، يتصرفان تقريبًا كأضداد جزيئية. في خلايا وعيّنات مرضى AML، وجد المؤلفون ميلًا قويًا نحو النسخة كاملة الطول التي تدعم نمو الخلية السرطانية، بينما النسخة الأقصر، التي تبدو أكثر حماية، كانت ممثلة بنسب أقل. في خلايا جذعية وسلفية دموية سليمة، بالمقابل، تُحفظ النسختان في توازن. يشير هذا الانحراف المتعلق باللوكيميا إلى أن النسخة كاملة الطول من BCLAF1 قد تعمل كعلامة للمرض وكمحرّك للسلوك الخبيث.
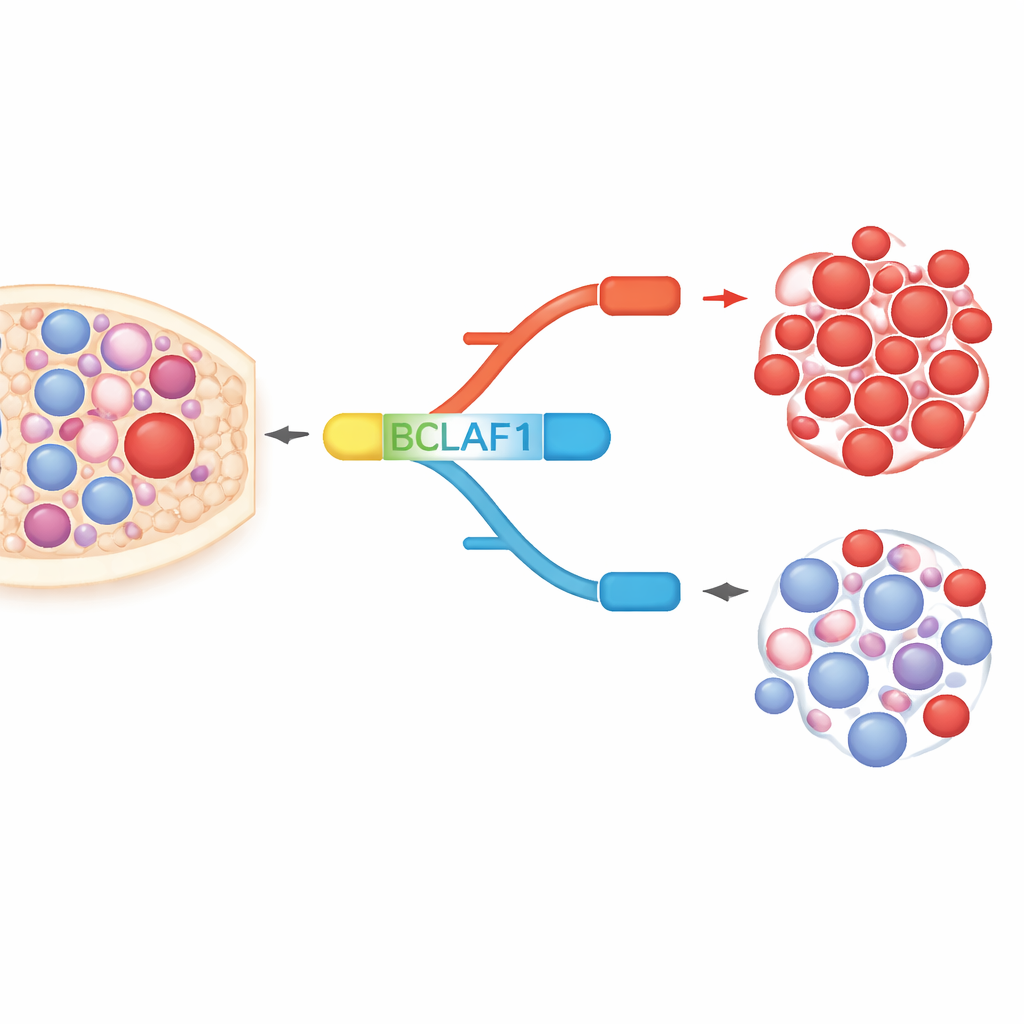
كيف تعيد المفاتيح الكيميائية تشكيل القَصّ
سأل الفريق بعد ذلك ما إذا كانت الأدوية اللاجينية—المركبات التي تعدّل كيفية ترتيب وقراءة الحمض النووي—يمكنها إعادة ضبط هذا الخلل. عالجوا خطوط خلايا اللوكيميا بعدة عوامل من هذا النوع، بما في ذلك مثبّط ديأسيتلاز الهيستون SAHA (فورينوستات) ومركبات تستهدف مثيلة الحمض النووي. ظهر نمط واضح: بعض الأدوية خفّضت النسخة كاملة الطول من BCLAF1 وزادت من النسخة الأقصر، دون أن تؤثر على متغيرات BCLAF1 الأخرى. أظهرت دراسات الكروماتين المفصّلة أنه في ظروف اللوكيميا الاعتيادية، تجلس إنزيمتان، DNMT3A وHDAC1، على مناطق مفتاحية من جين BCLAF1 وتساعدان في الحفاظ على تكوين قمعي يُفضّل القَصّ الكامل. أدى علاج SAHA إلى إرخاء هذا البناء، وإزاحة DNMT3A وHDAC1، وزيادة علامات هيستونية منشّطة، وسماح عامل آخر، MRG15، بالارتباط داخل الإكسون 5، مما حوّل القَصّ نحو النسخة الأقصر.
إنزيمان لمثيلة الحمض النووي، أدوار متعاكسة
لفكك أدوار الإنزيمين المرتبطين DNMT3A وDNMT3B، مهندس الباحثون خلايا AML يمكن فيها إيقاف كل إنزيم بشكل محدد. أدى تثبيط DNMT3A إلى إبطاء نمو الخلايا، وإضعاف ارتباط HDAC1 على جين BCLAF1، ودفع عملية القَصّ نحو النسخة الأقصر، التي يحتمل أن تكون مُكّونة مضادّة للورم. تصرّف DNMT3B بشكل مختلف تمامًا: فهو في الواقع منخفض في عينات مرضى AML، وعندما خفّض الفريق DNMT3B أكثر في الخلايا، زاد ذلك بشكل غير متوقع من النسخة كاملة الطول التي تُعزّز السرطان. كشفت تجارب بيوكيميائية أن DNMT3B يمكن أن يرتبط مباشرةً برنا BCLAF1 بدلاً من الارتباط بالحمض النووي فقط، وبعد علاج SAHA أو خسارة DNMT3A يشارك أيضًا مع شكل الرنا القصير. تقترح هذه النتائج معًا أن DNMT3A يشكل قَصّ BCLAF1 بشكل أساسي عبر بنية الكروماتين، بينما يقوم DNMT3B بضبط العملية بدقة عن طريق التفاعل مع الرنا ذاته.
ضبط BCLAF1 بعد تصنيعه
لا تنتهي القصة بمجرد إنتاج بروتين BCLAF1. بحث المؤلفون كيف تغيّر الشارات الكيميائية المضافة إلى BCLAF1 بعد الترجمة—وخاصة الفسفرة—استجابة للأدوية اللاجينية وكيف يؤثر ذلك على موضع البروتين داخل الخلية. مع علاج SAHA، لاحظوا تغيرات في الفسفرة عند مواقع محددة وتغيّرات في مدى تواجد BCLAF1 في النواة أو تسربه إلى السيتوبلازم. أظهرت تحليلات بروتيومية وفوسفوبروتيومية واسعة النطاق أن SAHA يخفف عمومًا المسارات المشاركة في نمو الخلايا وتضاعف الحمض النووي ومعالجة الرنا، بما في ذلك آلية المَسْلَخ (السبليسوسوم) التي تساعد في قطع وربط الرنا. تدعم هذه البيانات الفكرة أن BCLAF1 يقع عند مفترق يربط حالة الكروماتين، وقَصّ الرنا، والتحكم في دورة الخلية.
ما معنى هذا لعلاج اللوكيميا في المستقبل
بشكل عام، تكشف الدراسة أن خلايا AML تستغل الآلة اللاجينية لتفضيل نسخة BCLAF1 التي تعزز السرطان، بينما تكبح نسخة أقصر أكثر حماية. من خلال التدخل في إنزيمات رئيسية مثل DNMT3A وHDAC1 وDNMT3B، يمكن للأدوية اللاجينية إعادة توازن هذا القرار المتعلق بالقَصّ وإضعاف برامج بقاء خلايا اللوكيميا. للخارج العادي، الخلاصة الأساسية هي أن ليس فقط تشغيل الجينات أو إطفاؤها هو المهم، بل أيضًا كيف يُحرّر رسالة كل جين. قد يوفر استهداف المحرّرين—بدلًا من الجين نفسه—طريقة قوية لاستعادة أنماط استخدام جيني أكثر صحة وتحسين نتائج المرضى المصابين بـAML صعبة العلاج.
الاستشهاد: Sgueglia, G., Massaro, C., Muro, A. et al. Dynamic epigenetic regulation of BCLAF1 splicing in acute myeloid leukemia. Cell Death Dis 17, 344 (2026). https://doi.org/10.1038/s41419-026-08594-4
الكلمات المفتاحية: اللوكيميا النخاعية الحادة, القَصّ البديل, العلاج اللاجيني, BCLAF1, DNMT3A