Clear Sky Science · de
Dynamische epigenetische Regulation des Spleißens von BCLAF1 bei akuter myeloischer Leukämie
Warum das für Blutkrebs wichtig ist
Die akute myeloische Leukämie (AML) ist ein aggressiver Blutkrebs, bei dem unreife weiße Blutkörperchen unkontrolliert proliferieren und vielen Therapien widerstehen. Diese Studie zeigt, wie ein einzelnes Gen, BCLAF1, in Leukämiezellen in unterschiedliche Varianten „zusammengesetzt“ wird — und wie Wirkstoffe, die an den epigenetischen Schaltern der Zelle ansetzen, dieses Spleißmuster wieder in Richtung eines normaleren, weniger aggressiven Zustands kippen können. Das Verständnis dieser verborgenen Kontrollebene könnte neue Wege eröffnen, resistente Leukämien zu zähmen, ohne komplett neue Chemotherapien entwickeln zu müssen.
Ein Gen, zwei gegensätzliche Versionen
BCLAF1 ist ein vielseitiges Protein, das an programmiertem Zelltod, DNA-Reparatur und Stressantwort beteiligt ist. Das Gen kann in eine vollständige Form und eine kürzere Form gespleißt werden, die sich nahezu wie molekulare Gegenspieler verhalten. In AML-Zelllinien und Patientenproben fanden die Autoren eine starke Verschiebung zugunsten der vollständigen Variante, die das Krebszellwachstum unterstützt, während die kürzere, offenbar schützende Variante relativ unterrepräsentiert ist. In gesunden hämatopoetischen Stamm- und Vorläuferzellen dagegen halten sich beide Formen die Waage. Diese leukämiespezifische Schieflage deutet darauf hin, dass die vollständige BCLAF1‑Version sowohl als Krankheitsmarker als auch als Treiber malignen Verhaltens dienen könnte.
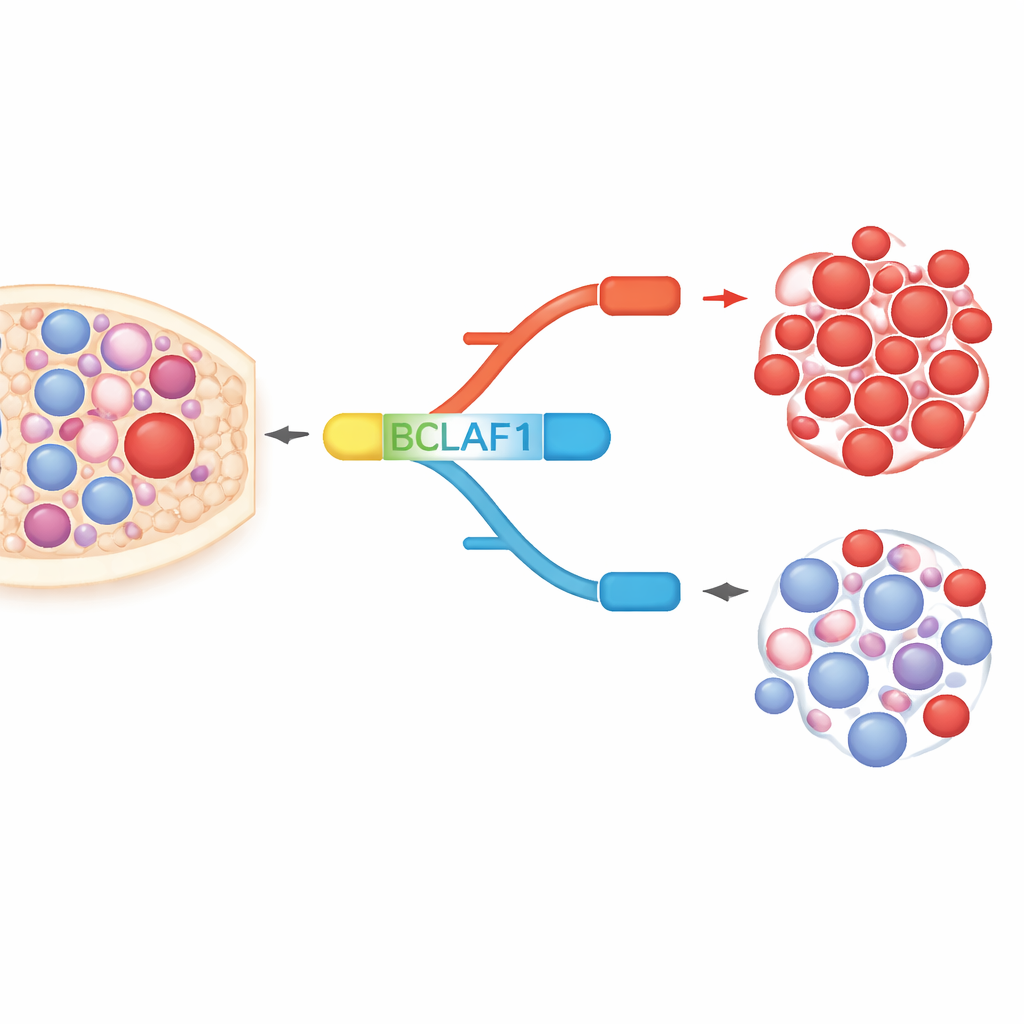
Wie chemische Schalter das Spleißen umgestalten
Das Team prüfte anschließend, ob epigenetische Arzneistoffe — Verbindungen, die beeinflussen, wie eng DNA verpackt und abgelesen wird — dieses Ungleichgewicht zurücksetzen können. Sie behandelten Leukämiezelllinien mit mehreren solchen Wirkstoffen, darunter dem Histondeacetylase-Inhibitor SAHA (Vorinostat) und Substanzen, die die DNA‑Methylierung ansprechen. Es zeichnete sich ein klares Muster ab: Bestimmte Mittel reduzierten die vollständige BCLAF1‑Form und steigerten die kurze Form, ohne andere BCLAF1‑Varianten zu beeinflussen. Detaillierte Chromatin‑Analysen zeigten, dass unter den üblichen Leukämiebedingungen zwei Enzyme, DNMT3A und HDAC1, auf Schlüsselregionen des BCLAF1‑Gens sitzen und eine repressive Konfiguration aufrechterhalten, die das vollständige Spleißen begünstigt. Die Behandlung mit SAHA lockerte diese Struktur, entfernte DNMT3A und HDAC1, erhöhte aktivierende Histonmarken und ermöglichte einem weiteren Faktor, MRG15, an Exon 5 zu binden, wodurch das Spleißen zugunsten der kürzeren Variante verschoben wurde.
Zwei DNA‑Methylierungsenzyme, gegensätzliche Rollen
Um die Rollen der verwandten Enzyme DNMT3A und DNMT3B zu entschlüsseln, konstruierten die Forscher AML‑Zellen, in denen jedes Enzym gezielt ausgeschaltet werden konnte. Die Herunterregulierung von DNMT3A verlangsamte das Zellwachstum, schwächte die HDAC1‑Bindung am BCLAF1‑Gen und trieb das Spleißen in Richtung der kürzeren, vermutlich tumorsuppressiven Variante. DNMT3B verhielt sich sehr unterschiedlich: Es ist in AML‑Patientenproben tatsächlich reduziert, und wenn das Team DNMT3B weiter verringerte, erhöhte dies unerwartet die krebsfördernde vollständige BCLAF1‑Isoform. Biochemische Assays zeigten, dass DNMT3B direkt an BCLAF1‑RNA binden kann und sich nach SAHA‑Behandlung oder Verlust von DNMT3A auch mit der kurzen RNA‑Form verbindet. Zusammengenommen deuten diese Befunde darauf hin, dass DNMT3A das BCLAF1‑Spleißen hauptsächlich über Chromatinstruktur steuert, während DNMT3B den Prozess durch direkte RNA‑Interaktion feinjustiert.
Feinabstimmung von BCLAF1 nach der Proteinsynthese
Die Geschichte endet nicht, sobald BCLAF1‑Protein gebildet ist. Die Autoren untersuchten, wie chemische Markierungen an BCLAF1 nach der Translation — insbesondere Phosphorylierung — als Reaktion auf epigenetische Wirkstoffe verändert werden und wie das die zelluläre Lokalisation des Proteins beeinflusst. Unter SAHA‑Behandlung beobachteten sie Änderungen der Phosphorylierung an bestimmten Stellen sowie Verschiebungen darin, ob BCLAF1 im Zellkern verbleibt oder ins Zytoplasma gelangt. groß angelegte proteomische und Phosphoproteom‑Analysen zeigten, dass SAHA breit Wege dämpft, die an Zellwachstum, DNA‑Replikation und RNA‑Verarbeitung beteiligt sind, einschließlich des Spleißosoms, das RNAs schneidet und verknüpft. Diese Daten stützen die Idee, dass BCLAF1 an einer Schnittstelle steht, die Chromatinstatus, RNA‑Spleißen und Zellzykluskontrolle verbindet.
Was das für künftige Leukämiebehandlungen bedeutet
Insgesamt zeigt die Studie, dass AML‑Zellen epigenetische Maschinerie ausnutzen, um eine krebsfördernde Version von BCLAF1 zu bevorzugen und gleichzeitig eine kürzere, schützende Form zu unterdrücken. Durch Eingreifen in Schlüsselenzyme wie DNMT3A, HDAC1 und DNMT3B können epigenetische Medikamente diese Spleißentscheidung wieder ins Gleichgewicht bringen und die Überlebensprogramme der Leukämiezellen schwächen. Für eine allgemein interessierte Leserschaft lautet die zentrale Botschaft: Nicht nur, welche Gene an oder aus sind, ist wichtig, sondern auch, wie die Botschaften eines Gens nachbearbeitet werden. Die Editoren dieser Botschaften zu adressieren — statt nur das Gen selbst — könnte einen wirkungsvollen Weg bieten, gesündere Gennutzungsmuster wiederherzustellen und die Ergebnisse für Patienten mit schwer behandelbarer AML zu verbessern.
Zitation: Sgueglia, G., Massaro, C., Muro, A. et al. Dynamic epigenetic regulation of BCLAF1 splicing in acute myeloid leukemia. Cell Death Dis 17, 344 (2026). https://doi.org/10.1038/s41419-026-08594-4
Schlüsselwörter: akute myeloische Leukämie, alternatives Spleißen, epigenetische Therapie, BCLAF1, DNMT3A