Clear Sky Science · ru
Динамическая эпигенетическая регуляция сплайсинга BCLAF1 при остром миелоидном лейкозе
Почему это важно для заболеваний крови
Острый миелоидный лейкоз (ОМЛ) — агрессивный рак крови, при котором незрелые лейкоциты бесконтрольно размножаются и устойчивы ко многим методам лечения. В этом исследовании показано, как один ген, BCLAF1, в клетках лейкоза перерабатывается в разные версии посредством сплайсинга — и как препараты, влияющие на «эпигенетические» переключатели клетки, могут вернуть этот паттерн сплайсинга к более нормальному, менее агрессивному состоянию. Понимание этого скрытого уровня регуляции может открыть новые способы сдерживания резистентных форм лейкоза без разработки полностью новых химиотерапевтических средств.
Один ген, две противоположные версии
BCLAF1 — многофункциональный белок, участвующий в программируемой гибели клеток, ремонте ДНК и ответе на стресс. Ген может сплайсироваться в полноразмерную форму и укороченную форму, которые по функциям почти противоположны. В клетках ОМЛ и в образцах пациентов исследователи обнаружили сильный сдвиг в сторону полноразмерной версии, поддерживающей рост раковых клеток, тогда как укороченная версия, выглядящая более защитной, относительно недопредставлена. У здоровых гемопоэтических стволовых и предшественниковых клеток, напротив, эти две формы находятся в равновесии. Этот специфичный для лейкоза перекос указывает на то, что полноразмерная версия BCLAF1 может служить маркером заболевания и драйвером злокачественного поведения.
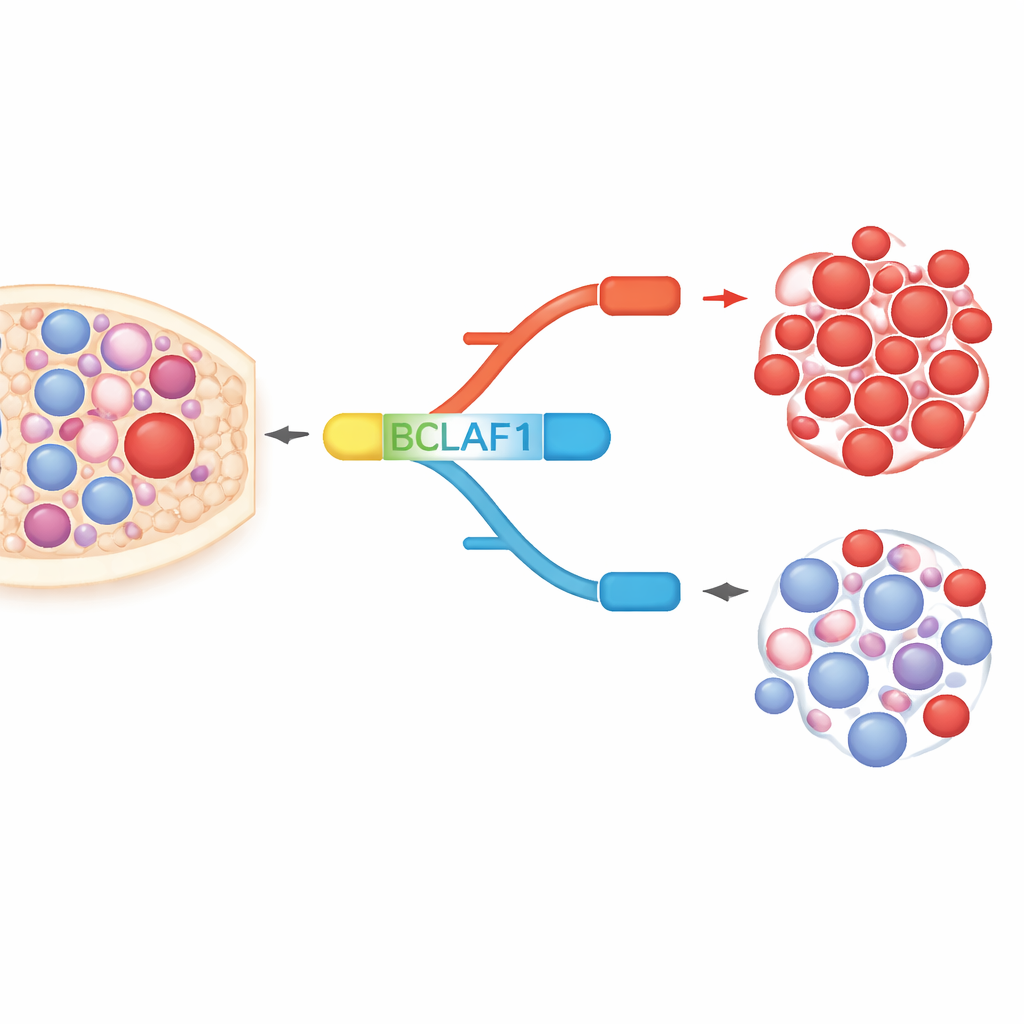
Как химические переключатели меняют сплайсинг
Затем команда спросила, могут ли эпигенетические препараты — соединения, модифицирующие упаковку ДНК и её считывание — восстановить этот дисбаланс. Они обработали линии лейкозных клеток несколькими такими агентами, включая ингибитор гистоновых деацетилаз SAHA (вориностат) и соединения, нацеленные на метилирование ДНК. Проявился ясный паттерн: некоторые препараты уменьшали долю полноразмерного BCLAF1 и усиливали укороченную форму, не влияя на другие варианты BCLAF1. Детальные исследования хроматина показали, что при типичных условиях лейкоза две ферменты, DNMT3A и HDAC1, локализуются на ключевых участках гена BCLAF1 и поддерживают репрессивную конфигурацию, благоприятную для полноразмерного сплайсинга. Лечение SAHA разрыхляло эту структуру, удаляло DNMT3A и HDAC1, увеличивало активирующие гистоновые метки и позволило фактору MRG15 связаться внутри экзона 5, сдвигая сплайсинг в сторону укороченной версии.
Две ферменты метилирования ДНК — противоположные роли
Чтобы разобраться в ролях родственных ферментов DNMT3A и DNMT3B, исследователи создали клетки ОМЛ, в которых каждую ферменту можно было избирательно выключать. Понижение экспрессии DNMT3A замедляло рост клеток, ослабляло связывание HDAC1 на гене BCLAF1 и сдвигало сплайсинг в сторону укороченной, вероятно опухолесдерживающей формы. DNMT3B вел себя иначе: его уровень действительно снижён в образцах пациентов с ОМЛ, и при дальнейшем уменьшении DNMT3B в клетках это неожиданно усиливало онкогенную полноразмерную изоформу BCLAF1. Биохимические анализы показали, что DNMT3B может напрямую связываться с РНК BCLAF1, а не только с ДНК, и после лечения SAHA или потери DNMT3A он также взаимодействует с короткой РНК-формой. В совокупности эти данные указывают, что DNMT3A формирует сплайсинг BCLAF1 главным образом через структуру хроматина, тогда как DNMT3B донастраивает процесс через взаимодействие с самой РНК.
Тонкая настройка BCLAF1 после синтеза
История не заканчивается после синтеза белка BCLAF1. Авторы исследовали, как химические метки, добавляемые к BCLAF1 посттрансляционно — в особенности фосфорилирование — меняются в ответ на эпигенетические препараты и как это влияет на локализацию белка в клетке. При лечении SAHA наблюдались изменения фосфорилирования в конкретных сайтах и сдвиги в распределении BCLAF1 между ядром и цитоплазмой. Масштабные протеомные и фосфопротеомные анализы показали, что SAHA в целом ослабляет пути, связанные с ростом клеток, репликацией ДНК и обработкой РНК, включая сплайсосому — машинерию, которая вырезает и соединяет РНК. Эти данные поддерживают идею о том, что BCLAF1 находится на перекрёстке, связывая состояние хроматина, сплайсинг РНК и контроль клеточного цикла.
Что это значит для будущей терапии лейкоза
В целом исследование показывает, что клетки ОМЛ используют эпигенетический аппарат, чтобы предпочитать онкогенную версию BCLAF1 и подавлять укороченную, более защитную форму. Вмешательство в ключевые ферменты, такие как DNMT3A, HDAC1 и DNMT3B, с помощью эпигенетических препаратов может уравновесить это сплайсинговое решение и ослабить программы выживания лейкозных клеток. Для непрофессионального читателя главный вывод таков: важно не только то, какие гены включены или выключены, но и как именно сообщение каждого гена редактируется. Нацеливание на «редакторов» — а не на сам ген — может дать мощный способ восстановить более здоровые закономерности использования генов и улучшить исходы у пациентов с трудноизлечимым ОМЛ.
Цитирование: Sgueglia, G., Massaro, C., Muro, A. et al. Dynamic epigenetic regulation of BCLAF1 splicing in acute myeloid leukemia. Cell Death Dis 17, 344 (2026). https://doi.org/10.1038/s41419-026-08594-4
Ключевые слова: острый миелоидный лейкоз, альтернативный сплайсинг, эпигенетическая терапия, BCLAF1, DNMT3A