Clear Sky Science · it
Regolazione epigenetica dinamica dello splicing di BCLAF1 nella leucemia mieloide acuta
Perché è importante per i tumori del sangue
La leucemia mieloide acuta (LMA) è un tumore del sangue aggressivo in cui cellule bianche immature proliferano in modo incontrollato e resistono a molti trattamenti. Questo studio rivela come un singolo gene, BCLAF1, venga tagliato e ricombinato in versioni diverse all’interno delle cellule leucemiche — e come farmaci che agiscono sugli interruttori «epigenetici» della cellula possano ribaltare questo schema di splicing verso uno stato più normale e meno aggressivo. Comprendere questo livello nascosto di controllo potrebbe aprire nuove strade per domare le leucemie resistenti senza dover sviluppare completamente nuovi chemioterapici.
Un gene, due versioni opposte
BCLAF1 è una proteina multitasking coinvolta nell’apoptosi, nella riparazione del DNA e nella risposta allo stress. Il gene può essere splicingato in una forma a lunghezza piena e in una forma più corta, che si comportano quasi come opposti molecolari. Nelle cellule di LMA e nei campioni dei pazienti, gli autori hanno riscontrato un marcato sbilanciamento verso la versione a lunghezza piena, che sostiene la crescita delle cellule tumorali, mentre la versione corta, che sembra più protettiva, è relativamente poco rappresentata. Nelle cellule staminali e progenitrici del sangue sane, invece, le due forme sono mantenute in equilibrio. Questo squilibrio specifico della leucemia suggerisce che la versione a lunghezza piena di BCLAF1 potrebbe funzionare sia da marcatore della malattia sia da driver del comportamento maligno.
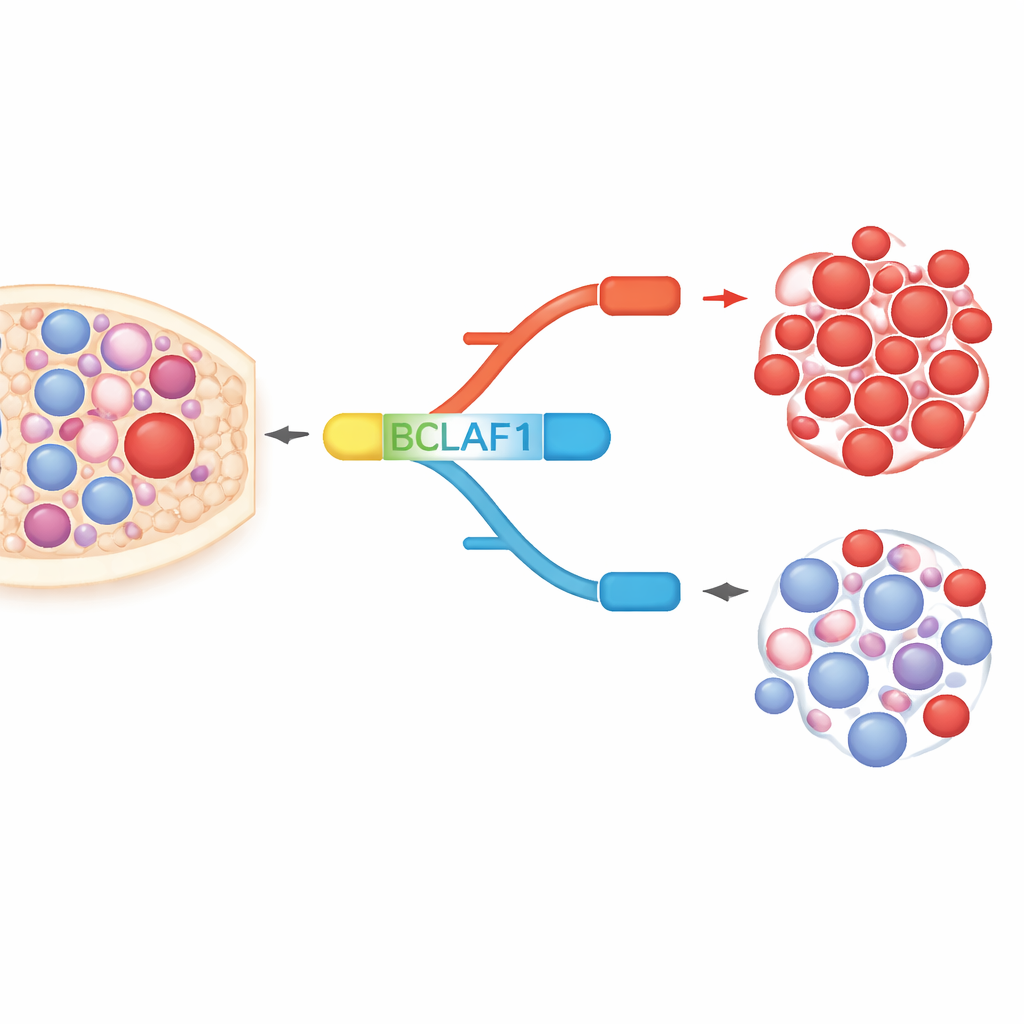
Come gli interruttori chimici rimodellano lo splicing
Il gruppo ha quindi indagato se i farmaci epigenetici — composti che modificano quanto strettamente il DNA è impacchettato e letto — potessero riequilibrare questo sbilanciamento. Hanno trattato linee cellulari leucemiche con diversi di questi agenti, incluso l’inibitore delle deacetilasi istoniche SAHA (vorinostat) e composti che mirano alla metilazione del DNA. È emerso un chiaro schema: certi farmaci riducono la forma a lunghezza piena di BCLAF1 e aumentano la forma più corta, senza alterare altri varianti di BCLAF1. Studi cromatinici dettagliati hanno mostrato che, nelle condizioni tipiche della LMA, due enzimi, DNMT3A e HDAC1, si posizionano su regioni chiave del gene BCLAF1 e contribuiscono a mantenere una configurazione repressiva che favorisce lo splicing verso la versione a lunghezza piena. Il trattamento con SAHA ha allentato questa struttura, rimosso DNMT3A e HDAC1, aumentato i marcatori istonici attivanti e permesso a un altro fattore, MRG15, di legarsi all’interno dell’esone 5, spostando lo splicing verso la versione più corta.
Due enzimi della metilazione del DNA, ruoli opposti
Per scomporre i ruoli degli enzimi correlati DNMT3A e DNMT3B, i ricercatori hanno ingegnerizzato cellule di LMA in cui ciascun enzima poteva essere specificamente spento. L’abbassamento di DNMT3A rallentava la crescita cellulare, indeboliva il legame di HDAC1 sul gene BCLAF1 e spingeva lo splicing verso la versione più corta, presumibilmente oncosoppressiva. DNMT3B si comportava in modo molto diverso: è infatti ridotto nei campioni di pazienti con LMA e, quando il team ha ulteriormente diminuito DNMT3B nelle cellule, questo ha inaspettatamente aumentato l’isoforma a lunghezza piena che favorisce il cancro. Saggi biochimici hanno rivelato che DNMT3B può legarsi direttamente all’RNA di BCLAF1 invece che solo al DNA, e dopo il trattamento con SAHA o la perdita di DNMT3A si impegna anche con la forma corta dell’RNA. Complessivamente, questi risultati suggeriscono che DNMT3A modella lo splicing di BCLAF1 principalmente attraverso la struttura della cromatina, mentre DNMT3B affina il processo interagendo direttamente con l’RNA.
Regolazione fine di BCLAF1 dopo la sintesi
La storia non finisce una volta che la proteina BCLAF1 è prodotta. Gli autori hanno investigato come i tag chimici aggiunti a BCLAF1 dopo la traduzione — in particolare la fosforilazione — cambino in risposta ai farmaci epigenetici e come questo influenzi la localizzazione della proteina nella cellula. Con il trattamento SAHA hanno osservato cambiamenti nella fosforilazione in siti specifici e variazioni nella presenza di BCLAF1 nel nucleo o nella fuoriuscita nel citoplasma. Analisi proteomiche e fosfoproteomiche su larga scala hanno mostrato che SAHA attenua in modo esteso le vie coinvolte nella crescita cellulare, nella replicazione del DNA e nell’elaborazione dell’RNA, incluso il macchinario dello spliceosoma che aiuta a tagliare e unire gli RNA. Questi dati supportano l’idea che BCLAF1 stia a un crocevia che collega lo stato della cromatina, lo splicing dell’RNA e il controllo del ciclo cellulare.
Cosa significa per la terapia futura della leucemia
Nel complesso, lo studio rivela che le cellule di LMA sfruttano il macchinario epigenetico per favorire una versione di BCLAF1 che promuove il cancro, sopprimendo nel contempo una forma più corta e protettiva. Interferendo con enzimi chiave come DNMT3A, HDAC1 e DNMT3B, i farmaci epigenetici possono riequilibrare questa decisione di splicing e indebolire i programmi di sopravvivenza delle cellule leucemiche. Per il lettore non specialistico, il punto chiave è che non conta solo se un gene è attivo o spento, ma anche come il messaggio di ciascun gene viene modificato. Mirare agli «editori» — piuttosto che al gene stesso — potrebbe offrire un modo potente per ripristinare schemi di utilizzo genico più sani e migliorare gli esiti per i pazienti con LMA difficili da trattare.
Citazione: Sgueglia, G., Massaro, C., Muro, A. et al. Dynamic epigenetic regulation of BCLAF1 splicing in acute myeloid leukemia. Cell Death Dis 17, 344 (2026). https://doi.org/10.1038/s41419-026-08594-4
Parole chiave: leucemia mieloide acuta, splicing alternativo, terapia epigenetica, BCLAF1, DNMT3A