Clear Sky Science · pl
Dynamiczna epigenetyczna regulacja splicingu BCLAF1 w ostrym białaczku szpikowym
Dlaczego to ma znaczenie dla nowotworów krwi
Ostra białaczka szpikowa (AML) to agresywny nowotwór krwi, w którym niedojrzałe białe krwinki rozmnażają się bez kontroli i bywają odporne na wiele terapii. W tym badaniu wykazano, jak pojedynczy gen, BCLAF1, jest składany w komórkach białaczkowych w różne warianty — oraz jak leki oddziałujące na „epigenetyczne” przełączniki komórkowe mogą odwrócić ten wzorzec splicingu w stronę bardziej normalnego, mniej agresywnego stanu. Zrozumienie tej ukrytej warstwy regulacji może otworzyć nowe drogi do ujarzmienia opornych białaczek bez konieczności opracowywania zupełnie nowych chemioterapeutyków.
Jeden gen, dwie przeciwstawne formy
BCLAF1 to białko o wielu funkcjach, zaangażowane w apoptozę, naprawę DNA i reakcję na stres. Gen może być splicowany do formy pełnej długości oraz krótszej formy, które zachowują się niemal jak molekularne przeciwieństwa. W komórkach AML i próbkach pacjentów autorzy zaobserwowali wyraźne przesunięcie w stronę formy pełnej długości, która wspiera wzrost komórek nowotworowych, podczas gdy krótsza, pozornie bardziej ochronna forma, jest relatywnie niedoreprezentowana. Dla porównania, w zdrowych komórkach macierzystych i progenitorowych krwi obie formy są utrzymywane w równowadze. Ten specyficzny dla białaczki przesyt sugeruje, że forma pełnej długości BCLAF1 może pełnić rolę zarówno markera choroby, jak i czynnika napędzającego złośliwe zachowanie.
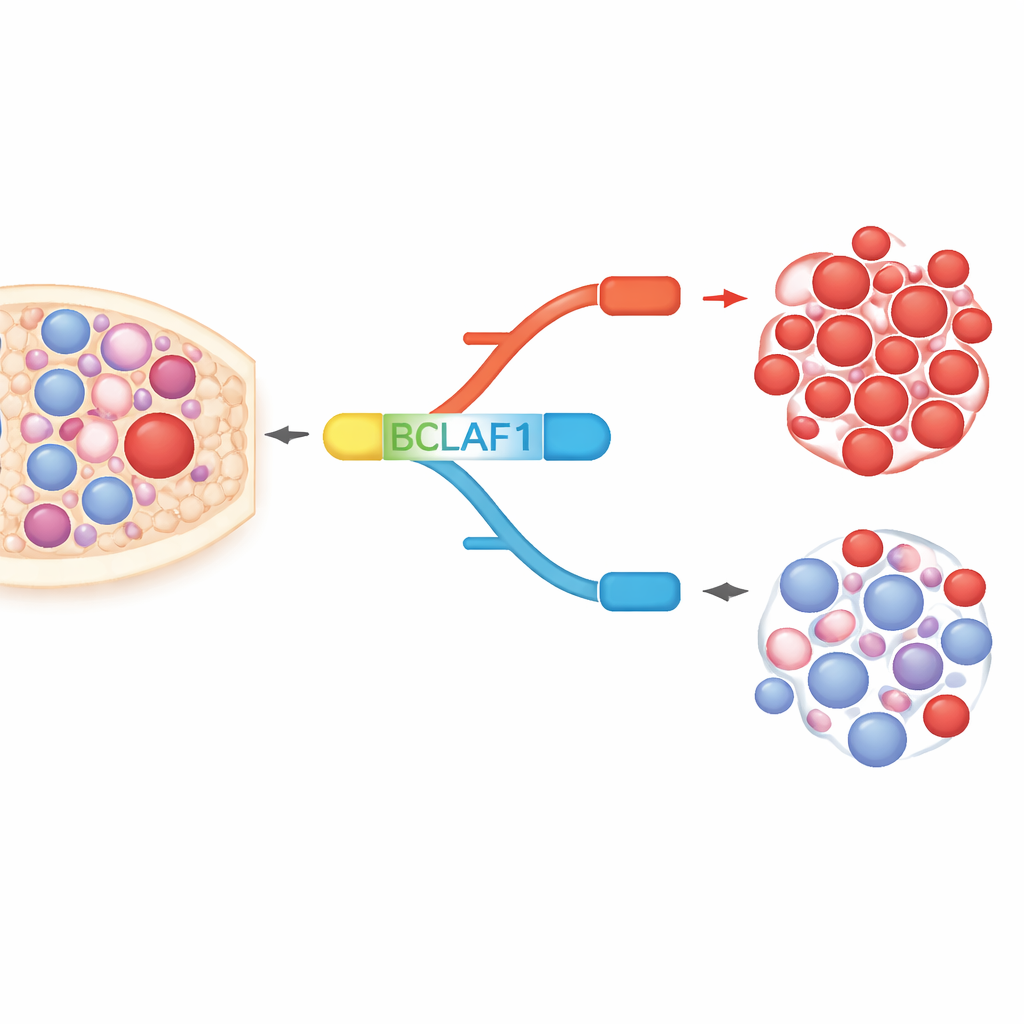
Jak chemiczne przełączniki kształtują splicing
Zespół zadał następnie pytanie, czy leki epigenetyczne — związki modyfikujące sposób pakowania i odczytu DNA — mogą przywrócić równowagę. Leczyli linie komórkowe białaczki kilkoma takimi środkami, w tym inhibitorem deacetylaz histonowych SAHA (worinostat) oraz związkami celującymi metylację DNA. Wyłonił się wyraźny wzorzec: niektóre leki zmniejszały ilość formy pełnej długości BCLAF1 i zwiększały udział formy krótszej, nie wpływając na inne warianty BCLAF1. Szczegółowe analizy chromatyny wykazały, że w warunkach typowych dla białaczki dwa enzymy, DNMT3A i HDAC1, lokalizują się w kluczowych regionach genu BCLAF1 i pomagają utrzymać represyjną konfigurację sprzyjającą splicingowi w stronę formy pełnej. Leczenie SAHA rozluźniało tę strukturę, usuwało DNMT3A i HDAC1, zwiększało aktywujące markery histonowe i pozwalało czynnikowi MRG15 związać się w obrębie eksonu 5, przesuwając splicing w kierunku formy krótszej.
Dwa enzymy metylacji DNA, przeciwne role
Aby rozróżnić role powiązanych enzymów DNMT3A i DNMT3B, badacze przygotowali komórki AML, w których można było specyficznie wyłączyć każdy z nich. Upośledzenie DNMT3A spowalniało wzrost komórek, osłabiało wiązanie HDAC1 z genem BCLAF1 i przesuwało splicing w stronę krótszej, prawdopodobnie supresorowej formy. DNMT3B zachowywał się bardzo inaczej: jest w rzeczywistości obniżony w próbkach pacjentów z AML, a dalsze zmniejszenie DNMT3B w komórkach niespodziewanie zwiększało promującą nowotwór formę pełnej długości BCLAF1. Testy biochemiczne wykazały, że DNMT3B może wiązać się bezpośrednio z RNA BCLAF1, a nie tylko z DNA, i po leczeniu SAHA lub utracie DNMT3A wiąże się też z krótką formą RNA. Wspólnie te obserwacje sugerują, że DNMT3A kształtuje splicing BCLAF1 głównie przez strukturę chromatyny, podczas gdy DNMT3B dopracowuje ten proces poprzez interakcję z samym RNA.
Dostrajanianie BCLAF1 po jego wytworzeniu
Opowieść nie kończy się w momencie powstania białka BCLAF1. Autorzy zbadali, jak chemiczne modyfikacje dodawane do BCLAF1 po translacji — szczególnie fosforylacja — zmieniają się w odpowiedzi na leki epigenetyczne i jak wpływają na lokalizację białka w komórce. Po leczeniu SAHA zaobserwowano przesunięcia w fosforylacji na określonych miejscach oraz zmiany w tym, czy BCLAF1 pozostaje w jądrze, czy przemieszcza się do cytoplazmy. Analizy proteomiczne i fosfoproteomiczne na dużą skalę wykazały, że SAHA szeroko tłumi szlaki zaangażowane w wzrost komórek, replikację DNA i przetwarzanie RNA, w tym maszynerię spliceosomu, która pomaga przecinać i łączyć RNA. Dane te wspierają tezę, że BCLAF1 leży na styku łączącym stan chromatyny, splicing RNA i kontrolę cyklu komórkowego.
Co to oznacza dla przyszłej terapii białaczki
Podsumowując, badanie ujawnia, że komórki AML wykorzystują maszynerię epigenetyczną, by faworyzować formę BCLAF1 sprzyjającą nowotworowi, jednocześnie tłumiąc krótszą, bardziej ochronną formę. Przez ingerencję w kluczowe enzymy takie jak DNMT3A, HDAC1 i DNMT3B, leki epigenetyczne mogą przywrócić równowagę tego wyboru splicingu i osłabić programy przetrwania komórek białaczkowych. Dla obserwatora niebędącego specjalistą kluczowy wniosek jest taki, że nie tylko to, które geny są włączone lub wyłączone, ma znaczenie, ale także to, jak każda wiadomość genowa jest edytowana. Celowanie w redaktorów — zamiast w sam gen — może zaoferować silny sposób przywracania zdrowszych wzorców wykorzystania genów i poprawy wyników u pacjentów z trudnym do leczenia AML.
Cytowanie: Sgueglia, G., Massaro, C., Muro, A. et al. Dynamic epigenetic regulation of BCLAF1 splicing in acute myeloid leukemia. Cell Death Dis 17, 344 (2026). https://doi.org/10.1038/s41419-026-08594-4
Słowa kluczowe: ostra białaczka szpikowa, alternatywny splicing, terapia epigenetyczna, BCLAF1, DNMT3A