Clear Sky Science · tr
Akut miyeloid lösemide BCLAF1 kesilmesinin dinamik epigenetik düzenlenmesi
Kanser için bunun önemi
Akut miyeloid lösemi (AML), olgunlaşmamış beyaz kan hücrelerinin kontrolsüz şekilde çoğaldığı ve birçok tedaviye direnç gösterdiği agresif bir kan kanseridir. Bu çalışma, tek bir gen olan BCLAF1’in lösemi hücrelerinde farklı versiyonlara nasıl kesilip yapıştırıldığını ve hücrenin “epigenetik” anahtarlarına etki eden ilaçların bu kesilme desenini daha normal, daha az agresif bir yöne nasıl çevirebildiğini ortaya koyuyor. Bu gizli kontrol katmanını anlamak, tamamen yeni kemoterapi ilaçlarına ihtiyaç duymadan dirençli lösemileri dizginlemenin yeni yollarını açabilir.
Tek gen, zıt iki versiyon
BCLAF1, hücre ölümü, DNA onarımı ve strese yanıt gibi görevlerde çok yönlü bir proteindir. Gen, tam uzunlukta bir form ve daha kısa bir form olarak kesilebiliyor; bu iki form moleküler açıdan neredeyse zıt davranıyor. AML hücrelerinde ve hasta örneklerinde araştırmacılar, kanser hücresi büyümesini destekleyen tam uzunluklu versiyona belirgin bir eğilim olduğunu, daha koruyucu görünen kısa versiyonun ise görece az temsil edildiğini buldular. Buna karşılık sağlıklı kan kök ve progenitor hücrelerinde iki form dengede tutuluyor. Bu lösemiye özgü dengesizlik, tam uzunluklu BCLAF1 versiyonunun hem hastalığın bir belirteci hem de kötü huylu davranışın sürücüsü olabileceğini düşündürüyor.
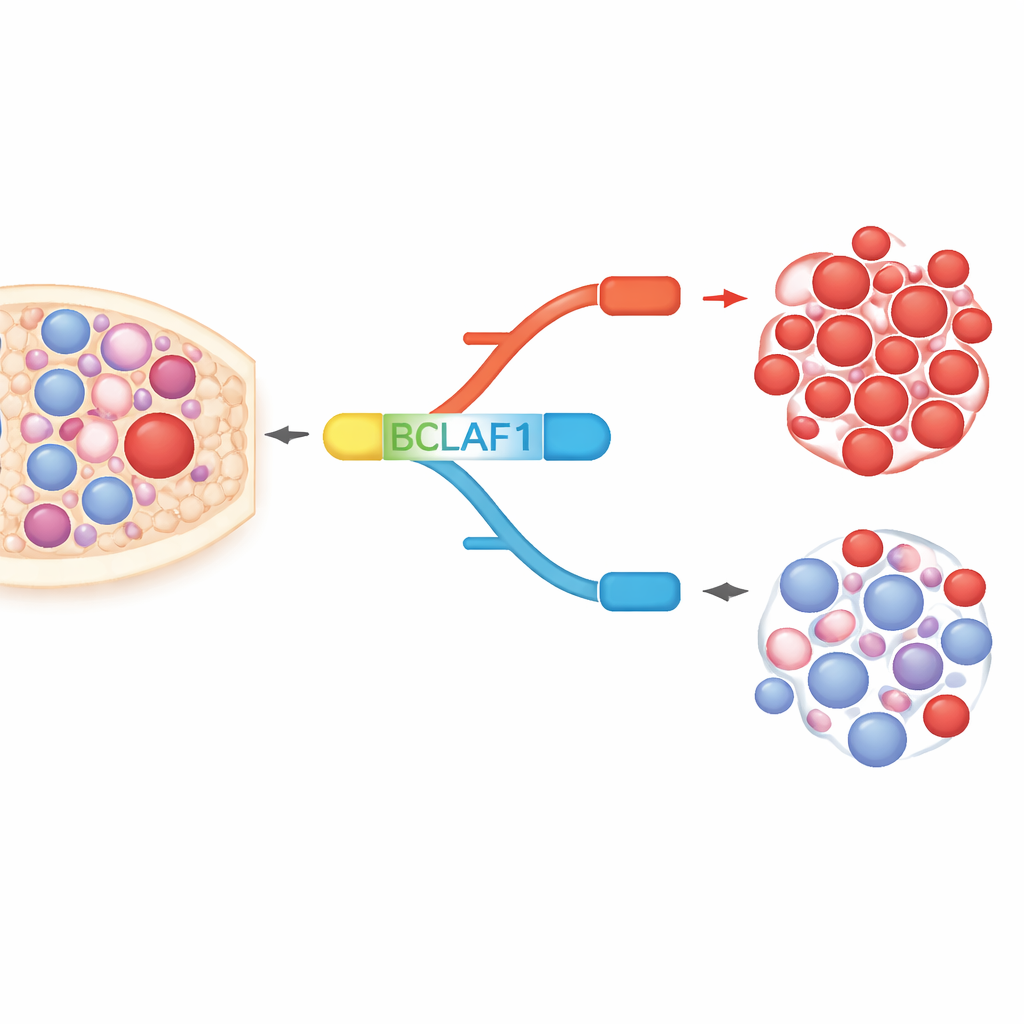
Kimyasal anahtarlar kesilmeyi nasıl yeniden şekillendiriyor
Araştırma ekibi daha sonra epigenetik ilaçlar—DNA’nın ne kadar sıkı paketlendiğini ve nasıl okunacağını değiştiren bileşikler—bu dengesizliği sıfırlayıp sıfırlayamayacağını sordu. Lösemi hücre hatlarını, histon deasetilaz inhibitörü SAHA (vorinostat) ve DNA metilasyonunu hedefleyen bileşikler dahil birkaç ajanla tedavi ettiler. Net bir desen ortaya çıktı: belirli ilaçlar tam uzunluklu BCLAF1 formunu azalttı ve diğer BCLAF1 varyantlarını etkilemeden kısa formu artırdı. Ayrıntılı kromatin çalışmaları, normal lösemi koşullarında DNMT3A ve HDAC1 adlı iki enzimin BCLAF1 geninin anahtar bölgelerine yerleşip tam uzunluklu splicing’i destekleyen baskılayıcı bir yapı sürdürdüğünü gösterdi. SAHA tedavisi bu yapıyı gevşetti, DNMT3A ve HDAC1’i uzaklaştırdı, etkinleştirici histon işaretlerini artırdı ve MRG15 adlı başka bir faktörün ekson 5 içinde bağlanmasına izin vererek kesilmeyi daha kısa form lehine kaydırdı.
İki DNA metilasyon enzimi, zıt roller
İlgili enzimler DNMT3A ve DNMT3B’nin rollerini ayrıştırmak için araştırmacılar her enzimin özel olarak kapatılabildiği mühendislenmiş AML hücreleri yarattılar. DNMT3A’nın baskılanması hücre büyümesini yavaşlattı, BCLAF1 genindeki HDAC1 bağlanmasını zayıflattı ve kesilmeyi muhtemelen tümör baskılayıcı olan daha kısa versiyon yönünde sürükledi. DNMT3B çok farklı davrandı: AML hasta örneklerinde aslında azalmış durumdaydı ve ekip hücrelerde DNMT3B’yi daha da azalttığında bu beklenmedik şekilde kanseri teşvik eden tam uzunluklu BCLAF1 izoformunu artırdı. Biyokimyasal testler DNMT3B’nin sadece DNA’ya değil doğrudan BCLAF1 RNA’sına bağlanabildiğini ve SAHA tedavisi veya DNMT3A kaybı sonrasında kısa RNA formuyla da etkileşime girdiğini ortaya koydu. Birlikte ele alındığında bu bulgular DNMT3A’nın BCLAF1 kesilmesini ağırlıklı olarak kromatin yapısı yoluyla şekillendirdiğini, DNMT3B’nin ise süreci RNA ile etkileşerek ince ayarladığını öneriyor.
Üretildikten sonra BCLAF1’in ince ayarı
BCLAF1 proteini üretildikten sonra hikâye bitmiyor. Yazarlar, özellikle fosforilasyon olmak üzere translasyon sonrası BCLAF1’e eklenen kimyasal etiketlerin epigenetik ilaçlara nasıl yanıt verdiğini ve bunun proteinin hücre içindeki konumunu nasıl etkilediğini incelediler. SAHA tedavisi ile belirli bölgelerde fosforilasyonda değişimler ve BCLAF1’in nükleusta kalıp kalmaması veya sitoplazmaya sızıp sızmaması yönünde kaymalar gözlemlediler. Büyük ölçekli proteomik ve fosfoproteomik analizler SAHA’nın hücre büyümesi, DNA replikasyonu ve RNA işlemeyi içeren yolları ve RNA’ları kesip birleştiren spliceozom makinesini geniş çapta baskıladığını gösterdi. Bu veriler, BCLAF1’in kromatin durumu, RNA kesilmesi ve hücre döngüsü kontrolünü birbirine bağlayan bir kavşakta yer aldığı fikrini destekliyor.
Geleceğin lösemi tedavisi için anlamı
Genel olarak çalışma, AML hücrelerinin epigenetik mekanizmayı kanserleştiren bir BCLAF1 versiyonunu desteklemek ve daha kısa, koruyucu bir formu baskılamak için kullandığını ortaya koyuyor. DNMT3A, HDAC1 ve DNMT3B gibi kilit enzimlere müdahale eden epigenetik ilaçlar bu splicing kararını yeniden dengeleyebilir ve lösemi hücresi hayatta kalma programlarını zayıflatabilir. Bir okuyucu için temel çıkarım, hangi genlerin açık veya kapalı olduğunun önemli olmasının ötesinde, her genin mesajının nasıl düzenlendiğinin de önemli olduğudur. Düzenleyicileri—genin kendisini değil—hedeflemek, daha sağlıklı gen kullanımı desenlerini geri getirmek ve zor tedavi edilen AML hastalarında sonuçları iyileştirmek için güçlü bir yol sunabilir.
Atıf: Sgueglia, G., Massaro, C., Muro, A. et al. Dynamic epigenetic regulation of BCLAF1 splicing in acute myeloid leukemia. Cell Death Dis 17, 344 (2026). https://doi.org/10.1038/s41419-026-08594-4
Anahtar kelimeler: akut miyeloid lösemi, alternatif kesilme (splicing), epigenetik tedavi, BCLAF1, DNMT3A