Clear Sky Science · nl
Dynamische epigenetische regulatie van BCLAF1-splicing bij acute myeloïde leukemie
Waarom dit belangrijk is voor bloedkanker
Acute myeloïde leukemie (AML) is een agressieve bloedkanker waarbij onrijpe witte bloedcellen ongecontroleerd groeien en veel behandelingen weerstaan. Deze studie onthult hoe één gen, BCLAF1, in leukemiecellen in verschillende versies wordt geknipt en geplakt — en hoe medicijnen die werken op de epigenetische schakelaars van de cel dit splicingpatroon weer kunnen terugzetten naar een meer normale, minder agressieve toestand. Inzicht in deze verborgen regellaag kan nieuwe manieren openen om resistente leukemieën te temmen zonder geheel nieuwe chemotherapieën te hoeven ontwikkelen.
Één gen, twee tegengestelde versies
BCLAF1 is een multifunctioneel eiwit betrokken bij celdood, DNA-herstel en stressreacties. Het gen kan worden gespliced tot een volledige, lange vorm en een kortere vorm, die zich bijna als moleculaire tegenpolen gedragen. In AML-cellen en patiëntmonsters vonden de auteurs een sterke voorkeur voor de volledige vorm, die de groei van kankercellen ondersteunt, terwijl de kortere vorm, die meer beschermend lijkt, relatief ondervertegenwoordigd is. In gezonde bloedstam- en voorlopercellen daarentegen zijn de twee vormen in balans. Deze leukemie-specifieke scheefstand suggereert dat de volledige BCLAF1-vorm zowel als markeerder van de ziekte als als motor van kwaadaardig gedrag kan fungeren.
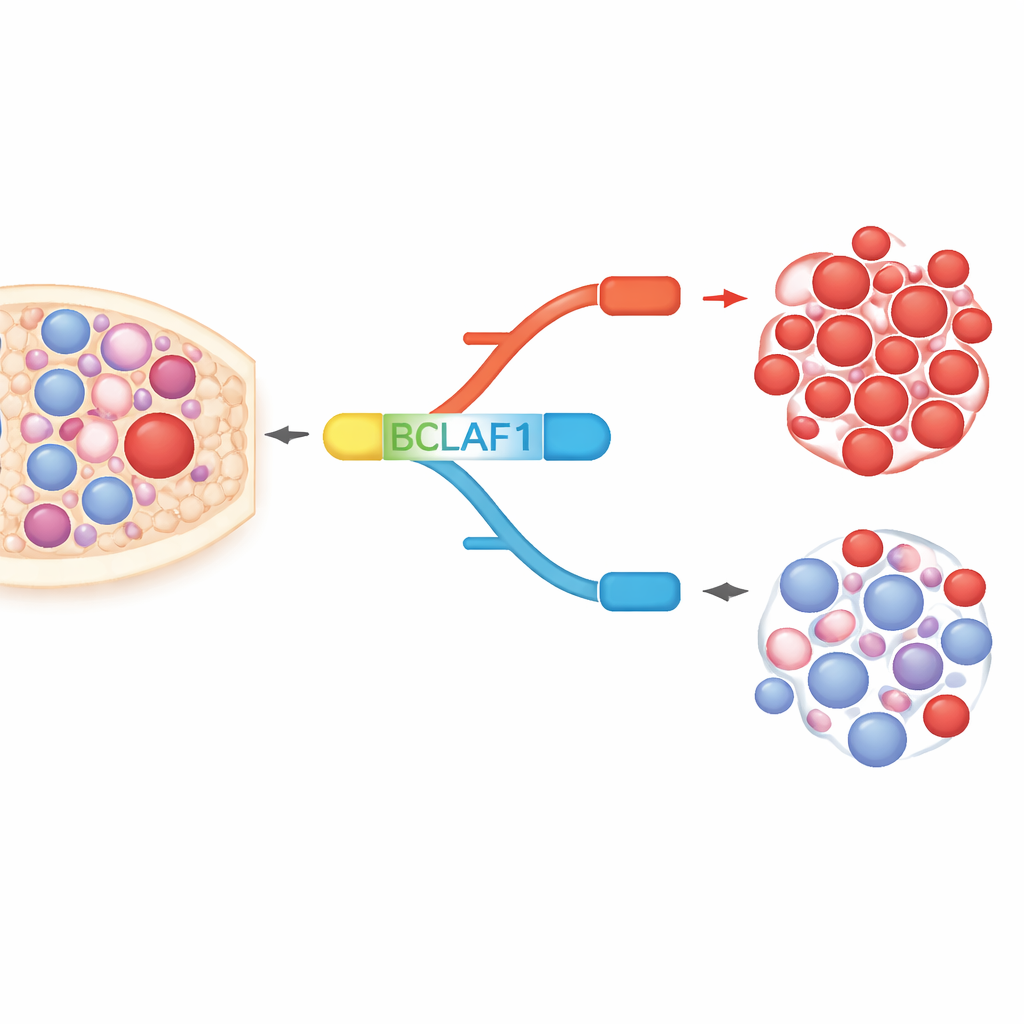
Hoe chemische schakelaars splicing herschikken
Het team vroeg zich vervolgens af of epigenetische geneesmiddelen — verbindingen die beïnvloeden hoe strak DNA is verpakt en afgelezen wordt — dit onevenwicht konden herstellen. Ze behandelden leukemiecellen lijnen met verschillende van zulke middelen, waaronder de histon-deacetylaseremmer SAHA (vorinostat) en middelen gericht op DNA-methylatie. Een duidelijk patroon verscheen: bepaalde medicijnen verminderden de volledige BCLAF1-vorm en verhoogden de kortere vorm, zonder andere BCLAF1-varianten te beïnvloeden. Gedetailleerde chromatine-studies toonden aan dat onder normale leukemische omstandigheden twee enzymen, DNMT3A en HDAC1, op sleutelregio’s van het BCLAF1-gen zitten en een repressieve configuratie in stand houden die de volledige splice bevordert. SAHA-behandeling versoepelde deze structuur, verwijderde DNMT3A en HDAC1, verhoogde activerende histonmerken en stond een andere factor, MRG15, toe om binnen exon 5 te binden, waardoor splicing naar de kortere versie verschuift.
Twee DNA-methylatie-enzymen, tegengestelde rollen
Om de rollen van verwante enzymen DNMT3A en DNMT3B uit te splitsen, ontwikkelden de onderzoekers AML-cellen waarin elk enzym specifiek uitgeschakeld kon worden. Het terugschakelen van DNMT3A vertraagde de celgroei, verzwakte HDAC1-binding op het BCLAF1-gen en stuurde splicing naar de kortere, waarschijnlijk tumorsupressieve versie. DNMT3B gedroeg zich heel anders: het is juist verminderd in AML-patiëntenmonsters, en wanneer het team DNMT3B verder verminderde in cellen, nam onverwacht de kankerversterkende volledige BCLAF1-isoform toe. Biochemische assays toonden dat DNMT3B direct kan binden aan BCLAF1-RNA in plaats van alleen aan DNA, en na SAHA-behandeling of verlies van DNMT3A gaat het ook in interactie met de korte RNA-vorm. Gezamenlijk suggereren deze bevindingen dat DNMT3A BCLAF1-splicing vooral via chromatinestructuur beïnvloedt, terwijl DNMT3B het proces fijn afstemt door met het RNA zelf te interageren.
Fijnregeling van BCLAF1 nadat het gemaakt is
Het verhaal eindigt niet zodra het BCLAF1-eiwit is geproduceerd. De auteurs onderzochten hoe chemische tags die aan BCLAF1 na translatie worden toegevoegd — vooral fosforylering — veranderen als reactie op epigenetische medicijnen en hoe dit de locatie van het eiwit in de cel beïnvloedt. Bij SAHA-behandeling observeerden ze verschuivingen in fosforylering op specifieke sites en veranderingen in of BCLAF1 in de kern bleef zitten of in het cytoplasma lekte. Grootschalige proteomische en fosfoproteomische analyses lieten zien dat SAHA breedweg paden dempt die betrokken zijn bij celgroei, DNA-replicatie en RNA-verwerking, inclusief het spliceosoommachinery dat helpt RNA’s knippen en verbinden. Deze gegevens ondersteunen het idee dat BCLAF1 op een kruispunt zit dat chromatine-status, RNA-splicing en celcycluscontrole verbindt.
Wat dit betekent voor toekomstige leukemietherapie
Samengevat onthult de studie dat AML-cellen epigenetische machines exploiteren om een kankerversterkende versie van BCLAF1 te bevoordelen, terwijl een kortere, meer beschermende vorm wordt onderdrukt. Door in te grijpen op sleutelenzymen zoals DNMT3A, HDAC1 en DNMT3B, kunnen epigenetische medicijnen deze splicingbeslissing in evenwicht brengen en de overlevingsprogramma’s van leukemiecellen verzwakken. Voor de niet-specialist is de belangrijkste conclusie dat niet alleen het aan- of uitstaan van genen van belang is, maar ook hoe het bericht van elk gen wordt bewerkt. Het richten op de redacteuren — in plaats van op het gen zelf — kan een krachtige manier bieden om gezondere patronen van gengebruik te herstellen en de uitkomsten voor patiënten met moeilijk behandelbare AML te verbeteren.
Bronvermelding: Sgueglia, G., Massaro, C., Muro, A. et al. Dynamic epigenetic regulation of BCLAF1 splicing in acute myeloid leukemia. Cell Death Dis 17, 344 (2026). https://doi.org/10.1038/s41419-026-08594-4
Trefwoorden: acute myeloïde leukemie, alternatieve splicing, epigenetische therapie, BCLAF1, DNMT3A