Clear Sky Science · es
Regulación epigenética dinámica del empalme de BCLAF1 en la leucemia mieloide aguda
Por qué importa esto para el cáncer de la sangre
La leucemia mieloide aguda (LMA) es un cáncer sanguíneo agresivo en el que las células blancas inmaduras proliferan sin control y resisten muchos tratamientos. Este estudio revela cómo un único gen, BCLAF1, se corta y recompone en versiones diferentes dentro de las células leucémicas—y cómo fármacos que actúan sobre los interruptores “epigenéticos” de la célula pueden invertir este patrón de empalme hacia un estado más normal y menos agresivo. Comprender esta capa oculta de control podría abrir nuevas vías para domar las leucemias resistentes sin necesidad de desarrollar por completo fármacos de quimioterapia nuevos.
Un gen, dos versiones opuestas
BCLAF1 es una proteína multifuncional implicada en la muerte celular, la reparación del ADN y la respuesta al estrés. El gen puede empalmarse en una forma de longitud completa y en una forma más corta, que se comportan casi como opuestos moleculares. En líneas celulares de LMA y en muestras de pacientes, los autores encontraron una marcada inclinación hacia la versión de longitud completa, que favorece el crecimiento de las células cancerosas, mientras que la versión corta, que parece más protectora, está relativamente subrepresentada. En células madre y progenitoras sanguíneas sanas, en cambio, las dos formas se mantienen en equilibrio. Este sesgo específico de la leucemia sugiere que la versión de longitud completa de BCLAF1 podría servir tanto como marcador de la enfermedad como impulsor del comportamiento maligno.
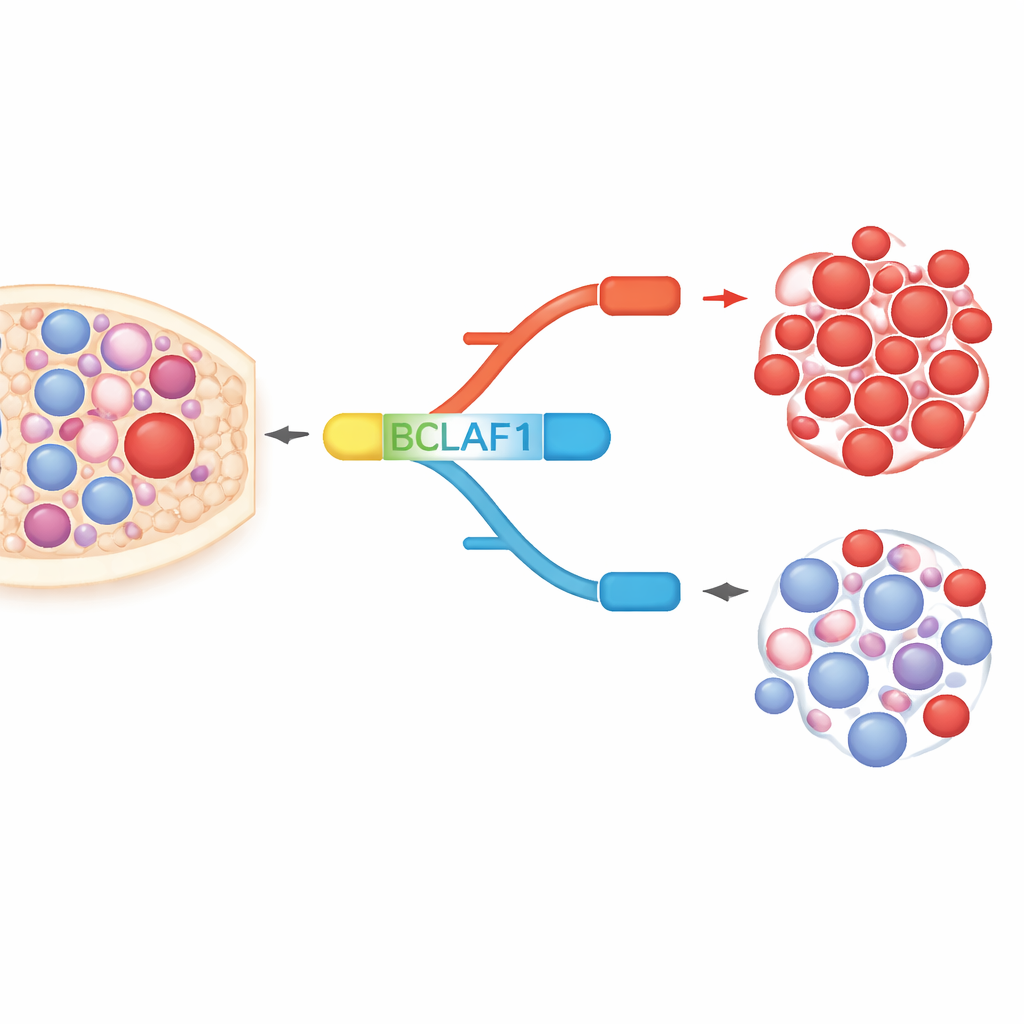
Cómo los interruptores químicos remodelan el empalme
El equipo se preguntó si los fármacos epigenéticos—compuestos que modifican cuán compactado y leído está el ADN—podían restablecer este desequilibrio. Trataron líneas celulares leucémicas con varios de estos agentes, incluido el inhibidor de histona deacetilasa SAHA (vorinostat) y compuestos dirigidos a la metilación del ADN. Surgió un patrón claro: ciertos fármacos redujeron la forma de longitud completa de BCLAF1 y aumentaron la forma corta, sin afectar otras variantes de BCLAF1. Estudios detallados de cromatina mostraron que, en condiciones leucémicas normales, dos enzimas, DNMT3A y HDAC1, se sitúan en regiones clave del gen BCLAF1 y ayudan a mantener una configuración represora que favorece el empalme hacia la forma de longitud completa. El tratamiento con SAHA aflojó esta estructura, eliminó DNMT3A y HDAC1, aumentó marcas de histonas activadoras y permitió que otro factor, MRG15, se uniera dentro del exón 5, desplazando el empalme hacia la versión corta.
Dos enzimas de metilación del ADN, roles opuestos
Para dilucidar los papeles de las enzimas relacionadas DNMT3A y DNMT3B, los investigadores diseñaron células de LMA en las que cada enzima podía apagarse específicamente. La reducción de DNMT3A ralentizó el crecimiento celular, debilitó la unión de HDAC1 en el gen BCLAF1 y dirigió el empalme hacia la versión corta, probablemente supresora tumoral. DNMT3B se comportó de forma muy diferente: en muestras de pacientes con LMA está, de hecho, reducida, y cuando el equipo disminuyó aún más DNMT3B en células, esto aumentó de manera inesperada la isoforma de longitud completa de BCLAF1 que promueve el cáncer. Ensayos bioquímicos revelaron que DNMT3B puede unirse directamente al ARN de BCLAF1 en lugar de solo al ADN, y tras el tratamiento con SAHA o la pérdida de DNMT3A también se asocia con la forma corta del ARN. En conjunto, estos hallazgos sugieren que DNMT3A modela el empalme de BCLAF1 principalmente a través de la estructura de la cromatina, mientras que DNMT3B ajusta finamente el proceso interactuando con el ARN mismo.
Afinando BCLAF1 después de su producción
La historia no termina una vez que se produce la proteína BCLAF1. Los autores investigaron cómo las etiquetas químicas añadidas a BCLAF1 tras la traducción—especialmente la fosforilación—cambian en respuesta a fármacos epigenéticos y cómo esto afecta la localización de la proteína en la célula. Con el tratamiento de SAHA, observaron cambios en la fosforilación en sitios específicos y variaciones en si BCLAF1 permanecía en el núcleo o se filtraba al citoplasma. Análisis proteómicos y fosfoproteómicos a gran escala mostraron que SAHA atenúa de forma amplia las vías implicadas en el crecimiento celular, la replicación del ADN y el procesamiento del ARN, incluida la maquinaria del spliceosoma que ayuda a cortar y unir ARN. Estos datos apoyan la idea de que BCLAF1 se sitúa en un cruce que vincula el estado de la cromatina, el empalme del ARN y el control del ciclo celular.
Qué significa esto para futuras terapias de la leucemia
En general, el estudio revela que las células de LMA explotan la maquinaria epigenética para favorecer una versión de BCLAF1 que promueve el cáncer, mientras suprimen una forma más corta y protectora. Al interferir con enzimas clave como DNMT3A, HDAC1 y DNMT3B, los fármacos epigenéticos pueden reequilibrar esta decisión de empalme y debilitar los programas de supervivencia de las células leucémicas. Para un lector no especializado, la conclusión principal es que no solo importa qué genes están activos o inactivos, sino también cómo se edita el mensaje de cada gen. Dirigirse a los editores—más que al propio gen—puede ofrecer una forma potente de restaurar patrones de uso génico más saludables y mejorar los resultados en pacientes con LMA de difícil tratamiento.
Cita: Sgueglia, G., Massaro, C., Muro, A. et al. Dynamic epigenetic regulation of BCLAF1 splicing in acute myeloid leukemia. Cell Death Dis 17, 344 (2026). https://doi.org/10.1038/s41419-026-08594-4
Palabras clave: leucemia mieloide aguda, splicing alternativo, terapia epigenética, BCLAF1, DNMT3A