Clear Sky Science · fr
Régulation épigénétique dynamique de l’épissage de BCLAF1 dans la leucémie myéloblastique aiguë
Pourquoi c’est important pour le cancer du sang
La leucémie myéloïde aiguë (LMA) est un cancer du sang agressif dans lequel des globules blancs immatures prolifèrent de manière incontrôlée et résistent à de nombreux traitements. Cette étude révèle comment un seul gène, BCLAF1, est découpé et réassemblé en différentes versions dans les cellules leucémiques — et comment des médicaments ciblant les « interrupteurs » épigénétiques de la cellule peuvent inverser ce profil d’épissage vers un état plus normal et moins agressif. Comprendre cette couche cachée de régulation pourrait ouvrir de nouvelles pistes pour maîtriser des leucémies résistantes sans recourir à des chimiothérapies entièrement nouvelles.
Un gène, deux versions opposées
BCLAF1 est une protéine multifonction impliquée dans la mort cellulaire, la réparation de l’ADN et la réponse au stress. Le gène peut être épissé en une forme pleine longueur et une forme plus courte, qui se comportent presque comme des opposés moléculaires. Dans les cellules de LMA et les échantillons de patients, les auteurs ont observé une nette prédominance de la version pleine longueur, qui favorise la croissance des cellules cancéreuses, tandis que la version courte, apparemment plus protectrice, est relativement sous-représentée. En revanche, dans les cellules souches et progénitrices sanguines saines, les deux formes sont maintenues en équilibre. Ce déséquilibre spécifique à la leucémie suggère que la version pleine longueur de BCLAF1 pourrait servir à la fois de marqueur de la maladie et de moteur du comportement malin.
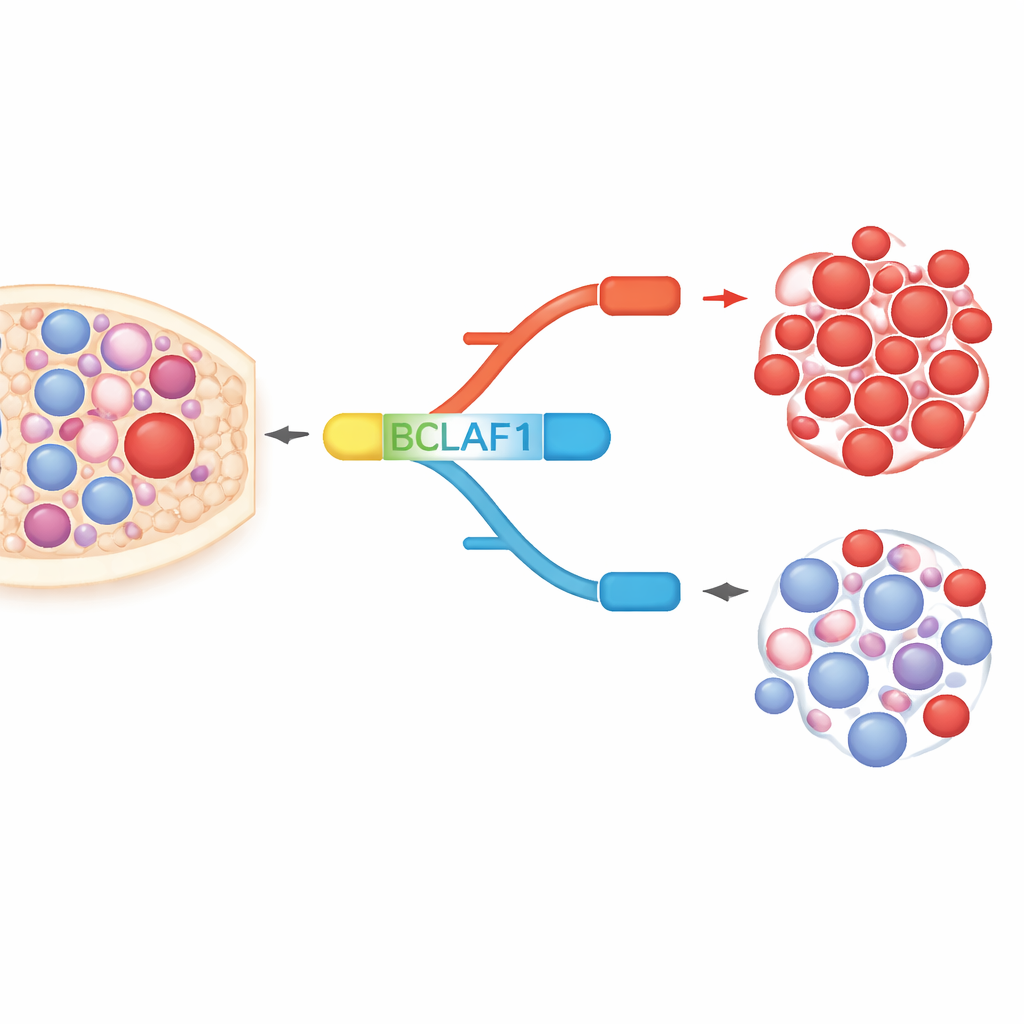
Comment les commutateurs chimiques remodèlent l’épissage
L’équipe s’est ensuite demandé si des médicaments épigénétiques — des composés qui modifient la façon dont l’ADN est empaqueté et lu — pouvaient rétablir cet équilibre. Ils ont traité des lignées cellulaires leucémiques avec plusieurs de ces agents, y compris l’inhibiteur des histone désacétylases SAHA (vorinostat) et des composés ciblant la méthylation de l’ADN. Un schéma clair est apparu : certains médicaments ont réduit la forme pleine longueur de BCLAF1 et augmenté la forme courte, sans affecter d’autres variants de BCLAF1. Des analyses détaillées de la chromatine ont montré que, dans les conditions leucémiques normales, deux enzymes, DNMT3A et HDAC1, sont présentes sur des régions clés du gène BCLAF1 et contribuent à maintenir une configuration répressive favorisant l’épissage en pleine longueur. Le traitement par SAHA a desserré cette structure, évincé DNMT3A et HDAC1, augmenté les marques d’histones associées à l’activation et permis à un autre facteur, MRG15, de se lier à l’intérieur de l’exon 5, orientant ainsi l’épissage vers la version courte.
Deux enzymes de méthylation de l’ADN, des rôles opposés
Pour disséquer les rôles des enzymes apparentées DNMT3A et DNMT3B, les chercheurs ont conçu des cellules de LMA dans lesquelles chaque enzyme pouvait être spécifiquement désactivée. L’inhibition de DNMT3A a ralenti la croissance cellulaire, affaibli la liaison de HDAC1 sur le gène BCLAF1 et entraîné un épissage vers la version courte, probablement suppresseur de tumeur. DNMT3B s’est comportée très différemment : elle est en fait réduite dans les échantillons de patients atteints de LMA, et lorsque l’équipe a encore diminué DNMT3B dans les cellules, cela a étonnamment augmenté l’isoforme pleine longueur favorisant le cancer. Des essais biochimiques ont révélé que DNMT3B peut se lier directement à l’ARN de BCLAF1 plutôt qu’à l’ADN uniquement, et après traitement par SAHA ou perte de DNMT3A, elle interagit aussi avec la forme d’ARN courte. Ensemble, ces observations suggèrent que DNMT3A module l’épissage de BCLAF1 principalement via la structure de la chromatine, tandis que DNMT3B ajuste finement le processus en interagissant avec l’ARN lui-même.
Ajuster BCLAF1 après sa synthèse
L’histoire ne s’arrête pas une fois la protéine BCLAF1 produite. Les auteurs ont étudié comment les étiquettes chimiques ajoutées à BCLAF1 après la traduction — en particulier la phosphorylation — évoluent en réponse aux médicaments épigénétiques et comment cela modifie la localisation de la protéine dans la cellule. Sous traitement par SAHA, ils ont observé des modifications de la phosphorylation en sites spécifiques et des changements quant à savoir si BCLAF1 se trouvait dans le noyau ou diffusait dans le cytoplasme. Des analyses protéomiques et phosphoprotéomiques à grande échelle ont montré que SAHA atténue de manière générale les voies impliquées dans la croissance cellulaire, la réplication de l’ADN et le traitement des ARN, y compris la machinerie du spliceosome qui aide à découper et joindre les ARN. Ces données soutiennent l’idée que BCLAF1 se situe à une intersection reliant l’état de la chromatine, l’épissage de l’ARN et le contrôle du cycle cellulaire.
Ce que cela signifie pour les thérapies futures de la leucémie
Globalement, l’étude révèle que les cellules de LMA exploitent la machinerie épigénétique pour favoriser une version de BCLAF1 promouvant le cancer, tout en réprimant une forme courte et plus protectrice. En perturbant des enzymes clés telles que DNMT3A, HDAC1 et DNMT3B, les médicaments épigénétiques peuvent rééquilibrer cette décision d’épissage et affaiblir les programmes de survie des cellules leucémiques. Pour un lecteur non spécialiste, l’idée essentielle est que ce n’est pas seulement l’allumage ou l’extinction des gènes qui compte, mais aussi la façon dont le message de chaque gène est édité. Cibler les éditeurs — plutôt que le gène lui‑même — pourrait offrir un moyen puissant de restaurer des schémas d’utilisation des gènes plus sains et d’améliorer les résultats pour les patients atteints de LMA difficiles à traiter.
Citation: Sgueglia, G., Massaro, C., Muro, A. et al. Dynamic epigenetic regulation of BCLAF1 splicing in acute myeloid leukemia. Cell Death Dis 17, 344 (2026). https://doi.org/10.1038/s41419-026-08594-4
Mots-clés: leucémie myéloïde aiguë, épissage alternatif, thérapie épigénétique, BCLAF1, DNMT3A