Clear Sky Science · zh
鞘氨醇-1-磷酸通过外泌体转移TGFBR2促使乳腺癌中CD8 T细胞衰竭
这对癌症治疗为何重要
许多现代癌症疗法旨在释放机体自身的免疫系统,尤其是杀伤性CD8 T细胞,以攻击肿瘤。然而在许多乳腺癌中,这些细胞会变得疲惫且无效,处于所谓的衰竭状态,因此免疫治疗常常效果有限。本研究揭示了乳腺肿瘤以一种先前未被注意到的方式在远处化学性“镇静”CD8 T细胞,暴露出一条新的信号通路,可能通过阻断该通路来增强现有免疫疗法的效果。
一种塑造肿瘤微环境的脂类分子
研究人员将注意力集中在鞘氨醇-1-磷酸(S1P)上,这是一种类脂信号分子,在乳腺癌中含量偏高。S1P已知有助于肿瘤生成血管、转移并对治疗产生耐受性。本研究团队探讨S1P是否也帮助肿瘤在其周围使CD8 T细胞失能。当他们在含S1P的条件下培养人类乳腺癌细胞,并与人CD8 T细胞共培养时,T细胞的分裂明显减少,即便两者不能直接接触也如此。这种无需接触的抑制提示肿瘤细胞向培养体系释放了某种携带信息的颗粒。
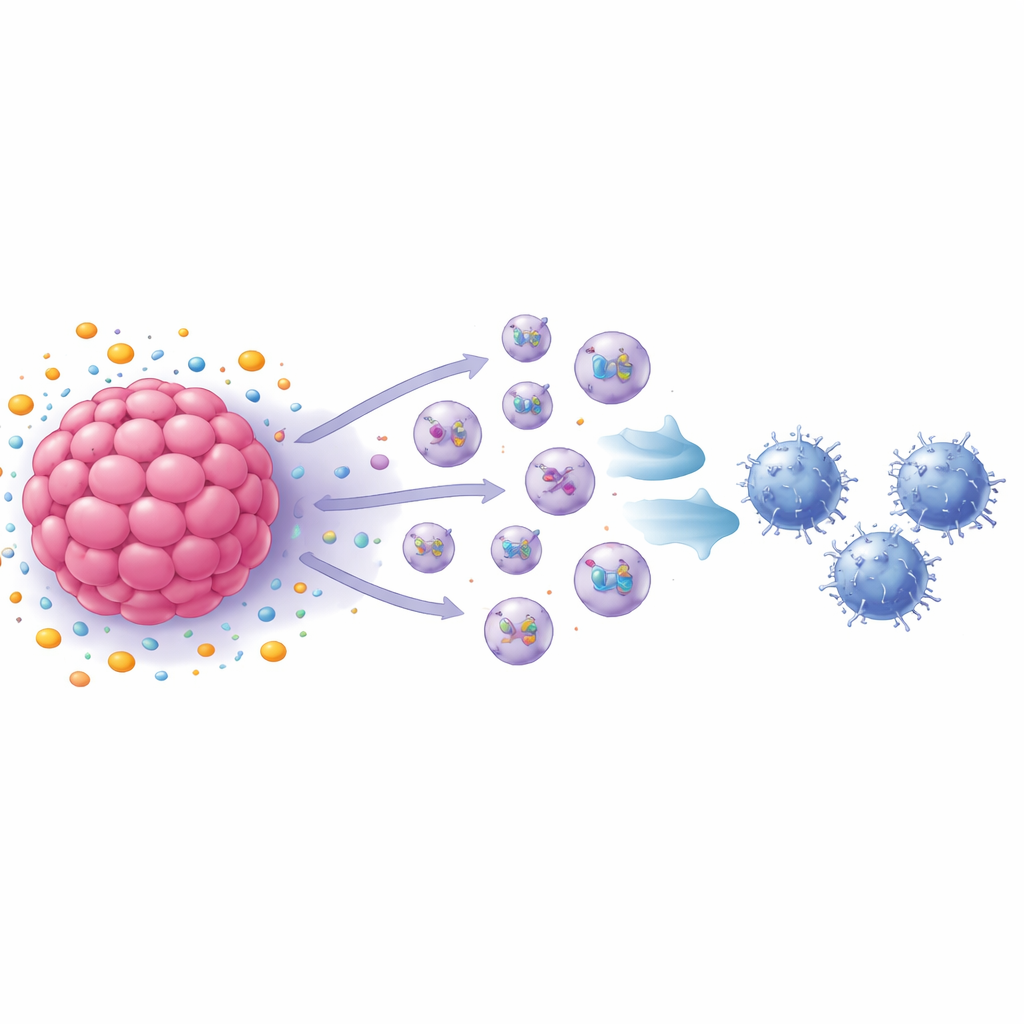
作为免疫抑制信使的微小囊泡
团队随后转向外泌体——由细胞释放的纳米级囊泡,可携带蛋白质和其他分子到远处靶点。阻断外泌体的产生在很大程度上恢复了CD8 T细胞的增殖,分析显示经S1P处理的乳腺癌细胞释放的外泌体数量多于未处理细胞。当将这些外泌体直接加入活化的CD8 T细胞时,T细胞的增殖放慢,并开始出现衰竭特征,包括若干与功能衰竭相关的表面和细胞内标志物。在动物实验中,来自S1P处理的小鼠乳腺癌细胞的外泌体加速了肿瘤生长并增加了肿瘤内的衰竭CD8 T细胞,而来自缺失关键受体的细胞的外泌体则产生相反效果。
装载在外泌体内的受体造成破坏
为探究这些外泌体为何有害,科学家们考察了其货物中富集的免疫相关蛋白。他们发现一种蛋白——转化生长因子β受体2(TGFBR2)在S1P处理后显著增加,而另一种知名免疫检查点蛋白PD-L1则未见增加。外泌体与CD8 T细胞融合并将TGFBR2递送到T细胞表面,实际上为T细胞配备了额外的一份能在细胞内驱动衰竭程序的受体。当团队用抗体阻断外泌体上的TGFBR2或在癌细胞中降低其含量时,这些外泌体不再抑制T细胞活性或诱导衰竭标志物,CD8 T细胞也重新获得产生关键攻击分子的能力。
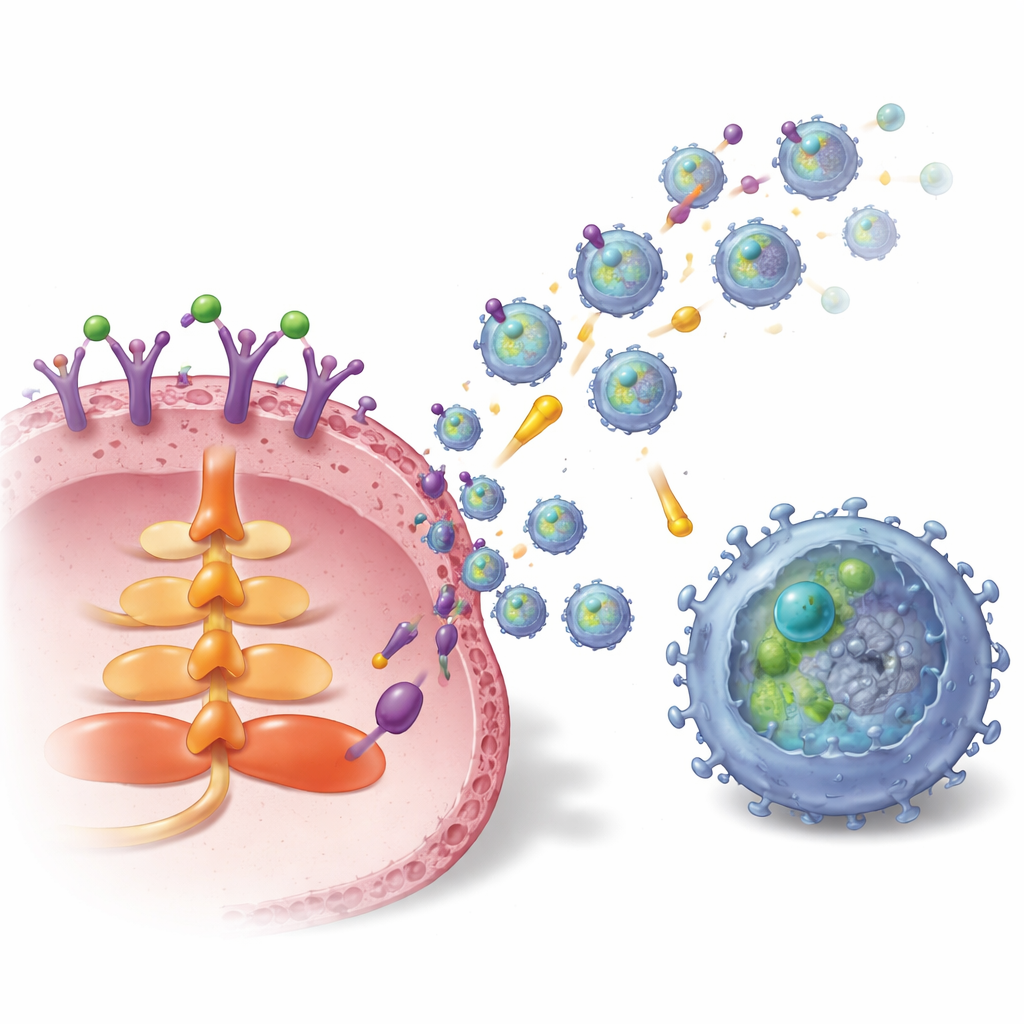
肿瘤如何装载并发射这些囊泡
研究接着描绘了将S1P与外泌体产生及TGFBR2装载连接起来的内部线路。乳腺癌细胞上一种特定的S1P受体,称为S1P1,被激活后启动了AKT信号通路和一种名为Rab27a的转运蛋白,这两者对外泌体释放至关重要。同时,S1P1还提高了癌细胞内TGFBR2的数量和稳定性。这通过两种方式实现:一是激活转录因子LEF1,增加TGFBR2基因的表达;二是通过ERK–CREB1信号轴提升去泛素化酶USP8的水平。USP8减缓了TGFBR2的降解,使更多受体积累并被打包进外泌体。在来自患者的乳腺肿瘤样本中,S1P1和TGFBR2在肿瘤组织及来源于肿瘤的外泌体中均高于邻近正常组织,且外泌体上更高的TGFBR2与更多衰竭的CD8 T细胞相关。
对患者意味着什么
对非专业读者而言,核心信息是某些乳腺癌创造了富含S1P的化学环境,指示肿瘤细胞大量分泌装载有受体TGFBR2的微小囊泡,这些囊泡使CD8 T细胞失去活性。它们像隐蔽的信包一样将附近的杀伤细胞重新编程,使其变得迟缓并对肿瘤宽容。通过明确S1P–S1P1–TGFBR2的事件链,以及控制外泌体释放和受体积累的内部开关,这项工作提出了若干新的药物靶点。抑制S1P信号、阻断S1P1或阻止TGFBR2被装载或稳定存在于外泌体上,可能减少CD8 T细胞的衰竭并使现有免疫治疗对乳腺癌患者更为有效。
引用: Bhoumick, A., Ghosh, A., Singh, A. et al. Sphingosine-1-phosphate promotes CD8 T cell exhaustion in breast cancer via exosomal transfer of TGFBR2. Cell Death Dis 17, 278 (2026). https://doi.org/10.1038/s41419-026-08523-5
关键词: 乳腺癌免疫治疗, CD8 T细胞衰竭, 鞘氨醇-1-磷酸, 外泌体, TGFBR2信号