Clear Sky Science · pt
Sfingosina-1-fosfato promove exaustão de células T CD8 no câncer de mama via transferência exossomal de TGFBR2
Por que isso importa para o tratamento do câncer
Muitas terapias modernas contra o câncer buscam liberar o próprio sistema imunológico do corpo, especialmente as células T CD8 citotóxicas, para atacar tumores. Ainda assim, em muitos cânceres de mama essas células ficam cansadas e ineficazes, um estado conhecido como exaustão, e a imunoterapia muitas vezes tem efeito modesto. Este estudo revela um modo antes oculto pelo qual tumores mamários “sedam” quimicamente as células T CD8 à distância, apontando uma via de sinalização nova que pode ser bloqueada para ajudar as imunoterapias existentes a funcionarem melhor.
Uma molécula lipídica que modela o microambiente tumoral
Os pesquisadores focaram na sfingosina-1-fosfato (S1P), uma molécula semelhante a um lipídio encontrada em níveis elevados no câncer de mama. S1P já é conhecida por ajudar tumores a formar vasos sanguíneos, espalhar-se e resistir a tratamentos. Aqui, a equipe perguntou se a S1P também ajuda tumores a desarmar células T CD8 em seu entorno. Quando cultivaram células humanas de câncer de mama tratadas com S1P e, em seguida, as co-cultivaram com células T CD8 humanas, as T tiveram proliferação muito menor, mesmo quando não havia contato físico com as células tumorais. Essa supressão sem contato sugeriu que as células tumorais liberavam algum tipo de partículas mensageiras na cultura.
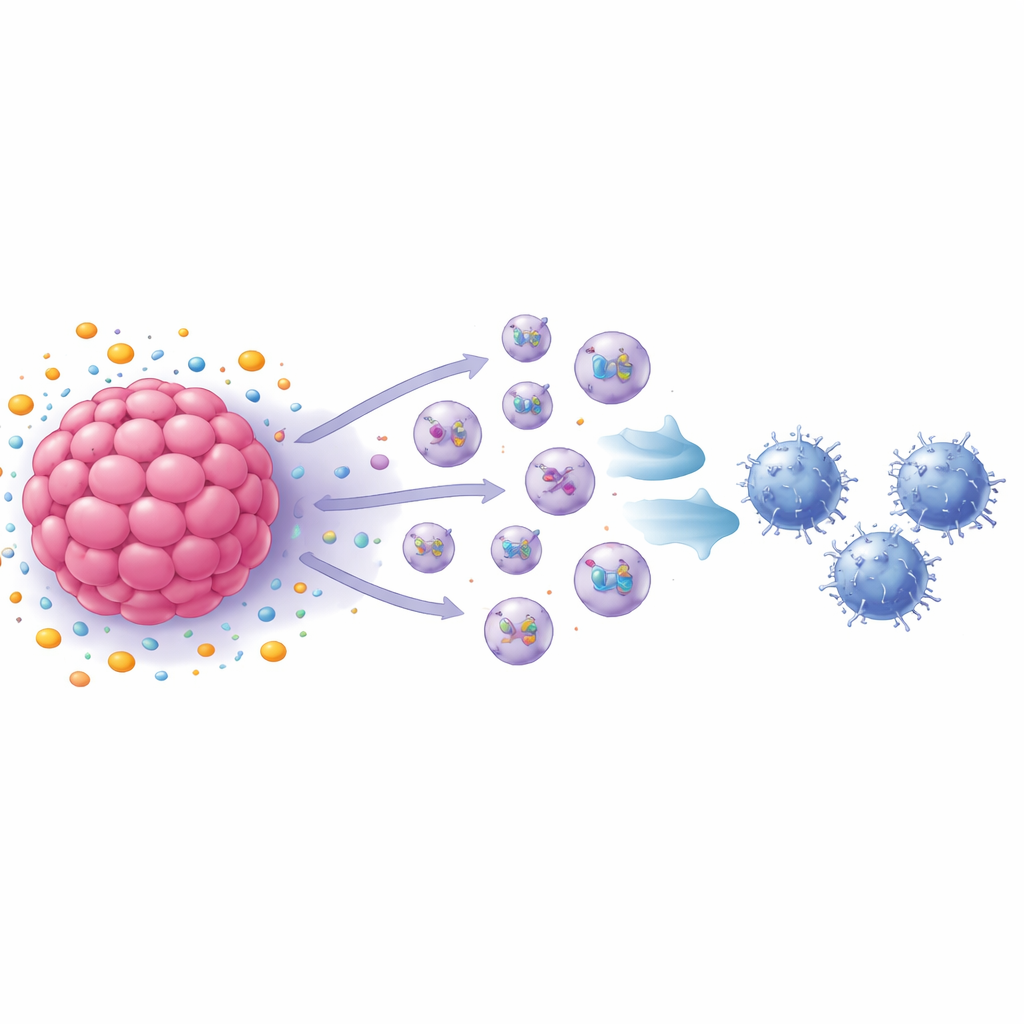
Vesículas minúsculas como mensageiras da supressão imune
O grupo então concentrou-se nos exossomos—vesículas na escala de nanômetros liberadas por células que transportam proteínas e outras moléculas para alvos distantes. Bloquear a produção de exossomos restaurou em grande parte o crescimento das células T CD8, e a análise mostrou que células de câncer de mama tratadas com S1P liberaram muito mais exossomos do que células não tratadas. Quando esses exossomos foram adicionados diretamente a células T CD8 ativadas, as T reduziram sua proliferação e passaram a exibir sinais de exaustão, incluindo vários marcadores de superfície e internos associados a células imunes desgastadas. Em experimentos animais, exossomos de células de câncer de mama de camundongo tratadas com S1P aceleraram o crescimento tumoral e aumentaram as células T CD8 exaustas dentro dos tumores, enquanto exossomos de células sem um receptor chave tiveram o efeito oposto.
Um receptor embalado nos exossomos causa o dano
Ao investigar o que tornava esses exossomos tão nocivos, os cientistas analisaram proteínas relacionadas à imunidade enriquecidas em seu conteúdo. Encontraram que uma proteína, o receptor do fator de crescimento transformador beta 2 (TGFBR2), estava fortemente aumentada nos exossomos após o tratamento com S1P, enquanto outra proteína de ponto de checagem bem conhecida, PD-L1, não estava. Os exossomos se fundiram com as células T CD8 e entregaram TGFBR2 à superfície das T, efetivamente equipando as células com uma cópia adicional de um receptor que ativa programas de exaustão dentro da célula. Quando a equipe bloqueou TGFBR2 nos exossomos com um anticorpo ou reduziu seus níveis nas células tumorais, os exossomos não conseguiram mais suprimir a atividade das T nem induzir marcadores de exaustão, e as células T CD8 recuperaram a capacidade de produzir moléculas-chave de ataque.
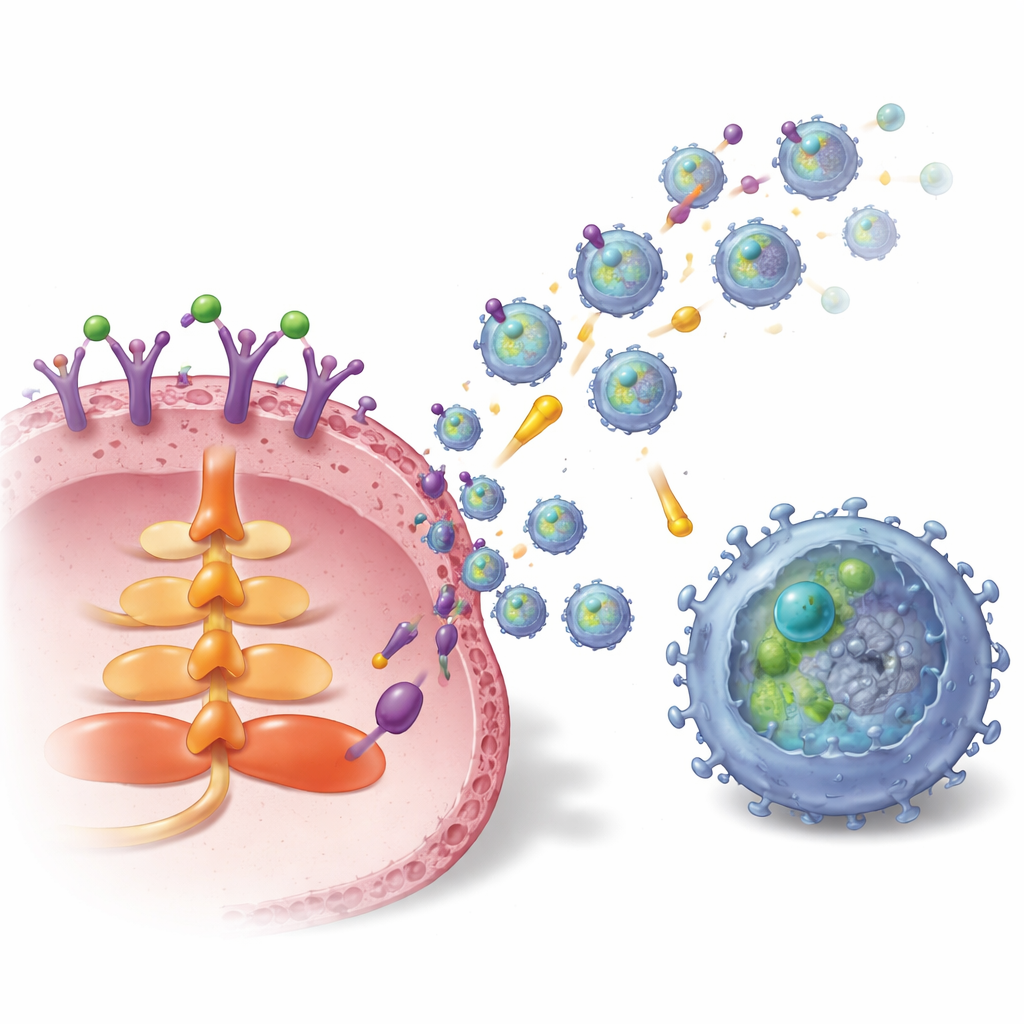
Como o tumor carrega e lança essas vesículas
O estudo mapeou então a fiação interna que conecta S1P à produção de exossomos e ao carregamento de TGFBR2. A ativação de um receptor específico de S1P nas células de câncer de mama, chamado S1P1, ligou a via de sinalização AKT e uma proteína de tráfego nomeada Rab27a, ambas cruciais para a liberação de exossomos. Ao mesmo tempo, S1P1 aumentou a quantidade e a estabilidade de TGFBR2 dentro das células tumorais. Fez isso de duas maneiras: primeiro ativando um fator de transcrição, LEF1, que eleva a expressão do gene TGFBR2; e segundo aumentando os níveis de uma desubiquitinase, USP8, por meio de uma rota de sinalização ERK–CREB1. USP8 retarda a degradação de TGFBR2, permitindo que mais do receptor se acumule e seja empacotado em exossomos. Em amostras de tumores mamários de pacientes, tanto S1P1 quanto TGFBR2 estavam mais altos no tecido tumoral e nos exossomos derivados do tumor do que no tecido normal vizinho, e níveis mais altos de TGFBR2 nos exossomos correlacionaram-se com maior presença de células T CD8 exaustas.
O que isso significa para os pacientes
Para um público não especializado, a mensagem central é que certos cânceres de mama criam um ambiente químico rico em S1P que instrui as células tumorais a bombear pequenas vesículas carregadas com um receptor, TGFBR2, que desativa as células T CD8. Essas vesículas agem como pacotes furtivos que reprogramam células citotóxicas próximas para ficarem lentas e tolerantes ao tumor. Ao identificar a cadeia de eventos S1P–S1P1–TGFBR2, incluindo os interruptores internos que controlam a liberação de exossomos e o acúmulo do receptor, este trabalho sugere vários novos alvos farmacológicos. Inibir a sinalização de S1P, bloquear S1P1 ou impedir que TGFBR2 alcance ou se estabilize nos exossomos pode reduzir a exaustão de células T CD8 e tornar as imunoterapias existentes mais eficazes para pacientes com câncer de mama.
Citação: Bhoumick, A., Ghosh, A., Singh, A. et al. Sphingosine-1-phosphate promotes CD8 T cell exhaustion in breast cancer via exosomal transfer of TGFBR2. Cell Death Dis 17, 278 (2026). https://doi.org/10.1038/s41419-026-08523-5
Palavras-chave: imunoterapia do câncer de mama, exaustão de células T CD8, sfingosina-1-fosfato, exossomos, sinalização TGFBR2