Clear Sky Science · nl
Sphingosine-1-fosfaat bevordert uitputting van CD8-T-cellen bij borstkanker via exosomale overdracht van TGFBR2
Waarom dit belangrijk is voor kankerbehandeling
Veel moderne kankertherapieën richten zich op het vrijmaken van het eigen immuunsysteem van het lichaam, in het bijzonder de dodelijke CD8-T-cellen, om tumoren aan te vallen. Toch raken deze cellen bij veel borsttumoren uitgeput en ondoeltreffend—een toestand die bekendstaat als uitputting—waardoor immunotherapie vaak slechts beperkte effecten heeft. Deze studie onthult een eerder verborgen manier waarop borsttumoren CD8-T-cellen op afstand chemisch 'verdoven', en toont een nieuw signaalpad dat geblokkeerd zou kunnen worden om bestaande immunotherapieën beter te laten werken.
Een vetmolecuul dat de tumoromgeving vormt
De onderzoekers concentreerden zich op sphingosine-1-fosfaat (S1P), een vetachtig signaalmolecuul dat in hoge concentraties voorkomt bij borstkanker. Van S1P is al bekend dat het tumoren helpt bloedvaten te vormen, uitzaaien te bevorderen en resistentie tegen behandelingen te geven. Hier onderzochten de onderzoekers of S1P ook helpt tumoren CD8-T-cellen in hun omgeving uit te schakelen. Wanneer ze menselijke borstkankercellen met S1P lieten groeien en die vervolgens co-cultiveerden met menselijke CD8-T-cellen, deelden de T-cellen veel minder, zelfs wanneer er geen fysiek contact met de kankercellen mogelijk was. Deze contactloze onderdrukking wees erop dat de tumorcellen een soort berichtdragende deeltjes in het kweekmedium vrijgaven.
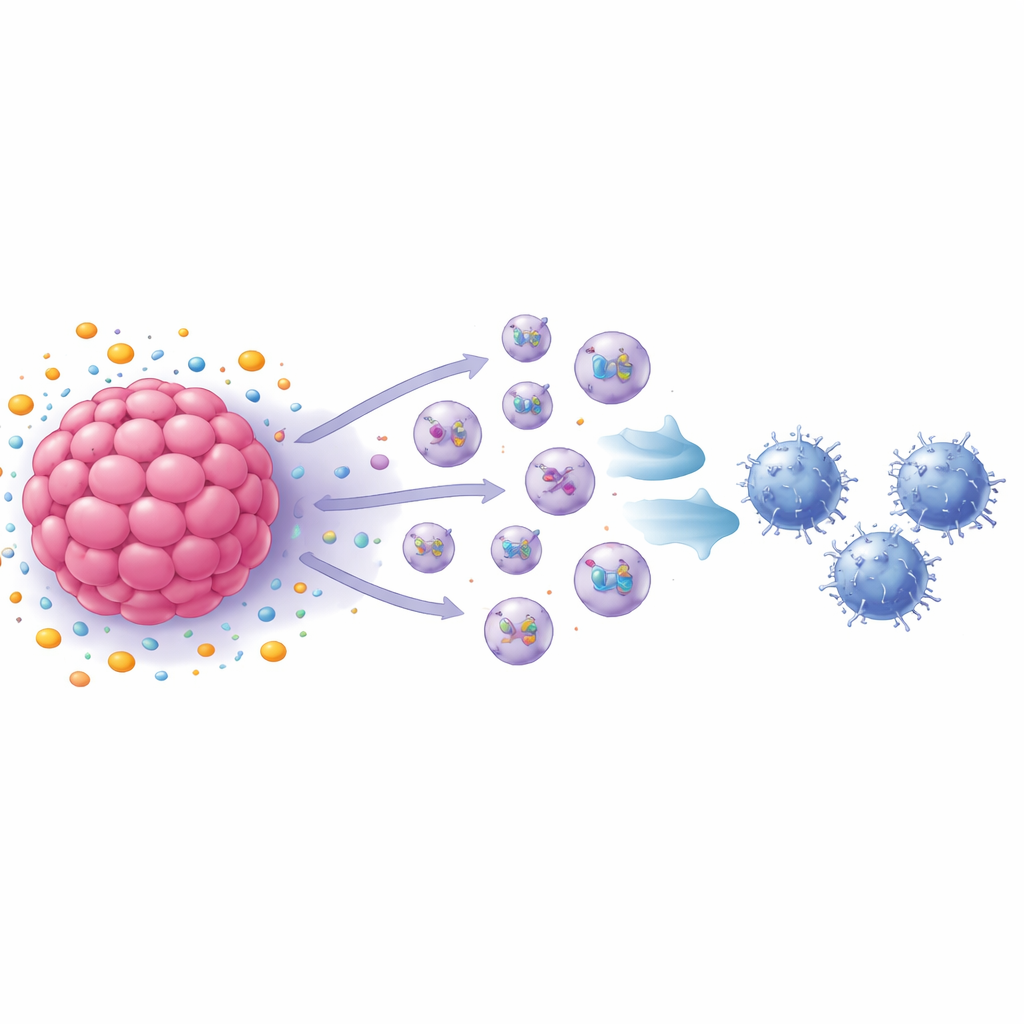
Minuscule blaasjes als boodschappers van immuunsuppressie
De groep richtte zich vervolgens op exosomen—vesikels op de nanometerschaal die door cellen worden afgescheiden en eiwitten en andere moleculen naar verre doelen vervoeren. Het blokkeren van exosoomproductie herstelde grotendeels de groei van CD8-T-cellen, en analyse toonde aan dat S1P-behandelde borstkankercellen veel meer exosomen afgeven dan onbehandelde cellen. Wanneer deze exosomen rechtstreeks aan geactiveerde CD8-T-cellen werden toegevoegd, vertraagden de T-cellen hun proliferatie en begonnen ze kenmerken van uitputting te vertonen, waaronder meerdere oppervlakte- en intracellulaire merkers die geassocieerd zijn met uitgeputte immuuncellen. In proefdieren versnelden exosomen van S1P-behandelde muizenborstkankercellen de tumorgroei en verhoogden ze het aantal uitgeputte CD8-T-cellen in tumoren, terwijl exosomen van cellen zonder een sleutelreceptor het tegengestelde effect hadden.
Een receptor verpakt in exosomen doet de schade
Om te achterhalen wat deze exosomen zo schadelijk maakte, onderzochten de wetenschappers immuun-gerelateerde eiwitten die verrijkt waren in hun lading. Ze vonden dat één eiwit, de transforming growth factor beta receptor 2 (TGFBR2), sterk verhoogd aanwezig was op exosomen na S1P-behandeling, terwijl een ander bekend checkpoint-eiwit, PD-L1, dat niet was. De exosomen fuseerden met CD8-T-cellen en leverden TGFBR2 aan het celoppervlak van de T-cellen, waardoor de T-cellen effectief werden uitgerust met een extra kopie van een receptor die uitputtingsprogramma’s binnenin de cel activeert. Wanneer het team TGFBR2 op de exosomen blokkeerde met een antilichaam of de niveaus ervan in de kankercellen verlaagde, konden de exosomen de T-celactiviteit niet langer onderdrukken of uitputtingsmerkers induceren, en herwonnen CD8-T-cellen hun vermogen om sleutelmoleculen voor aanval te produceren.
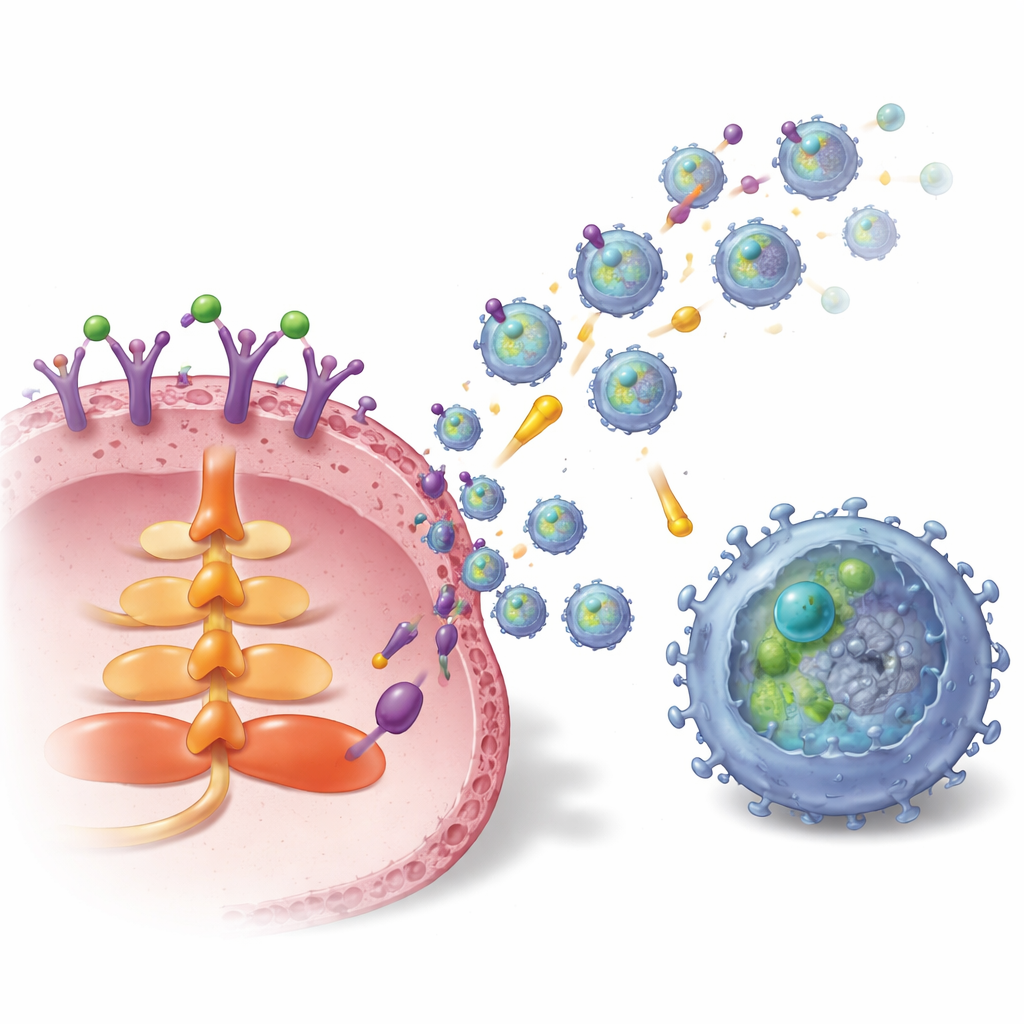
Hoe de tumor deze vesikels laadt en lanceert
De studie bracht vervolgens de interne bedrading in kaart die S1P verbindt met exosoomproductie en TGFBR2-belading. Activatie van een specifieke S1P-receptor op borstkankercellen, S1P1 genoemd, schakelde het AKT-signaalpad in en een trafficking-eiwit genaamd Rab27a, die beiden cruciaal zijn voor exosoomafgifte. Tegelijkertijd verhoogde S1P1 de hoeveelheid en stabiliteit van TGFBR2 in kankercellen. Dit gebeurde op twee manieren: eerst door een transcriptiefactor, LEF1, aan te zetten die de expressie van het TGFBR2-gen verhoogt, en ten tweede door via een ERK–CREB1-signaalroute de niveaus van een deubiquitinasem, USP8, te verhogen. USP8 vertraagt de afbraak van TGFBR2, waardoor meer van de receptor zich ophoopt en in exosomen kan worden verpakt. In borsttumor-monsters van patiënten waren zowel S1P1 als TGFBR2 hoger in tumorgebied en in tumor-afgeleide exosomen dan in het naburige normale weefsel, en hogere TGFBR2 op exosomen correleerde met meer uitgeputte CD8-T-cellen.
Wat dit betekent voor patiënten
Voor niet-specialisten is de kernboodschap dat bepaalde borstkankers een chemisch bad rijk aan S1P creëren dat tumorcellen instrueert om kleine vesikels uit te pompen die geladen zijn met een receptor, TGFBR2, die CD8-T-cellen uitschakelt. Deze vesikels werken als sluipende pakketjes die nabijgelegen dodelijke cellen herprogrammeren tot traagheid en tolerantie ten opzichte van de tumor. Door de S1P–S1P1–TGFBR2-keten van gebeurtenissen te ontleden, inclusief de interne schakelaars die exosoomafgifte en receptoropeenhoping controleren, suggereert dit werk meerdere nieuwe geneesmiddelendoelen. Het remmen van S1P-signaalgeving, het blokkeren van S1P1, of het verhinderen dat TGFBR2 exosomen bereikt of daar stabiel wordt, kan de uitputting van CD8-T-cellen verminderen en bestaande immunotherapieën effectiever maken voor borstkankerpatiënten.
Bronvermelding: Bhoumick, A., Ghosh, A., Singh, A. et al. Sphingosine-1-phosphate promotes CD8 T cell exhaustion in breast cancer via exosomal transfer of TGFBR2. Cell Death Dis 17, 278 (2026). https://doi.org/10.1038/s41419-026-08523-5
Trefwoorden: immunotherapie bij borstkanker, uitputting van CD8-T-cellen, sphingosine-1-fosfaat, exosomen, TGFBR2-signaaloverdracht