Clear Sky Science · de
Sphingosin-1-phosphat fördert die Erschöpfung von CD8-T-Zellen bei Brustkrebs durch exosomalen Transfer von TGFBR2
Warum das für die Krebstherapie wichtig ist
Viele moderne Krebstherapien zielen darauf ab, das körpereigene Immunsystem — insbesondere die zytotoxischen CD8-T-Zellen — zu mobilisieren, damit es Tumore angreift. Bei vielen Brustkrebserkrankungen werden diese Zellen jedoch müde und wirkungslos, ein Zustand, der als Erschöpfung bezeichnet wird, weshalb Immuntherapien oft nur begrenzt wirksam sind. Diese Studie deckt einen zuvor verborgenen Mechanismus auf, mit dem Brusttumore CD8-T-Zellen aus der Ferne chemisch „beruhigen“ und beschreibt eine neue Signalroute, die blockiert werden könnte, um bestehende Immuntherapien zu verbessern.
Ein fettähnliches Molekül, das das Tumorumfeld formt
Die Forschenden konzentrierten sich auf Sphingosin-1-phosphat (S1P), ein fettähnliches Signalmolekül, das in Brustkrebs erhöht vorkommt. S1P ist bereits dafür bekannt, Tumoren beim Aufbau von Blutgefäßen, bei der Metastasierung und bei der Therapieflucht zu unterstützen. Hier untersuchte das Team, ob S1P auch dazu beiträgt, CD8-T-Zellen in der Tumorumgebung zu entwaffnen. Wuchsen menschliche Brustkrebszellen mit S1P und wurden anschließend gemeinsam mit menschlichen CD8-T-Zellen kultiviert, teilten sich die T-Zellen deutlich weniger, selbst wenn kein physischer Kontakt zwischen beiden Zelltypen bestand. Diese kontaktfreie Unterdrückung deutete darauf hin, dass die Tumorzellen Botschafts-transportierende Partikel in die Kultur freisetzten.
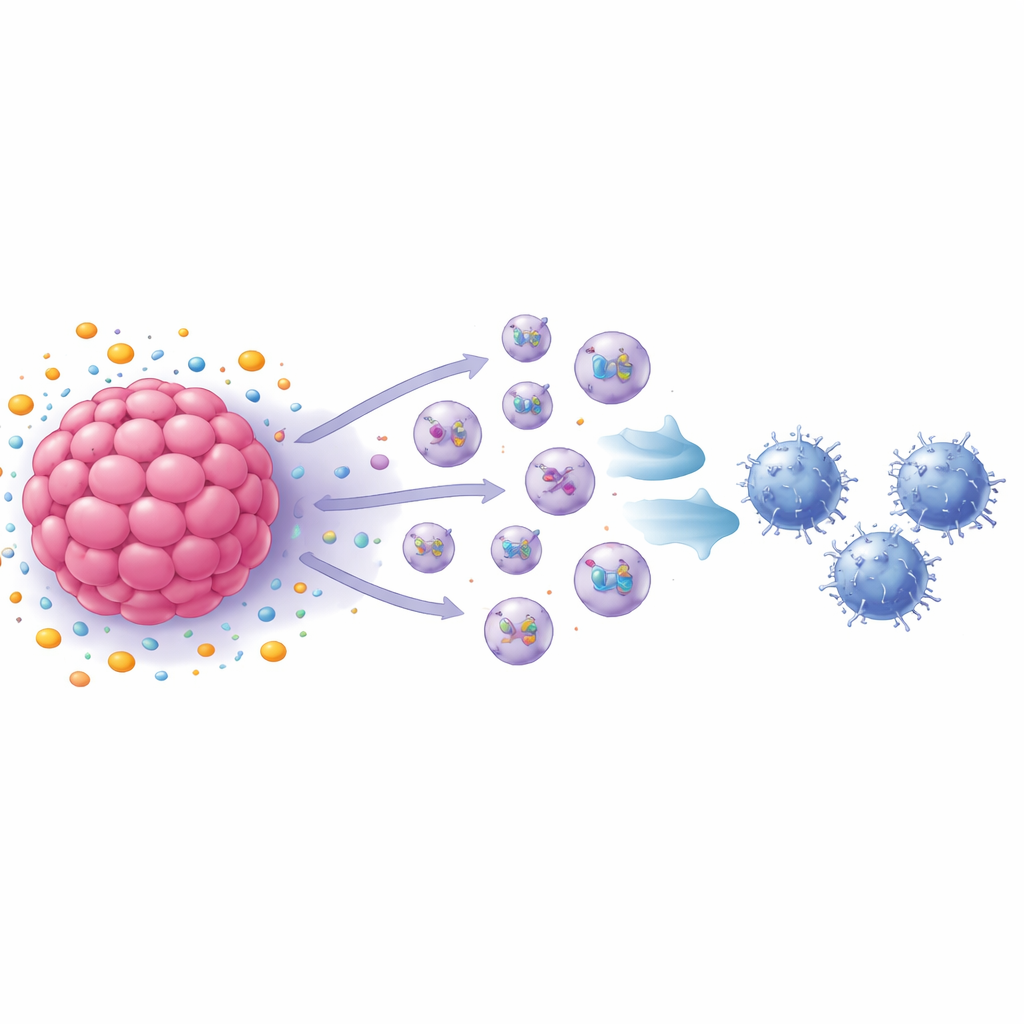
Kleine Vesikel als Boten der Immunsuppression
Die Gruppe richtete den Blick als Nächstes auf Exosomen — nanometergroße Vesikel, die Zellen absondern und Proteine sowie andere Moleküle zu entfernten Zielen transportieren. Die Blockade der Exosomenbildung stellte weitgehend das Wachstum der CD8-T-Zellen wieder her, und Analysen zeigten, dass S1P-behandelte Brustkrebszellen deutlich mehr Exosomen freisetzten als unbehandelte Zellen. Wurden diese Exosomen direkt zu aktivierten CD8-T-Zellen gegeben, verlangsamte sich die Proliferation der T-Zellen und sie begannen, Kennzeichen der Erschöpfung zu zeigen, darunter mehrere Oberflächen- und intrazelluläre Marker, die mit ausgepowerten Immunzellen assoziiert sind. In Tierversuchen beschleunigten Exosomen aus S1P-behandelten Maus-Brustkrebszellen das Tumorwachstum und erhöhten den Anteil erschöpfter CD8-T-Zellen in den Tumoren, während Exosomen aus Zellen ohne den Schlüsselrezeptor den gegenteiligen Effekt hatten.
Ein in Exosomen verpackter Rezeptor richtet den Schaden an
Um herauszufinden, was diese Exosomen so schädlich machte, untersuchten die Wissenschaftler immunrelevante Proteine, die in ihrem Inhalt angereichert waren. Sie fanden, dass ein Protein, der Transforming Growth Factor Beta Receptor 2 (TGFBR2), nach S1P-Behandlung auf Exosomen stark erhöht war, während ein anderer bekannter Checkpoint-Protein, PD-L1, dies nicht war. Die Exosomen verschmolzen mit CD8-T-Zellen und lieferten TGFBR2 an die T-Zell-Oberfläche, wodurch die T-Zellen effektiv mit einer zusätzlichen Kopie eines Rezeptors ausgestattet wurden, der Erschöpfungsprogramme in der Zelle auslöst. Blockierte das Team TGFBR2 auf den Exosomen mit einem Antikörper oder reduzierten es dessen Menge in den Krebszellen, konnten die Exosomen die T-Zell-Aktivität nicht mehr unterdrücken und keine Erschöpfungsmarker mehr induzieren; die CD8-T-Zellen erlangten wieder die Fähigkeit, wichtige Angriffsmoleküle zu produzieren.
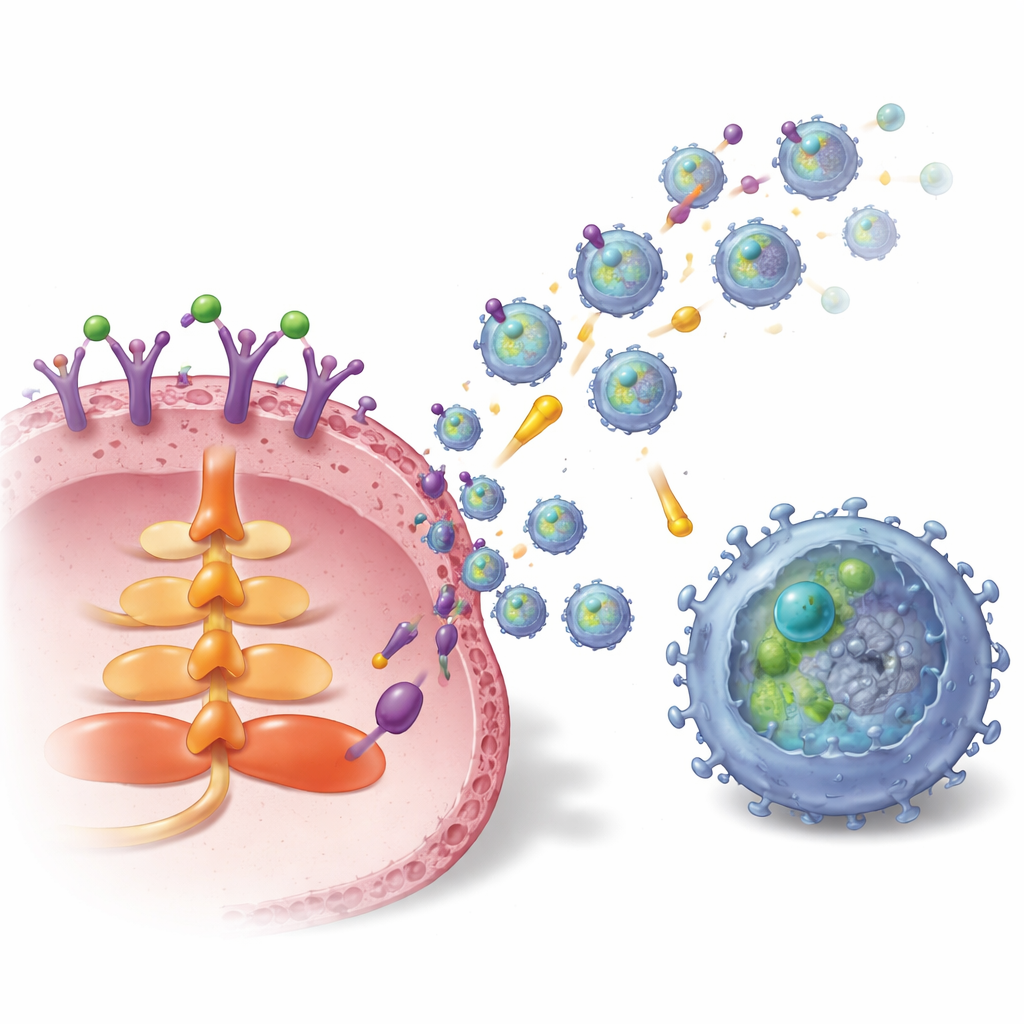
Wie der Tumor diese Vesikel belädt und abfeuert
Die Studie kartierte dann die interne Verschaltung, die S1P mit der Exosomenproduktion und der Beladung mit TGFBR2 verbindet. Die Aktivierung eines spezifischen S1P-Rezeptors auf Brustkrebszellen, genannt S1P1, schaltete den AKT-Signalweg und ein Transportprotein namens Rab27a ein, die beide für die Freisetzung von Exosomen entscheidend sind. Gleichzeitig erhöhte S1P1 Menge und Stabilität von TGFBR2 in Krebszellen. Das geschah auf zwei Wegen: erstens durch Aktivierung eines Transkriptionsfaktors, LEF1, der die TGFBR2-Genexpression steigert, und zweitens durch Anhebung der Spiegel eines Deubiquitinase-Enzyms, USP8, über eine ERK–CREB1-Signalkaskade. USP8 verlangsamt den Abbau von TGFBR2, wodurch mehr Rezeptor akkumuliert und in Exosomen verpackt werden kann. In Brusttumorproben von Patientinnen und Patienten waren sowohl S1P1 als auch TGFBR2 im Tumorgewebe und in tumorabgeleiteten Exosomen höher als im angrenzenden Normalgewebe, und höhere TGFBR2-Spiegel auf Exosomen korrelierten mit mehr erschöpften CD8-T-Zellen.
Was das für Patientinnen und Patienten bedeutet
Für Nicht-Spezialisten lautet die Kernbotschaft: Bestimmte Brustkrebserkrankungen erzeugen ein chemisches Milieu mit hohem S1P, das die Tumorzellen anweist, winzige Vesikel voller des Rezeptors TGFBR2 auszusenden, die CD8-T-Zellen abschalten. Diese Vesikel wirken wie Tarnpakete, die nahegelegene Killerzellen so umprogrammieren, dass sie träge werden und dem Tumor gegenüber tolerant bleiben. Durch die Identifizierung der S1P–S1P1–TGFBR2-Kaskade sowie der internen Schalter, die Exosomenfreisetzung und Rezeptorakkumulation steuern, schlägt diese Arbeit mehrere neue pharmakologische Angriffspunkte vor. Die Hemmung der S1P-Signalgebung, das Blockieren von S1P1 oder das Verhindern, dass TGFBR2 Exosomen erreicht oder dort stabilisiert wird, könnte die Erschöpfung von CD8-T-Zellen reduzieren und bestehende Immuntherapien bei Brustkrebspatientinnen und -patienten wirksamer machen.
Zitation: Bhoumick, A., Ghosh, A., Singh, A. et al. Sphingosine-1-phosphate promotes CD8 T cell exhaustion in breast cancer via exosomal transfer of TGFBR2. Cell Death Dis 17, 278 (2026). https://doi.org/10.1038/s41419-026-08523-5
Schlüsselwörter: Immuntherapie bei Brustkrebs, Erschöpfung von CD8-T-Zellen, Sphingosin-1-phosphat, Exosomen, TGFBR2-Signalübertragung