Clear Sky Science · ar
يسهم سفنغوزين-1-فوسفات في إجهاد الخلايا T CD8 في سرطان الثدي عبر نقل TGFBR2 بواسطة الحويصلات النَفْسَجِيَّة
لماذا يهم هذا لعلاج السرطان
تهدف العديد من علاجات السرطان الحديثة إلى تحرير نظام المناعة الخاص بالجسم، لا سيما خلايا القتل CD8 T، لمهاجمة الأورام. ومع ذلك، في كثير من سرطانات الثدي، تصبح هذه الخلايا مرهقة وغير فعالة، حالة تعرف بالإجهاد، وغالبًا ما تعمل العلاجات المناعية بشكل محدود. تكشف هذه الدراسة عن مسار كيميائي مخفي سابقًا يستخدمه ورم الثدي لـ"تخدير" خلايا CD8 عن بعد، ما يبرز مسار إشارات جديد قد يمكن حظره لمساعدة العلاجات المناعية الحالية على العمل بشكل أفضل.
جزيء دهني يشكل بيئة الورم
ركز الباحثون على سفنغوزين-1-فوسفات (S1P)، وهو جزيء شبيه بالدهون موجود بمستويات عالية في سرطان الثدي. يُعرف عن S1P أنه يساعد الأورام على تكوين أوعية دموية، والانتشار، والمقاومة للعلاج. هنا، سأل الفريق ما إذا كان S1P يساعد أيضًا الأورام على تعطيل خلايا CD8 في محيطها. عندما زرعوا خلايا سرطانية بشرية للثدي مع S1P ثم أجروا تعايشًا خلويًا مع خلايا CD8 بشرية، انقسمت خلايا T بنسبة أقل بكثير، حتى عندما لم يكن بالإمكان للمسخدمين الاتصال المادي مع خلايا السرطان. هذا القمع دون اتصال أشار إلى أن خلايا الورم كانت تطلق نوعًا من الجسيمات الحاملة للرسائل في الوسط.
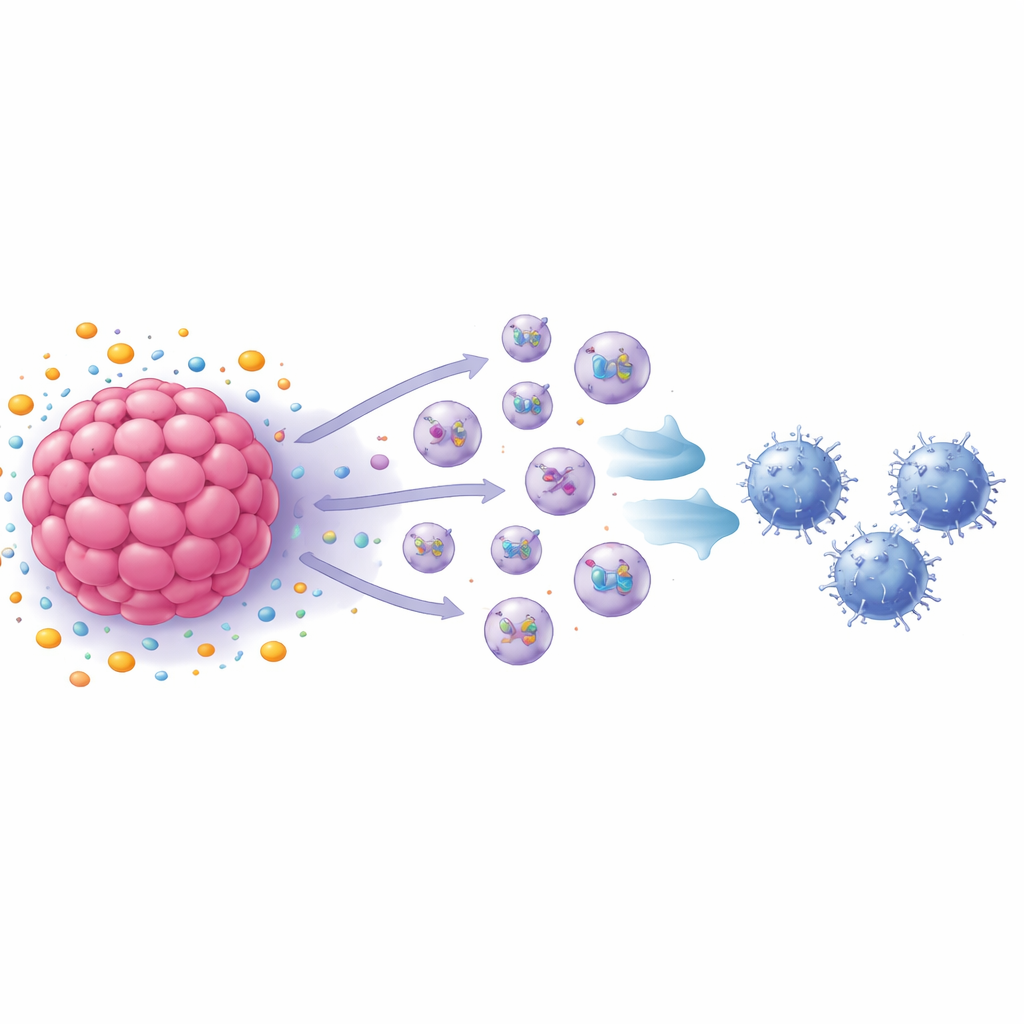
حويصلات دقيقة كرسائل لقمع المناعة
تحول الفريق بعد ذلك إلى الإكسوسومات—حويصلات على مقياس النانومتر تفرزها الخلايا وتحمل البروتينات وجزيئات أخرى إلى أهداف بعيدة. أدى حظر إنتاج الإكسوسومات إلى استعادة نمو خلايا CD8 في الغالب، وأظهر التحليل أن خلايا سرطان الثدي المعالجة بـ S1P أفرزت عددًا أكبر بكثير من الإكسوسومات مقارنة بالخلايا غير المعالجة. عندما أضيفت هذه الإكسوسومات مباشرة إلى خلايا CD8 المنشطة، تباطأ تكاثر خلايا T وبدأت تظهر عليها علامات الإجهاد، بما في ذلك عدة مؤشرات سطحية وداخلية مرتبطة بخلايا المناعة المتعبة. في تجارب على الحيوانات، سرّعت الإكسوسومات من خلايا سرطان الثدي الفأرية المعالجة بـ S1P نمو الورم وزادت من عدد خلايا CD8 المتعبة داخل الأورام، بينما كانت للإكسوسومات القادمة من خلايا تفتقر إلى مستقبل رئيسي تأثير معاكس.
مستقبل محمّل داخل الإكسوسومات يلحِق الضرر
للبحث فيما يجعل هذه الإكسوسومات ضارة للغاية، درس العلماء البروتينات المرتبطة بالمناعة والمركزة في حمولتها. وجدوا أن بروتينًا واحدًا، مستقبل عامل نمو التحول بيتا 2 (TGFBR2)، ازداد بقوة على الإكسوسومات بعد معالجة S1P، بينما لم يزد أحد بروتينات نقاط التفتيش المعروفة، PD-L1. اندمجت الإكسوسومات مع خلايا CD8 وسلمت TGFBR2 إلى سطح الخلية اللمفاوية، مزودة إياها فعليًا بنسخة إضافية من مستقبل يُشغّل برامج الإجهاد داخل الخلية. عندما قام الفريق بحظر TGFBR2 على الإكسوسومات بواسطة جسم مضاد أو خفض مستوياته في خلايا السرطان، لم تعد الإكسوسومات قادرة على قمع نشاط الخلايا التائية أو إحداث علامات الإجهاد، واستعادت خلايا CD8 قدرتها على إنتاج جزيئات الهجوم الأساسية.
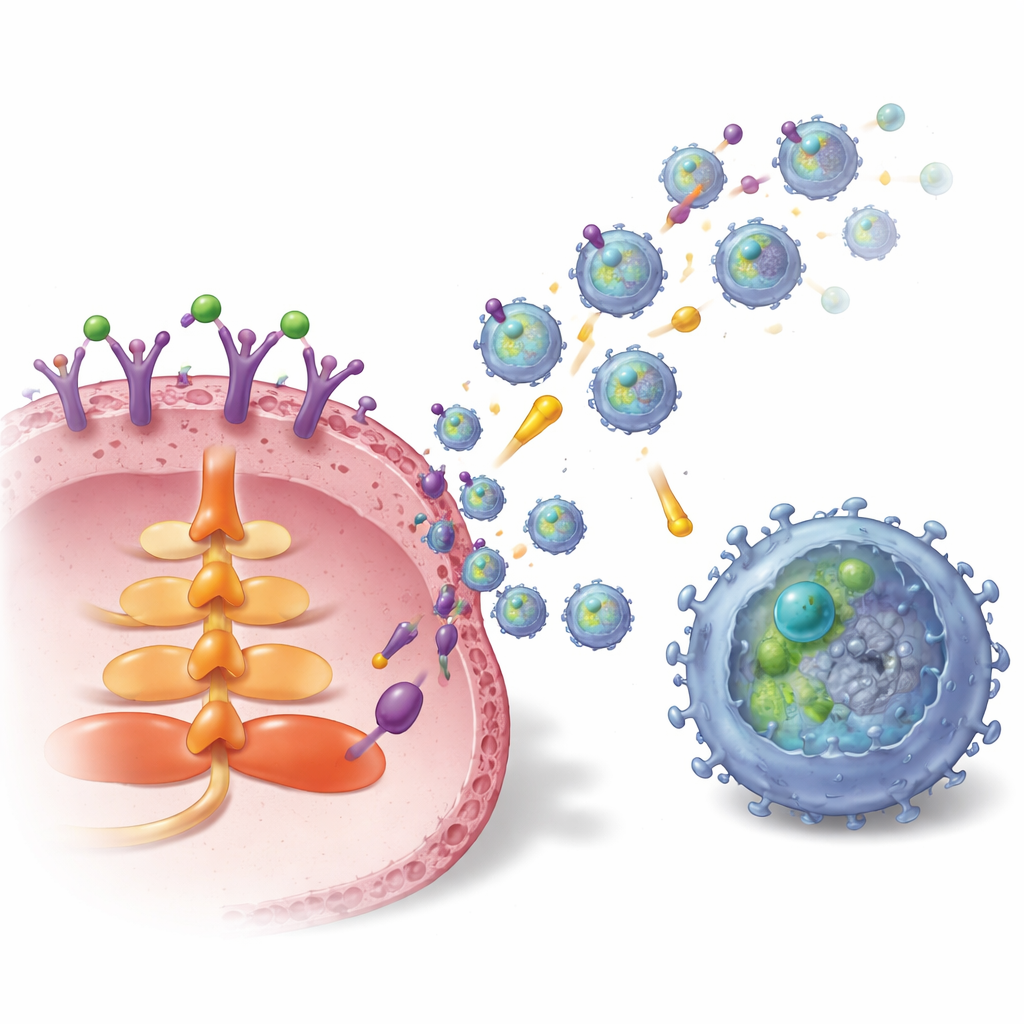
كيف تُحمَّل هذه الحويصلات وتُطلق من الورم
قامت الدراسة بعد ذلك برسم الخريطة الداخلية التي تربط S1P بإنتاج الإكسوسومات وتحميل TGFBR2. أدى تنشيط مستقبل محدد لـ S1P على خلايا سرطان الثدي، المسمى S1P1، إلى تشغيل مسار الإشارة AKT وبروتين نقل يُدعى Rab27a، وكلاهما ضروريان لإطلاق الإكسوسومات. في الوقت نفسه، عزز S1P1 كمية واستقرار TGFBR2 داخل خلايا السرطان. حدث ذلك بطريقتين: أولًا عن طريق تفعيل عامل النسخ LEF1 الذي يزيد من نسخ جين TGFBR2، وثانيًا برفع مستويات إنزيم إزالة اليوبكويتين، USP8، عبر مسار الإشارة ERK–CREB1. يبطئ USP8 تحلل TGFBR2، مما يسمح بتراكم المزيد من المستقبل ليُحمل داخل الإكسوسومات. في عينات أورام ثدي من مرضى، كان كل من S1P1 وTGFBR2 أعلى في نسيج الورم وفي الإكسوسومات المشتقة من الورم مقارنة بالنسيج الطبيعي المجاور، وكان ارتفاع TGFBR2 على الإكسوسومات مرتبطًا بوجود المزيد من خلايا CD8 المتعبة.
ماذا يعني هذا للمرضى
للغير متخصص، الرسالة الأساسية هي أن بعض سرطانات الثدي تخلق حمامًا كيميائيًا غنيًا بـ S1P يوجه خلايا الورم لإخراج حويصلات دقيقة محملة بمستقبل، TGFBR2، يطفئ خلايا CD8. تعمل هذه الحويصلات كطرود متخفية تعيد برمجة خلايا القتل المجاورة لتصبح بطيئة ومتساهلة تجاه الورم. من خلال تحديد سلسلة الأحداث S1P–S1P1–TGFBR2، بما في ذلك المفاتيح الداخلية التي تتحكم في إطلاق الإكسوسومات وتراكم المستقبل، تشير هذه الدراسة إلى عدة أهداف دوائية جديدة. قد يقلل تثبيط إشارة S1P أو حجب S1P1 أو منع وصول TGFBR2 إلى الإكسوسومات أو تثبيته عليها من إجهاد خلايا CD8 ويجعل العلاجات المناعية الحالية أكثر فعالية لمرضى سرطان الثدي.
الاستشهاد: Bhoumick, A., Ghosh, A., Singh, A. et al. Sphingosine-1-phosphate promotes CD8 T cell exhaustion in breast cancer via exosomal transfer of TGFBR2. Cell Death Dis 17, 278 (2026). https://doi.org/10.1038/s41419-026-08523-5
الكلمات المفتاحية: المناعة المناعية لسرطان الثدي, إجهاد خلايا T CD8, سفنغوزين-1-فوسفات, الحويصلات النَفْسَجِيَّة (إكسوسومات), إشارة TGFBR2