Clear Sky Science · ru
Сфингозин-1-фосфат способствует истощению CD8 Т-клеток при раке молочной железы посредством экзосомного переноса TGFBR2
Почему это важно для лечения рака
Многие современные противораковые терапии направлены на активацию собственной иммунной системы организма, особенно киллерных CD8 Т-клеток, для атаки опухолей. Тем не менее в ряде случаев рака молочной железы эти клетки истощаются и перестают эффективно действовать — состояние, известное как истощение, — поэтому иммунотерапия часто дает лишь скромные результаты. В этом исследовании обнаружен ранее не распознанный путь, с помощью которого опухоли молочной железы химически «усыпляют» CD8 Т-клетки на расстоянии, что выявляет новый сигнальный маршрут, который можно заблокировать, чтобы повысить эффективность существующих иммунотерапий.
Жироподобная молекула, формирующая опухолевое окружение
Исследователи сосредоточились на сфингозин-1-фосфате (S1P) — жироподобной сигнальной молекуле, содержание которой повышено при раке молочной железы. Известно, что S1P способствует росту сосудов в опухолях, их метастазированию и устойчивости к лечению. В этой работе команда задала вопрос, помогает ли S1P также обезвредить CD8 Т-клетки в микроокружении опухоли. Когда человеческие раковые клетки молочной железы выращивали в присутствии S1P, а затем совместно культивировали с человеческими CD8 Т-клетками, Т-клетки делились значительно реже, даже при отсутствии физического контакта с раковыми клетками. Это подавление без контакта указывало на то, что опухолевые клетки выделяют в культуру частицы, переносящие сигналы.
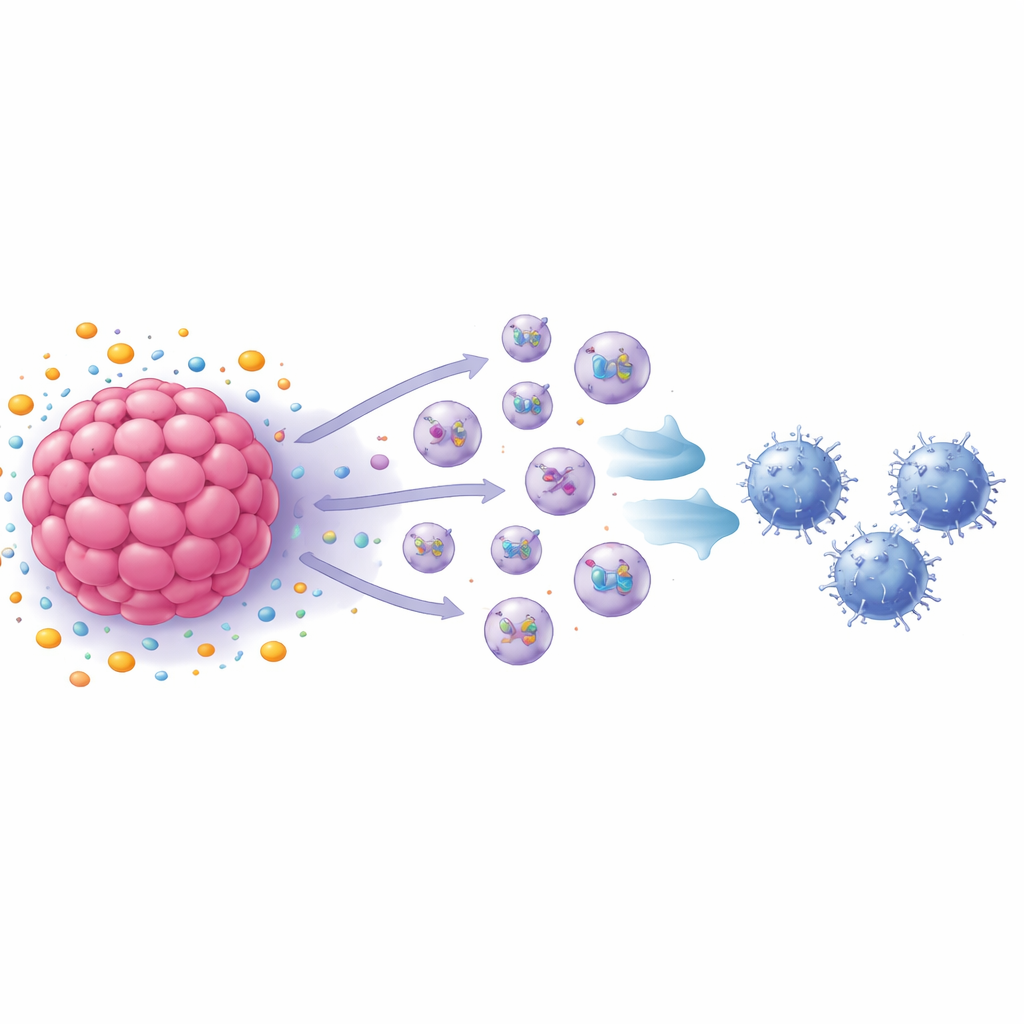
Крошечные везикулы как носители иммунного подавления
Далее группа обратила внимание на экзосомы — везикулы наномасштаба, которые клетки выбрасывают и которые переносят белки и другие молекулы к отдаленным приемникам. Блокирование образования экзосом в значительной степени восстановило пролиферацию CD8 Т-клеток, а анализ показал, что раковые клетки, обработанные S1P, выделяли значительно больше экзосом, чем необработанные. Когда эти экзосомы добавляли непосредственно к активированным CD8 Т-клеткам, пролиферация Т-клеток замедлялась, и они начинали демонстрировать признаки истощения, включая несколько поверхностных и внутриклеточных маркеров, связанных со «уставшими» иммунными клетками. В экспериментах на животных экзосомы от мышиных раковых клеток молочной железы, обработанных S1P, ускоряли рост опухолей и увеличивали долю истощенных CD8 Т-клеток в опухолях, тогда как экзосомы от клеток, лишенных ключевого рецептора, имели противоположный эффект.
Рецептор, упакованный в экзосомы, наносит ущерб
Изучая, что делает эти экзосомы такими вредоносными, ученые исследовали иммунно-связанные белки, обогащенные в их грузах. Они обнаружили, что один белок, рецептор трансформирующего фактора b2 (TGFBR2), сильно увеличивался в экзосомах после обработки S1P, тогда как другой известный контрольный белок, PD-L1, не был повышен. Экзосомы сливались с CD8 Т-клетками и доставляли TGFBR2 на поверхность Т-клеток, фактически обеспечивая Т-клетки дополнительной копией рецептора, который запускает внутриклеточные программы истощения. Когда команда блокировала TGFBR2 на экзосомах антителом или снижала его уровень в раковых клетках, экзосомы больше не могли подавлять активность Т-клеток или вызывать маркеры истощения, и CD8 Т-клетки восстанавливали способность вырабатывать ключевые молекулы для атаки.
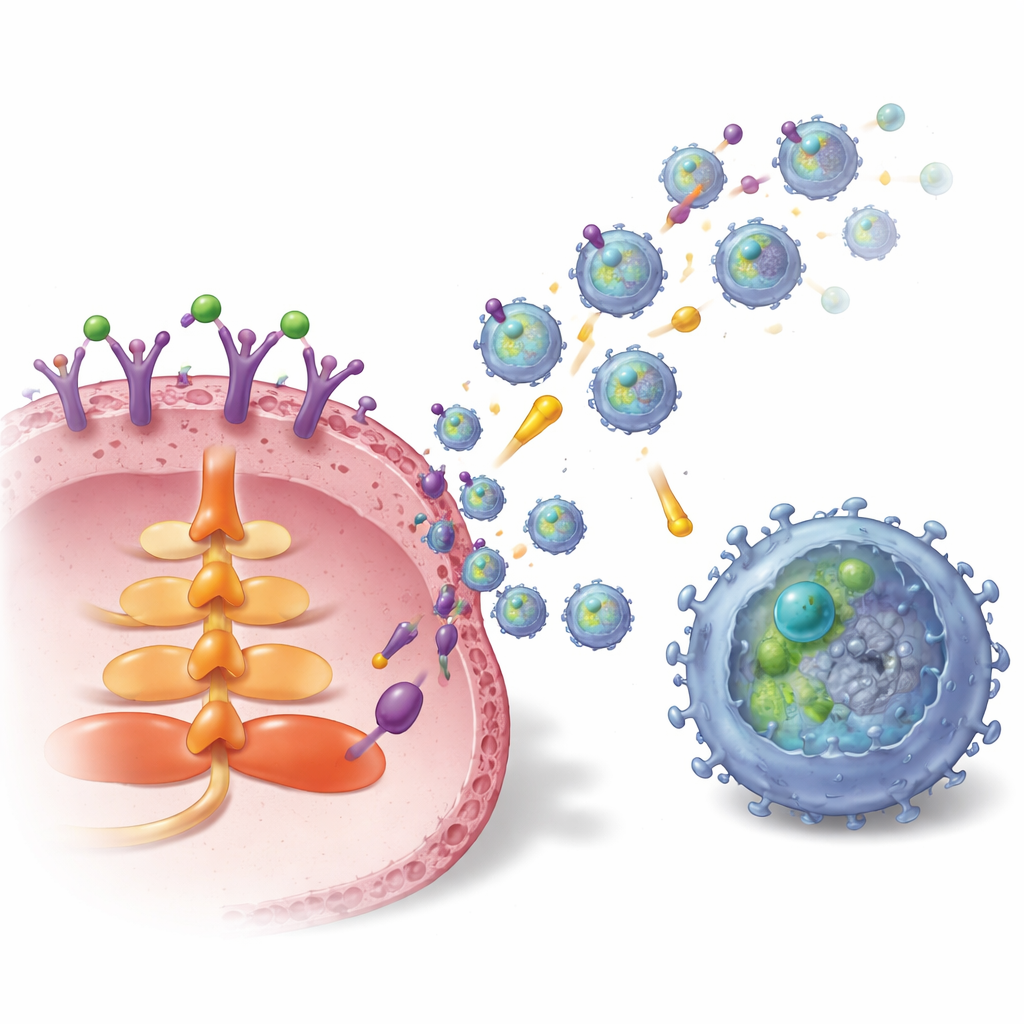
Как опухоль формирует и отсылает эти везикулы
В исследовании затем картировали внутренние механизмы, связывающие S1P с образованием экзосом и загрузкой TGFBR2. Активация определенного рецептора S1P на раковых клетках молочной железы, называемого S1P1, запускала сигнальный путь AKT и белок траффика Rab27a, которые оба необходимы для выделения экзосом. Одновременно S1P1 повышал количество и устойчивость TGFBR2 внутри раковых клеток. Это происходило двумя способами: во‑первых, через активацию транскрипционного фактора LEF1, который увеличивает экспрессию гена TGFBR2, и во‑вторых, через повышение уровня деубиквитиназы USP8 посредством сигнального пути ERK–CREB1. USP8 замедляет разрушение TGFBR2, позволяя рецептору накапливаться и упаковываться в экзосомы. В образцах опухолей молочной железы у пациентов и S1P1, и TGFBR2 были выше в опухолевой ткани и в экзосомах, полученных из опухолей, по сравнению с соседней нормальной тканью, а повышенное содержание TGFBR2 в экзосомах коррелировало с большим числом истощенных CD8 Т-клеток.
Что это означает для пациентов
Для неспециалиста основная мысль такова: некоторые опухоли молочной железы создают химическое «окружение», богатое S1P, которое заставляет раковые клетки выпускать крошечные везикулы, нагруженные рецептором TGFBR2, отключающим CD8 Т-клетки. Эти везикулы действуют как скрытые посылки, перенастраивающие киллерные клетки, делая их вялыми и терпимыми к опухоли. Выявив цепочку событий S1P–S1P1–TGFBR2, включая внутренние переключатели, контролирующие выделение экзосом и накопление рецептора, эта работа предлагает несколько новых мишеней для лекарств. Ингибирование сигнальной передачи S1P, блокирование S1P1 или предотвращение доставки и стабилизации TGFBR2 в экзосомах может снизить истощение CD8 Т-клеток и сделать существующие иммунотерапии более эффективными для пациентов с раком молочной железы.
Цитирование: Bhoumick, A., Ghosh, A., Singh, A. et al. Sphingosine-1-phosphate promotes CD8 T cell exhaustion in breast cancer via exosomal transfer of TGFBR2. Cell Death Dis 17, 278 (2026). https://doi.org/10.1038/s41419-026-08523-5
Ключевые слова: иммунотерапия рака молочной железы, истощение CD8 Т-клеток, сфингозин-1-фосфат, экзосомы, сигнализация TGFBR2