Clear Sky Science · tr
Sfingosin-1-fosfat, ekzosomal TGFBR2 transferi yoluyla meme kanserinde CD8 T hücre tükenmesini teşvik ediyor
Neden Kanser Tedavisi İçin Önemli
Çok sayıda modern kanser tedavisi, özellikle tümörü hedef alan CD8 öldürücü T hücrelerini harekete geçirerek vücudun kendi bağışıklık sistemini serbest bırakmayı amaçlar. Yine de birçok meme kanserinde bu hücreler yorulur ve etkisiz hale gelir; bu durum tükenme olarak adlandırılır ve immünoterapi çoğu zaman sınırlı etki gösterir. Bu çalışma, meme tümörlerinin CD8 T hücrelerini uzaktan kimyasal olarak “sedasyon” yoluyla etkisiz hâle getirdiği daha önce gizli bir mekanizmayı ortaya koyuyor ve mevcut immünoterapilerin etkinliğini artırmak üzere engellenebilecek yeni bir sinyal yolunu gösteriyor.
Tümör Ortamını Şekillendiren Bir Yağ Molekülü
Araştırmacılar, meme kanserinde yüksek düzeylerde bulunan yağ benzeri bir haberci molekül olan sfingosin-1-fosfat (S1P) üzerine odaklandı. S1P’nin tümörlerin damar oluşturmasına, yayılıma ve tedaviye direnç göstermesine yardımcı olduğu zaten biliniyordu. Burada ekip, S1P’nin tümör çevresindeki CD8 T hücrelerini devre dışı bırakıp bırakmadığını sordu. İnsan meme kanseri hücrelerini S1P ile yetiştirip ardından insan CD8 T hücreleriyle ko-kültürlediklerinde, T hücreleri fiziksel temas olmasa bile çok daha az bölündü. Bu temassız baskılanma, tümör hücrelerinin kültüre mesaj taşıyan partiküller salgıladığını işaret ediyordu.
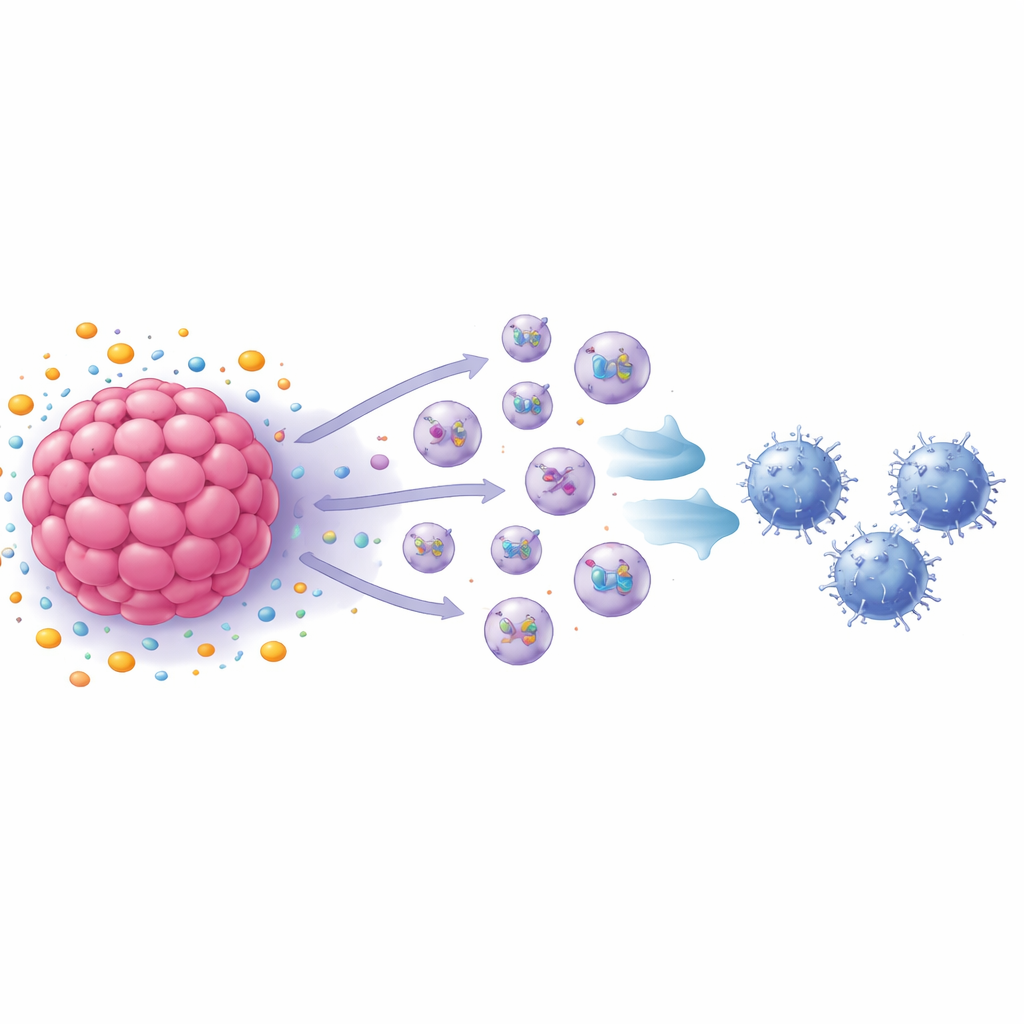
Bağışıklık Baskısının Elçileri Olarak Minik Veziküller
Grup daha sonra hücrelerin proteini ve diğer molekülleri uzak hedeflere taşıyan nanometre ölçeğindeki vezikülleri olan ekzosomlara yöneldi. Ekzosom üretimini engellemek CD8 T hücre büyümesini büyük ölçüde geri getirdi ve analiz, S1P ile muamele edilmiş meme kanseri hücrelerinin tedavi edilmemiş hücrelere kıyasla çok daha fazla ekzosom saldığını gösterdi. Bu ekzosomlar doğrudan aktive edilmiş CD8 T hücrelerine eklendiğinde, T hücreleri proliferasyonlarını yavaşlattı ve yüzey ve içsel belirteçler de dahil olmak üzere tükenmeye özgü özellikler göstermeye başladı. Hayvan deneylerinde, S1P ile muamele edilmiş fare meme kanseri hücrelerinden elde edilen ekzosomlar tümör büyümesini hızlandırdı ve tümör içindeki tükenmiş CD8 T hücrelerini artırdı; anahtar bir reseptörü eksik olan hücrelerin ekzosomları ise ters etki gösterdi.
Hasarı Yapan Ekzosomlara Paketlenmiş Bir Reseptör
Bu ekzosomları zararlı kılan şeyi araştırırken, bilim insanları kargolarında zenginleşmiş immünle ilgili proteinlere baktı. Sfingosin-1-fosfat tedavisinden sonra ekzosomlarda dönüşüm faktörü beta reseptörü 2 (TGFBR2) adlı bir proteinin güçlü şekilde arttığını, oysa daha iyi bilinen kontrol noktası proteini PD-L1’in artmadığını buldular. Ekzosomlar CD8 T hücreleriyle füzyona girip T hücre yüzeyine TGFBR2 teslim ederek, hücre içinde tükenme programlarını tetikleyen ilave bir reseptör kopyasıyla T hücreleri donatmış oldu. Ekip, ekzosomlardaki TGFBR2’yi bir antikorla bloke ettiğinde veya kanser hücrelerindeki seviyesini azalttığında, ekzosomlar artık T hücre aktivitesini baskılayamadı veya tükenme belirteçlerini indükleyemedi ve CD8 T hücreleri temel saldırı moleküllerini üretme yeteneklerini geri kazandı.
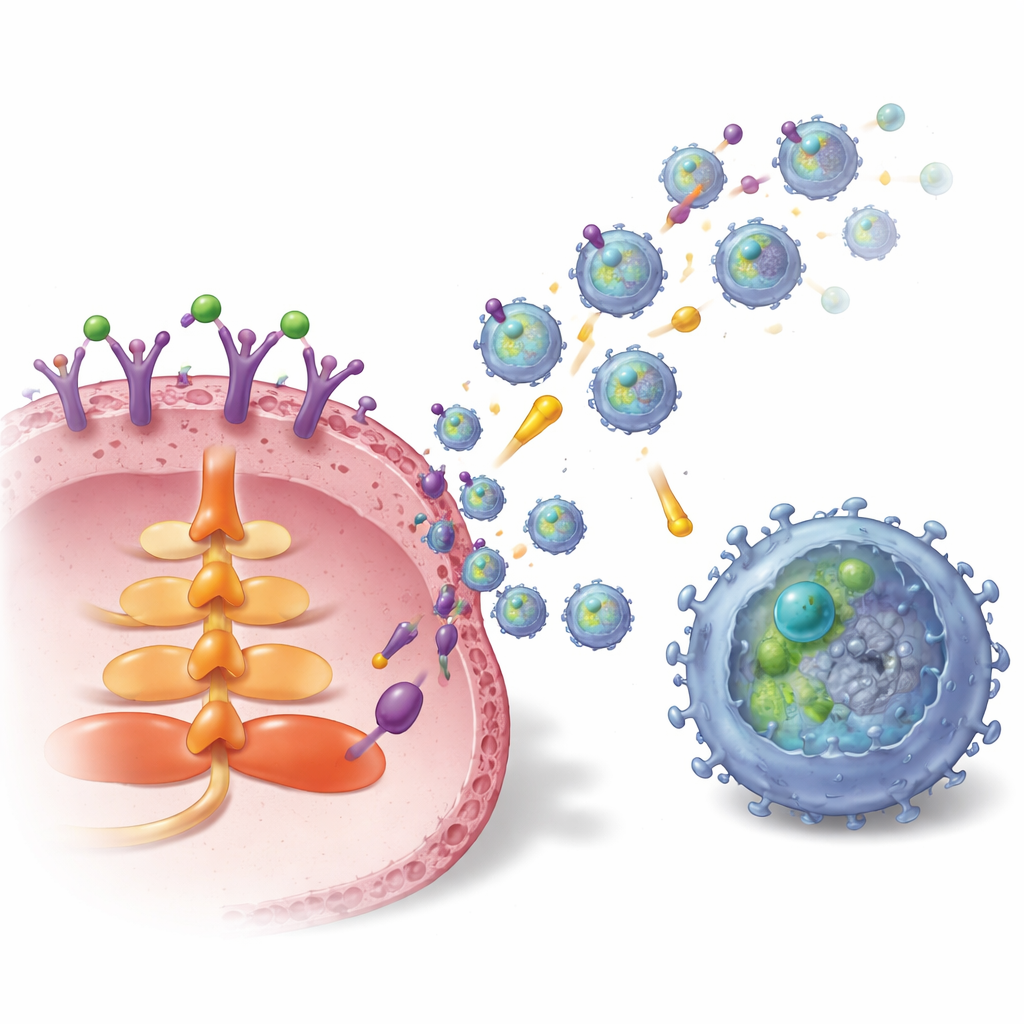
Tümörün Bu Vezikülleri Nasıl Paketleyip Fırlattığı
Çalışma daha sonra S1P’yi ekzosom üretimine ve TGFBR2 yüklemesine bağlayan iç devreyi haritalandırdı. Meme kanseri hücrelerinde S1P1 adı verilen spesifik bir S1P reseptörünün aktivasyonu AKT sinyal yolunu ve ekzosom salınımı için kritik olan taşıma proteini Rab27a’yı etkinleştirdi. Aynı zamanda S1P1, kanser hücreleri içindeki TGFBR2 miktarını ve stabilitesini artırdı. Bunu iki yolla yaptı: birincisi TGFBR2 gen ekspresyonunu artıran bir transkripsiyon faktörü olan LEF1’i açarak; ikincisi ise ERK–CREB1 sinyal yoluyla bir deubikuitinaz enzim olan USP8 seviyelerini yükselterek. USP8, TGFBR2’nin yıkımını yavaşlatarak reseptörün daha fazla birikmesine ve ekzosomlara paketlenmesine izin verdi. Hastalardan alınan meme tümörü örneklerinde hem S1P1 hem de TGFBR2, çevre normal dokuya kıyasla tümör dokusunda ve tümörden türetilen ekzosomlarda daha yüksekti ve ekzosomlardaki daha yüksek TGFBR2, daha fazla tükenmiş CD8 T hücresi ile koreleydi.
Hastalar İçin Anlamı
Uzman olmayan biri için ana mesaj şudur: Bazı meme kanserleri, tümör hücrelerini TGFBR2 ile dolu küçük veziküller pompalamaya yönlendiren S1P açısından zengin bir kimyasal ortam yaratır; bu reseptör CD8 T hücrelerini kapatan programları tetikler. Bu veziküller, çevredeki öldürücü hücreleri yavaş ve tümöre toleranslı hale getiren gizli paketler gibi davranır. S1P–S1P1–TGFBR2 olay zincirini, ekzosom salınımını ve reseptör birikimini kontrol eden iç anahtarları belirleyerek, bu çalışma birkaç yeni ilaç hedefi öneriyor. S1P sinyalini inhibe etmek, S1P1’i bloklamak veya TGFBR2’nin ekzosomlara ulaşmasını ya da stabilizasyonunu engellemek, CD8 T hücresi tükenmesini azaltabilir ve mevcut immünoterapilerin meme kanseri hastaları için daha etkili olmasını sağlayabilir.
Atıf: Bhoumick, A., Ghosh, A., Singh, A. et al. Sphingosine-1-phosphate promotes CD8 T cell exhaustion in breast cancer via exosomal transfer of TGFBR2. Cell Death Dis 17, 278 (2026). https://doi.org/10.1038/s41419-026-08523-5
Anahtar kelimeler: meme kanseri immünoterapisi, CD8 T hücre tükenmesi, sfingosin-1-fosfat, ekzosomlar, TGFBR2 sinyalleşmesi