Clear Sky Science · sv
Sphingosine-1-fosfat främjar utmattning av CD8 T‑celler vid bröstcancer via exosomal överföring av TGFBR2
Varför detta spelar roll för cancerbehandling
Många moderna cancerbehandlingar syftar till att frigöra kroppens eget immunsystem, särskilt mördande CD8 T‑celler, för att angripa tumörer. Ändå blir dessa celler i många bröstcancerformer trötta och ineffektiva — ett tillstånd som kallas utmattning — och immunterapi fungerar ofta bara måttligt. Denna studie avslöjar en tidigare dold mekanism där brösttumörer kemiskt ”bedövar” CD8 T‑celler på avstånd och visar en ny signalväg som kan blockeras för att hjälpa befintliga immunterapier att fungera bättre.
En fettmolekyl som formar tumörens omgivning
Forskarna fokuserade på sphingosine‑1‑fosfat (S1P), en fettliknande signalmolekyl som finns i höga nivåer vid bröstcancer. S1P är redan känd för att hjälpa tumörer att bilda blodkärl, sprida sig och motstå behandling. Här undersökte teamet om S1P också hjälper tumörer att oskadliggöra CD8 T‑celler i sin omgivning. När de odlade humana bröstcancerceller med S1P och sedan samodlade dem med humana CD8 T‑celler, delade sig T‑cellerna mycket mindre, även när de inte kunde röra vid cancercellerna. Denna kontaktfria suppression antydde att tumörcellerna frigav någon sorts meddelandebärande partiklar i kulturen.
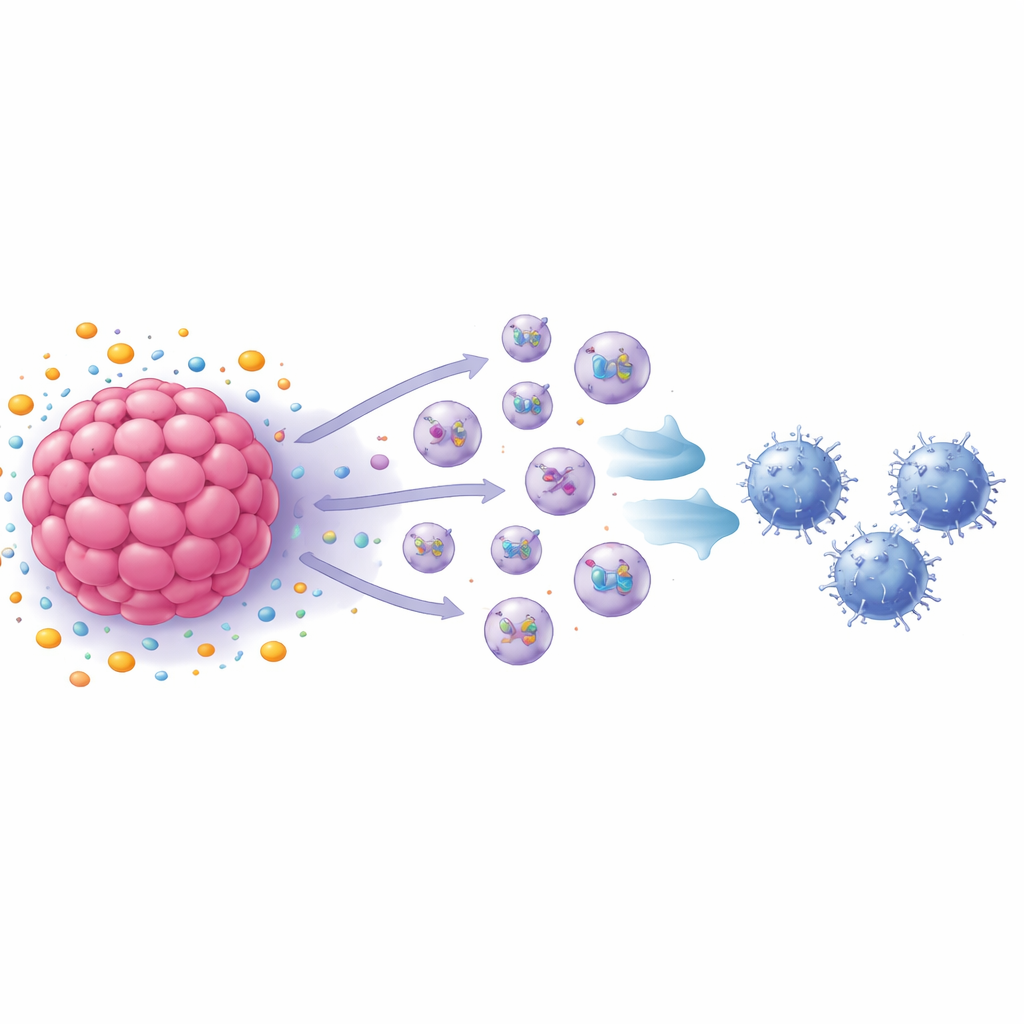
Små vesiklar som budbärare för immunundertryck
Gruppen vände sig därefter till exosomer — nanometerstora vesiklar som celler avsöndrar och som transporterar proteiner och andra molekyler till avlägsna mål. Genom att blockera exosomproduktionen återställdes till stor del CD8 T‑cellernas tillväxt, och analyser visade att S1P‑behandlade bröstcancerceller släppte ut betydligt fler exosomer än obehandlade celler. När dessa exosomer tillsattes direkt till aktiverade CD8 T‑celler saktade T‑cellernas proliferation ner och de började uppvisa kännetecken för utmattning, inklusive flera ytoch inre markörer för uttömda immunceller. I djurförsök påskyndade exosomer från S1P‑behandlade musbröstcancerceller tumörtillväxten och ökade andelen utmattade CD8 T‑celler i tumörerna, medan exosomer från celler utan en nyckelreceptor hade motsatt effekt.
En receptor packad i exosomerna orsakar skadan
För att ta reda på vad som gjorde dessa exosomer så skadliga granskade forskarna immuncellerelaterade proteiner som var rikliga i deras last. De fann att ett protein, omvandlande tillväxtfaktor‑beta‑receptor 2 (TGFBR2), ökade kraftigt på exosomer efter S1P‑behandling, medan ett annat välkänt kontrollpunktprotein, PD‑L1, inte gjorde det. Exosomerna smälte samman med CD8 T‑celler och levererade TGFBR2 till T‑cellens yta, vilket i praktiken utrustade T‑cellerna med en extra kopia av en receptor som driver utmattningsprogram inuti cellen. När teamet blockerade TGFBR2 på exosomerna med en antikropp eller minskade dess nivåer i cancercellerna, kunde exosomerna inte längre undertrycka T‑cellernas aktivitet eller inducera utmattningsmarkörer, och CD8 T‑celler återfick förmågan att producera viktiga angreppsmolekyler.
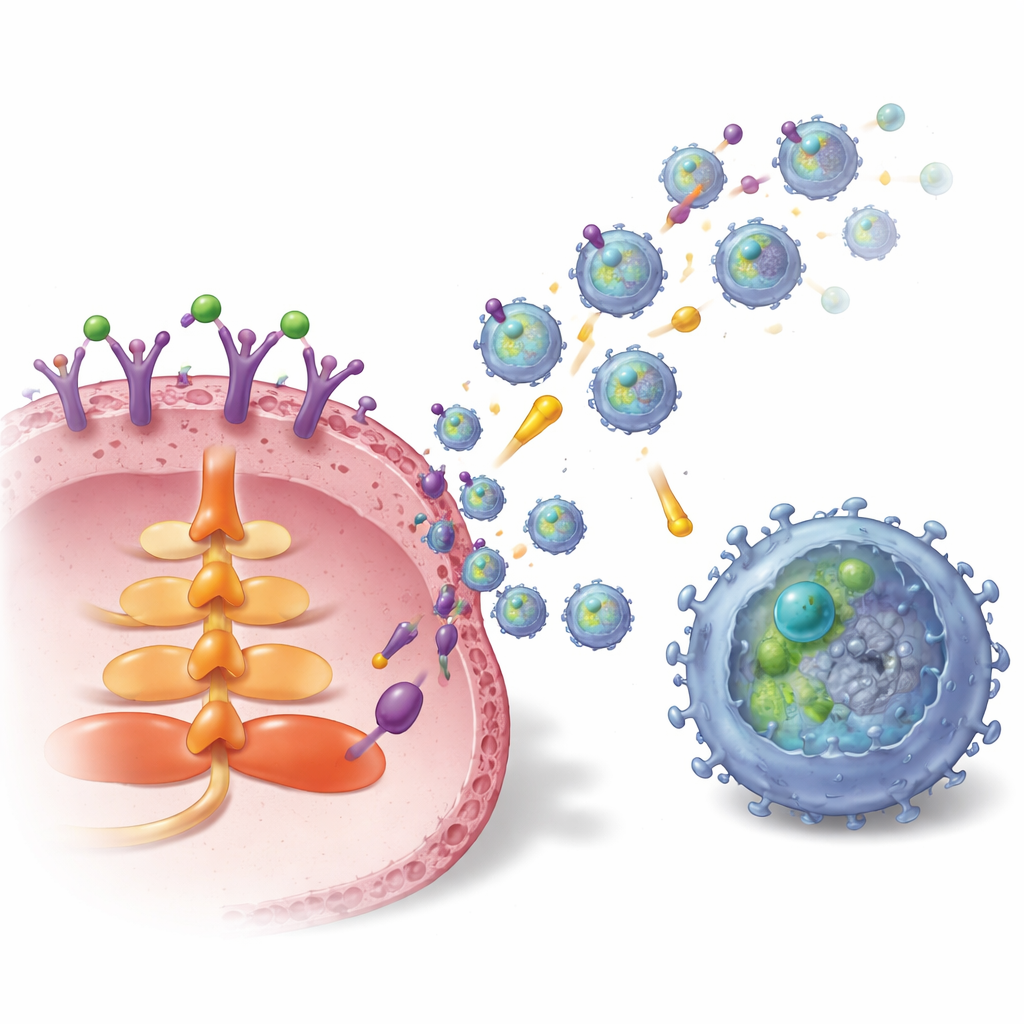
Hur tumören laddar och skickar iväg dessa vesiklar
Studien kartlade sedan den inre kopplingen som förenar S1P med exosomproduktion och TGFBR2‑packning. Aktivering av en specifik S1P‑receptor på bröstcancerceller, kallad S1P1, satte igång AKT‑signalvägen och ett trafikprotein som heter Rab27a — båda avgörande för exosomfrisättning. Samtidigt ökade S1P1 mängden och stabiliteten av TGFBR2 inne i cancercellerna. Detta skedde på två sätt: dels genom att slå på en transkriptionsfaktor, LEF1, som ökar TGFBR2‑genes uttryck, och dels genom att höja nivåerna av en deubikvitinas‑enzym, USP8, via en ERK–CREB1‑signalväg. USP8 bromsar nedbrytningen av TGFBR2, vilket tillåter mer receptor att ackumuleras och paketeras i exosomer. I brösttumörprover från patienter var både S1P1 och TGFBR2 högre i tumörvävnad och i tumör‑härledda exosomer än i intilliggande normalvävnad, och högre TGFBR2 på exosomer korrelerade med fler utmattade CD8 T‑celler.
Vad detta betyder för patienter
För icke‑specialisten är huvudbudskapet att vissa bröstcancerformer skapar ett kemiskt bad rikt på S1P som instruerar tumörcellerna att pumpa ut små vesiklar fyllda med en receptor, TGFBR2, som stänger av CD8 T‑celler. Dessa vesiklar fungerar som stealth‑paket som omprogrammerar närliggande mördarceller till att bli slöa och toleranta mot tumören. Genom att peka ut S1P–S1P1–TGFBR2‑kedjan av händelser, inklusive de inre brytarna som styr exosomfrisättning och receptoruppbyggnad, föreslår detta arbete flera nya läkemedelsmål. Att hämma S1P‑signalering, blockera S1P1 eller hindra TGFBR2 från att nå eller stabiliseras på exosomer skulle kunna minska utmattning av CD8 T‑celler och göra befintliga immunterapier mer effektiva för bröstcancerpatienter.
Citering: Bhoumick, A., Ghosh, A., Singh, A. et al. Sphingosine-1-phosphate promotes CD8 T cell exhaustion in breast cancer via exosomal transfer of TGFBR2. Cell Death Dis 17, 278 (2026). https://doi.org/10.1038/s41419-026-08523-5
Nyckelord: immunterapi mot bröstcancer, utmattning av CD8 T‑celler, sphingosine-1-fosfat, exosomer, TGFBR2‑signalering