Clear Sky Science · es
La esfingosina-1-fosfato promueve el agotamiento de células T CD8 en el cáncer de mama mediante la transferencia exosomal de TGFBR2
Por qué importa para el tratamiento del cáncer
Muchas terapias modernas contra el cáncer buscan liberar al propio sistema inmunitario del cuerpo, en particular a las células T CD8 citotóxicas, para que ataquen los tumores. Sin embargo, en muchos cánceres de mama estas células se vuelven fatigadas e ineficaces, un estado conocido como agotamiento, y la inmunoterapia suele funcionar solo de forma moderada. Este estudio desvela una vía previamente oculta por la cual los tumores mamarios “sedan” químicamente a las células T CD8 a distancia, revelando una nueva ruta de señalización que podría bloquearse para mejorar la eficacia de las inmunoterapias existentes.
Una molécula lipídica que moldea el vecindario tumoral
Los investigadores se centraron en la esfingosina-1-fosfato (S1P), una molécula señalizadora con carácter lipídico que se encuentra a niveles elevados en el cáncer de mama. Ya se sabe que la S1P ayuda a los tumores a formar vasos sanguíneos, a diseminarse y a resistir tratamientos. Aquí, el equipo investigó si la S1P también ayuda a los tumores a desactivar a las células T CD8 en su entorno. Cuando cultivaron células humanas de cáncer de mama con S1P y luego las co-cultivaron con células T CD8 humanas, las T se dividieron mucho menos, incluso cuando no podían tocar físicamente las células tumorales. Esta supresión sin contacto sugirió que las células tumorales estaban liberando algún tipo de partículas portadoras de mensajes hacia el cultivo.
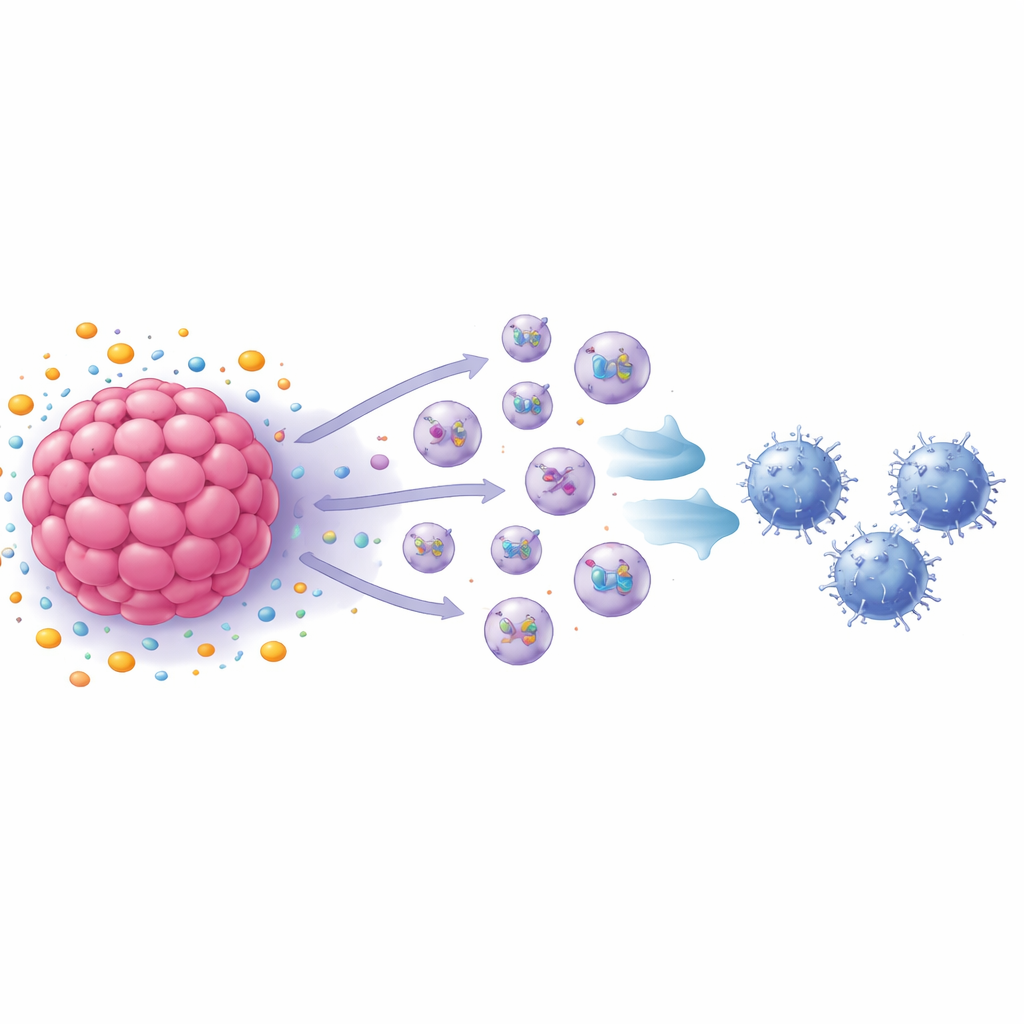
Vesículas diminutas como mensajeras de supresión inmune
El grupo se centró a continuación en los exosomas: vesículas de escala nanométrica desprendidas por las células que transportan proteínas y otras moléculas hacia objetivos distantes. Bloquear la producción de exosomas restauró en gran medida el crecimiento de las células T CD8, y el análisis mostró que las células de cáncer de mama tratadas con S1P liberaron muchos más exosomas que las células no tratadas. Cuando estos exosomas se añadieron directamente a células T CD8 activadas, las T redujeron su proliferación y empezaron a mostrar rasgos de agotamiento, incluidos varios marcadores de superficie e internos asociados a células inmunitarias agotadas. En experimentos con animales, los exosomas procedentes de células de cáncer de mama de ratón tratadas con S1P aceleraron el crecimiento tumoral e incrementaron el número de células T CD8 agotadas dentro de los tumores, mientras que los exosomas de células que carecían de un receptor clave tuvieron el efecto opuesto.
Un receptor empaquetado en exosomas causa el daño
Al profundizar en lo que hacía tan dañinos a estos exosomas, los científicos examinaron proteínas relacionadas con la inmunidad enriquecidas en su carga. Encontraron que una proteína, el receptor del factor de crecimiento transformante beta 2 (TGFBR2), aumentó fuertemente en los exosomas tras el tratamiento con S1P, mientras que otra proteína punto de control bien conocida, PD-L1, no lo hizo. Los exosomas se fusionaron con las células T CD8 y entregaron TGFBR2 a la superficie de las T, equipando efectivamente a las células T con una copia adicional de un receptor que impulsa programas de agotamiento dentro de la célula. Cuando el equipo bloqueó TGFBR2 en los exosomas con un anticuerpo o redujo sus niveles en las células tumorales, los exosomas ya no pudieron suprimir la actividad de las T ni inducir marcadores de agotamiento, y las células T CD8 recuperaron su capacidad de producir moléculas clave de ataque.
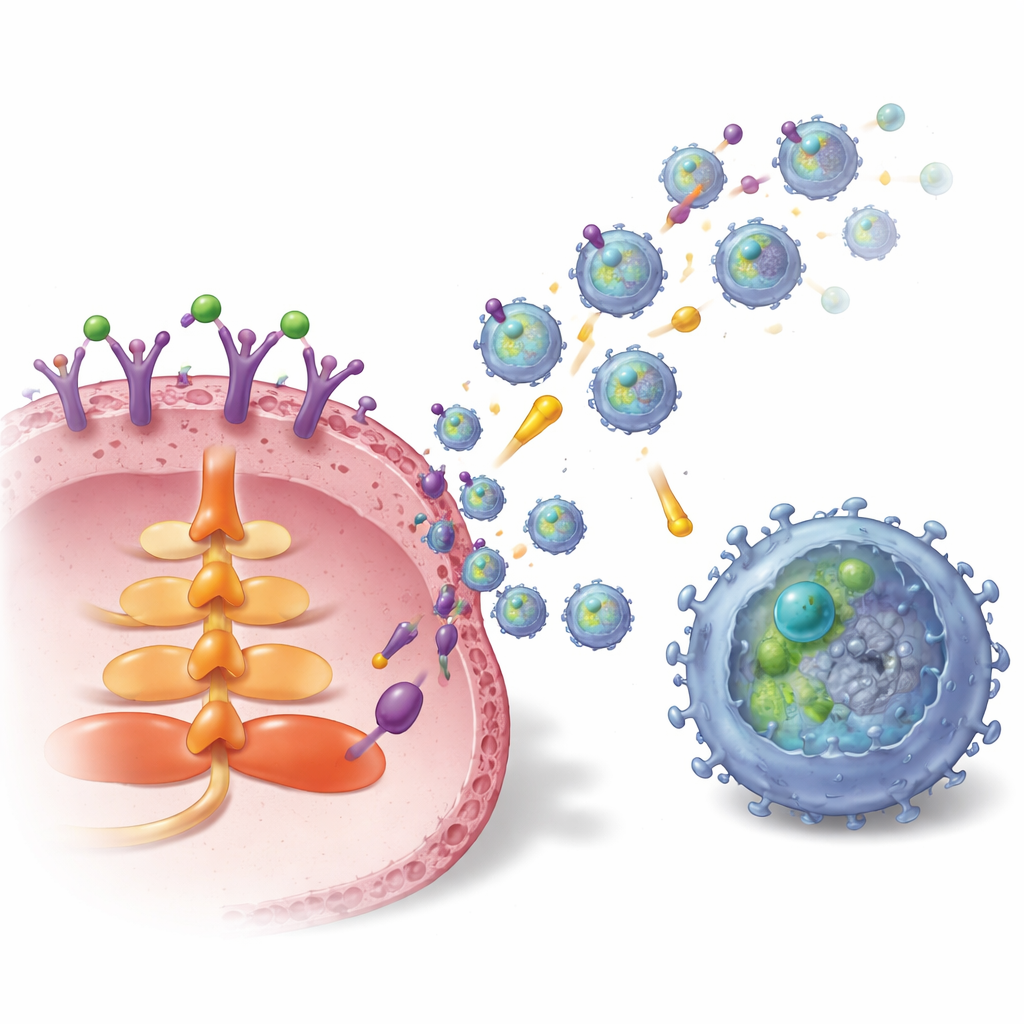
Cómo el tumor carga y lanza estas vesículas
El estudio trazó luego el cableado interno que conecta la S1P con la producción de exosomas y la incorporación de TGFBR2. La activación de un receptor específico de S1P en las células de cáncer de mama, llamado S1P1, activó la vía de señalización AKT y una proteína de tráfico llamada Rab27a, ambas cruciales para la liberación de exosomas. Al mismo tiempo, S1P1 aumentó la cantidad y la estabilidad de TGFBR2 dentro de las células tumorales. Lo hizo de dos maneras: primero activando un factor de transcripción, LEF1, que incrementa la expresión del gen TGFBR2, y segundo elevando los niveles de una desubiquitinasa, USP8, a través de una ruta de señalización ERK–CREB1. USP8 ralentiza la degradación de TGFBR2, permitiendo que se acumule más receptor y se empaquete en exosomas. En muestras de tumores mamarios de pacientes, tanto S1P1 como TGFBR2 fueron mayores en tejido tumoral y en exosomas derivados del tumor que en el tejido normal cercano, y una mayor cantidad de TGFBR2 en exosomas se correlacionó con más células T CD8 agotadas.
Qué significa esto para los pacientes
Para un no especialista, el mensaje central es que ciertos cánceres de mama crean un ambiente químico rico en S1P que indica a las células tumorales que expulsen diminutas vesículas cargadas con un receptor, TGFBR2, que apaga a las células T CD8. Estas vesículas actúan como paquetes encubiertos que reprograman a las células asesinas próximas para que se vuelvan lentas y tolerantes con el tumor. Al identificar la cadena de eventos S1P–S1P1–TGFBR2, incluidas las palancas internas que controlan la liberación de exosomas y la acumulación del receptor, este trabajo sugiere varios nuevos objetivos farmacológicos. Inhibir la señalización de S1P, bloquear S1P1 o impedir que TGFBR2 alcance o se estabilice en los exosomas podría reducir el agotamiento de las células T CD8 y aumentar la eficacia de las inmunoterapias existentes para pacientes con cáncer de mama.
Cita: Bhoumick, A., Ghosh, A., Singh, A. et al. Sphingosine-1-phosphate promotes CD8 T cell exhaustion in breast cancer via exosomal transfer of TGFBR2. Cell Death Dis 17, 278 (2026). https://doi.org/10.1038/s41419-026-08523-5
Palabras clave: inmunoterapia del cáncer de mama, agotamiento de células T CD8, esfingosina-1-fosfato, exosomas, señalización TGFBR2